 |
Главная |
Эпидемиология метаболического синдрома
|
из
5.00
|
По данным разных авторов, среди населения старше 30 лет его распространенность составляет 10
30%. Чаще болеют мужчины, у женщин распространенность возрастает в период менопаузы.
Высокая вариабельность распространенности метаболического синдрома по данным различных
исследований связана, в первую очередь, с недостаточно четкой, согласованной определенностью
диагностических критериев. Согласно анализу массивной базы данных, проведенному в США в
2001 году в соответствии с рекомендациями Образовательной программы США по холестерину,
распространенность метаболического синдрома среди взрослого населения составила 23.7% (24%
среди мужчин и 23.4% среди женщин). Согласно Российским данным от 2004 года, частота
встречаемости метаболического синдрома у мужчин 40-55 лет составляет 44.4%, у женщин той же
возрастной группы – 20.8%.
Этиология и патогенез. В этиопатогенезе МС выделяют две группы факторов: генетические и
средовые. Эпидемиологические исследования позволили сформулировать гипотезу
«экономичного (бережливого) генотипа» как основы его развития. Так, лица, проживающие в
неблагоприятных условиях, должны обладать максимальной способностью к накоплению энергии
в виде жировой ткани в благоприятный период. При смене условий среды на благоприятные,
генотип реализуется в нарушении толерантности к глюкозе (НТГ) или ожирении. Альтернативная
гипотеза носит название фетального программирования и указывает на большое влияние
внутриутробного питания в развитии МС. Сниженный вес при рождении является маркером
повышенного риска возникновения ИР. При проведении семейных исследований выявлено, что
снижение физической активности и высокоуглеводный характер питания являются главными
причинами того, что заболеваемость МС приобретает характер эпидемии. МС страдает около 25%
населения западных стран. Высокая частота встречаемости МС в некоторых этнических группах
доказывает существование генетической предрасположенности не только к частоте его
возникновения, но и к тяжести клинических проявлений.
Известно, что действие инсулина в организме направлено на накопление структурных и
энергетических материалов в клетках и тканях. Инсулин стимулирует образование гликогена,
синтез жиров и белка, способствует накоплению ионов натрия и калия внутри клеток. Наиболее
чувствительными к действию инсулина являются мышечная ткань, печень и жировая ткань.
Развивающаяся ИР способствует возникновению ГИ, которая способна длительно, в ряде случаев
до 15 лет, поддерживать нормогликемию. С истощением b-клеток поджелудочной железы
развивается ИР, а затем и СД. В условиях ГИ глюкоза метаболизируется в жирные кислоты (ЖК) с
последующим синтезом жиров и отложением их в жировой ткани. ЖК в повышенной
концентрации снижают активность липопротеидлипазы и других ферментов в тканях и усиливают
их резистентность к инсулину. Используя ЖК как энергосубстрат, печень начинает синтезировать
большое количество триглицеридов (ТГ). Снижается уровень липопротеинов высокой плотности
(ЛПВП) из-за ускорения их распада и замедления синтеза в условиях нарушенной активности
липопротеидлипазы. ГИ также способствует усилению синтеза липопротеинов очень низкой
плотности (ЛПОНП).
Получены доказательства метаболических связей между ИР и развитием абдоминального
ожирения. У больных с ожирением инсулинозависимые ткани не могут усваивать глюкозу при
нормальном содержании инсулина в организме. Контринсулярным гормоном является кортизол.
После тридцати лет снижается чувствительность гипоталамо-гипофизарной зоны к действию
кортизола, и компенсаторно возникает состояние гиперкортицизма [32]. Жировая ткань
абдоминальной области имеет высокую плотность рецепторов к кортизолу и относительно низкую
к инсулину. Всё это способствует развитию абдоминального типа ожирения и образованию
большого количества ЖК, поступающих непосредственно в портальную циркуляцию.
Гипертрофия адипоцитов приводит к уменьшению плотности рецепторов к инсулину на их
поверхности, тем самым усугубляя ИР.
Сама жировая ткань обладает эндокринной функцией, вырабатывая вещества, способные
вызывать ИР. Наиболее изучен в настоящее время гормон лептин, участвующий в регуляции
пищевого поведения и активности симпатической нервной системы. Установлена корреляция
между содержанием лептина в сыворотке крови, ИР и ГИ. Лептин вырабатывается в процессе
липогенеза и является стимулятором центра насыщения. При ожирении чувствительность
рецепторов к лептину в гипоталамусе снижается, несмотря на повышение его уровня в крови.
Эндокринный статус больных с МС характеризуется повышением уровня кортизола, тестостерона
(у женщин), норадреналина, снижением уровня прогестерона, тестостерона (у мужчин) и
соматотропного гормона. С ростом ГИ отмечается рост таких контринсулярных гормонах, как
глюкагон, тиреотропный гормон, тиреоидные гормоны и пролактин. Доказано патогенетическое
влияние этих гормонов на развитие МС.
Попытки установить единственный фактор, ответственный за развитие МС, привели к выделению
трёх равноценных компонентов: глюкозо-инсулиновая ассоциация, липидный компонент и
гипертензивный компонент. Активно изучаются и другие составляющие МС. Некоторые авторы
вводят в состав МС гиперандрогению у женщин, обеспечивающую высокий уровень свободного
тестостерона, гиперурикемию как индикатор метаболических сдвигов атеро- и диабетогенной
направленности. Всё это указывает на то, что МС - комплекс динамических нарушений, который,
имея в основе ИР и ожирение, может вызывать другие метаболические сдвиги или усугублять уже
имеющиеся.
Артериальная гипертензия (АГ) является одним из проявлений МС. Центральная нервная система
и почки сохраняют чувствительность к инсулину, что в условиях ГИ является фактором активации
симпатической нервной системы и повышения сосудистого тонуса. В условиях симпатикотонии
увеличивается фильтрация глюкозы клубочками почек, что приводит к усилению реабсорбции
натрия в проксимальных канальцах нефрона. В результате происходит задержка жидкости и
электролитов, часть из которых остаётся в сосудистой стенке.
Прямое действие инсулина в условиях ГИ также способствует уменьшению внутриклеточного калия и повышению кальция и натрия. В этих условиях чувствительность сосудистой стенки к прессорным воздействиям катехоламинов значительно возрастает. Развитию сопутствующей дисфункции эндотелия способствует недостаточная продукция оксида азота в сосудистой стенке и его инактивация. Этот эффект усиливается за счёт роста концентрации свободных радикалов в тканях и разрушения брадикинина. ГИ способствует ускорению пролиферации гладкомышечных клеток сосудистой стенке и гипертрофии левого желудочка сердца при концентрации иммунореактивного инсулина в крови более 12,7 мкЕД/мл.
Все факторы повышения общего периферического сосудистого сопротивления приводят к
снижению почечного кровотока, что вызывает активацию ренин-ангиотензин-альдостероновой
системы (РААС). Открытие тканевого компонента РААС способствовало пониманию механизма
стимуляции резистивных сосудов в скелетной мускулатуре. Тканевая РААС функционирует
независимо от уровня циркулирующего в плазме ренина и приводит к стимуляции липогенеза и
накоплению липидов в адипоцитах. С увеличением массы жировой ткани возможно развитие
системного действия тканевого ангиотензина II. С другой стороны, при длительной АГ к развитию
ИР приводит снижение периферического кровотока.
ГИ способствует нарушению фибринолитической активности крови через механизм синтеза в
жировой ткани ингибитора активации тканевого плазминогена, вследствие чего замедляется
скорость расщепления фибрина. Это один из механизмов нарушения гомеостаза при МС. В
условиях ИР повышается адгезивная и агрегационная способность тромбоцитов крови, что, по
мнению многих авторов, является одним из важных пусковых механизмов каскада
гемореологических нарушений, способствующих тромбообразованию и нарушению
микроциркуляции.
На основании многих исследований ГИ принято считать фактором риска или маркёром ИБС.
Отмечается роль не столько самой ИР, сколько её ассоциации с другими метаболическими
нарушениями, каждое из которых обладает атерогенным потенциалом. Установлено, что такой
показатель, как уровень инсулина натощак, входит в число параметров, прогнозирующих развитие
инфаркта миокарда в течение ближайших 5 лет. Среди других проявлений ИБС, сопряжённых с
ИР, выделяют стенокардию, в том числе вазоспастическую Интересные данные получены в
последнее время о наличии связи МС с кардиологическим синдромом Х (микрососудистая
стенокардия). Этот синдром может оказаться клиническим проявлением МС.
Диагностика. В 1999 году ВОЗ были приняты следующие критерии диагностики МС:
НТГ или СД, тип 2 и/или ИР;
АГ (более 160мм рт. ст. систолическое артериальное давление (АД) или более 90 мм рт. ст. диастолическое АД);
дислипидемия (ТГ в плазме крови более 1,7 ммоль/л и/или сниженная концентрация холестерина ЛПВП менее 0,9 ммоль/л для мужчин и менее 1,0 для женщин);
абдоминальное ожирение (отношение объёма талии (ОТ) к объёму бёдер (ОБ) более 0,9 для мужчин и более 0,85 для женщин) и/или ИМТ более 30 кг/м2;
микроальбуминурия (экскреция альбумина с мочой более 20 мг/мин или соотношение альбумин/креатинин более 20 мг/г).
Согласно критериям международной федерации диабета, 2005 год
Метаболический синдром – совокупность метаболических нарушений, основными из которых являются: абдоминальное ожирение, инсулинорезистентность и дислипидемия.
Компоненты метаболического синдрома:
Центральное ожирение: окружность талии (ОТ) ≥ 94 см у мужчин и ≥ 80 см у женщин в сочетании как минимум с двумя следующими нарушениями:
Повышенный уровень триглицеридов: ≥ 1,7 ммоль/л (150мг/дл);
Пониженный уровень холестерина липопротеидов высокой плотности (ХС-ЛПВП) < 1,04 ммоль/л (40 мг/дл) - у мужчин, < 1,29 ммоль/л (50мг/дл) - у женщин;
Повышенное АД: ≥ 130/85 мм рт. ст.;
Гипергликемия натощак: > 5,6 ммоль/л (100 мг/дл) или ранее диагностированный сахарный диабет (СД) 2 типа;
Установленный ранее СД 2 типа или нарушение толерантности к глюкозе.
Сформированы группы риска МС [18]:
пациенты с любыми проявлениями ИБС или другими атеросклеротическими заболеваниями;
здоровые люди, у которых при профилактическом обследовании выявлен один из признаков МС;
близкие родственники больных с ранними (у мужчин - до 55 лет, у женщин - до 60 лет) проявлениями атеросклеротических заболеваний.
С появлением возможности определять иммунореактивный инсулин показатель ИР приобрёл
количественное значение. Для оценки ИР используется эугликемический «клэмп-тест». О наличии
ИР можно судить также при расчёте индексов инсулинорезистентности и
инсулиночувствительности, основанных на соотношении концентрации инсулина и глюкозы в
плазме крови. Наиболее часто используется индекс Caro: отношение глюкозы (в мг/дл) и инсулину
(в мкМЕ/мл) в плазме крови натощак. Критерием наличия ИР считается значение индекса менее
6,0 (при измерении концентрации глюкозы в моль/л критическим является значение 0,33).
Предложена также модель оценки гомеостаза (НОМА) и ряд других индексов, диагностическая
ценность которых возрастает при проведении исследований с нагрузкой глюкозой и в динамике.
Глюкоза является основным энергетическим и пластическим веществом в организме. Она
поступает в организм в составе углеводов и откладывается в виде гликогена главным образом в
мышцах и печени. В здоровом организме соотношение глюкоза-инсулин поддерживает уровень
глюкозы в крови на определённом уровне. В организме больного МС в ответ на углеводную
нагрузку вырабатывается инсулин в гораздо большем количестве с целью преодоления тканевой
ИР. Уровень гормона настолько возрастает, что на каком-то этапе способствует
гипогликемическому состоянию, проявляющемуся слабостью, сердцебиением, бледностью
кожных покровов и головокружением. Внимательное отношение к указанным синдромам может
позволить заподозрить развивающуюся ИР уже на ранних стадиях.
Стабильное повышение уровня глюкозы в крови сопровождается гликозулированием белков
(неферментативное образование различных соединений глюкозы с белками), что приводит к
повреждению их структур и функций. Повреждение белков артериальных сосудов способствует
прогрессированию атеросклеротических изменений, белков мозга - к неврологическим
нарушениям. В результате формируются симптомы микро - и макроангиопатий, полинейропатий.
Выявление нарушения углеводного обмена является одним из важных шагов в диагностике МС. В
оценке используются критерии ВОЗ 1999 года, по данным которых о наличии СД говорят при
получении двух показателей глюкозы крови натощак более или равные 6,1 ммоль/л, взятые с
интервалом в 2-3 дня (здесь и далее нормы указаны для цельной капиллярной крови). Данный
уровень показателя позволяет установить диагноз СД на стадии отсутствия осложнений.
Используется также метод скрининга по выявлению СД: в течение суток измеряется
четырёхкратно случайная гипергликемия. Показатель (хотя бы один) гликемии 10 ммоль/л и более
указывает на вероятностный СД и требует дальнейшего целенаправленного поиска.
Базальная (тощаковая) гликемия в цельной крови от 5,6 до 6,1 ммоль/л является показанием к
проведению глюкозотолерантного теста (ГТТ) при клинических симптомах СД и при подозрении
на него. По данным теста судят о нарушении толерантности к глюкозе. Противопоказаниями к
проведению ГТТ служат неотложные состояния, роды, экстренные хирургические вмешательства
и манифестация СД с тощаковой гликемией более 6,0 ммоль/л.
Ожирение оценивается расчётом ИМТ, равным отношению массы тела (в кг) к росту (в м²).
Показатель более 30 кг/м² указывает на наличие ожирения. При диагностике МС важно оценить
абдоминальное ожирение, характеризующееся отложением жира в сальнике и брыжейке. Для
этого используется коэффициент отношения ОТ к ОБ, а так же их абсолютные величины. ОТ
измеряется в см на уровне пупка, ОБ - на уровне ягодиц.
При подозрении на МС исследуется общий холестерин. В случае выявления цифр более 5,0
ммоль/л необходимо провести более полное обследование липидного комплекса крови:
холестерина липопротеинов низкой плотности (ЛПНП), ЛПВП и ЛПОНП и ТГ.
Механизм, лежащий в основе дислипидемии при метаболическом синдроме.
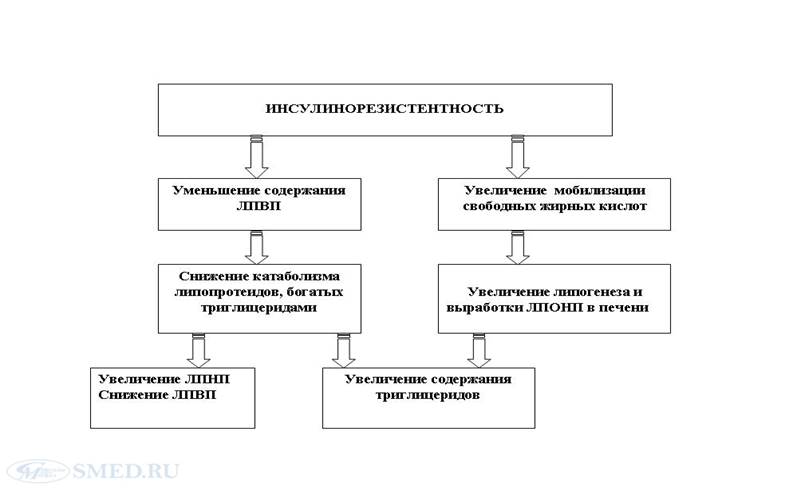 Ожирение как звено патогенеза метаболического синдрома.
Ожирение как звено патогенеза метаболического синдрома.
В настоящее время считается, что одним из ключевых моментов в развитии и прогрессировании метаболического синдрома является абдоминальный тип ожирения.
Абдоминальный (или андроидный, центральный) тип ожирения характеризуется расположением основной массы жира в брюшной полости, на передней брюшной стенке, туловище, шее и лице. Для определения типа ожирения разработаны соответствующие критерии. Причины развития такого типа ожирения до конца не выяснены. > >> 
Распределение жировой ткани в организме подвержено генетическому контролю. Избыточное же отложение жировой ткани по центральному типу развивается обычно после 30 лет, что. Вероятно, связано с возрастным повышением активности гипоталамуса и, в частности, системы АКТГ-кортизол, что подтверждается достоверным увеличением суточной экскреции метаболитов кортизола у лиц с андроидным ожирением не только по сравнению с контрольной группой, но и с пациентами с гиноидным типом. Имеются также данные о снижении активности гормончувствительной липазы у этих пациентов.
Жировую ткань подразделяют на висцеральную (интраабдоминальную) и подкожную. Именно повышение количества висцерального жира, как правило, сочетается с гиперинсулинемией, инсулинорезистентностью, артериальной гипертензией и дислипидемией. Висцеральная жировая ткань характеризуется морфологическими и функциональными особенностями; при абдоминальном ожирении содержание триглицеридов и неэстерифицированных жирных кислот (НЭЖК) крови обычно значимо выше, чем при гиноидном той же степени.
Избыток жировой ткани в абдоминальной области, нейрогормональные нарушения, сопутствующие абдоминальному ожирению, играют важную роль в развитии и прогрессировании инсулинрезистентности и связанных с ней метаболических расстройств. Увеличение объема жировых клеток сопровождается уменьшением плотности инсулиновых рецепторов на их поверхности и увеличением их инсулинрезистентности. Соответственно повышенное содержание инсулина ведет к усилению процесса синтеза жиров и блокированию их распада; с другой стороны, инсулинорезистентность жировой ткани проявляется в резистентности к антилиполитическому действию инсулина, приводящей к накоплению свободных жирных кислот и глицерина. Свободные жирные кислоты в больших количествах поступают в воротную вену и в печень, что приводит к уменьшению связывания гепатоцитами инсулина, его деградации и развитию инсулинорезистентности в печени, к торможению супрессивного действия инсулина на глюкогенез, а также к системной гиперинсулинемии, в свою очередь способствующей развитию периферической инсулинорезистентности. Существует и еще ряд механизмов, посредством которых избыток свободных жирных кислот способствует нарастанию периферической инсулинорезистентности, накоплению триглицеридов , холестерина ЛПОНП, ЛПНП .
Как известно, жировая ткань обладает ауто-, пара- и эндокринной функцией, выделяя значительное количество веществ, преимущественно негативно влияющих на статус инсулинорезистентности и атеросклероза. Это, в частности, адипонектин, резистин,интерлейкин-6, эстрогены,многие протеины РАС, апелин и др.
Наиболее изученными являются фактор некроза опухоли-α (ФНО-α) и лептин .
Фактор некроза опухоли-α - цитокин, синтезируемый макрофагами; в ряду других адипокинов рассматривается как фактор, связываюший ожирение и инсулинорезистентности. Отмечена положительная корреляция его содержания с ожирением и инсулинорезистентностью. Целенаправленное удаление гена ФНО-α или его рецепторов повышает чувствительность к инсулину и снижает содержание неэтерифицированных жирных кислот в крови животных.
Лептин - белковый гормон, секретируемый адипоцитами, продукт специфического «гена ожирения». Лептин регулирует чувство насыщения; предполагается, что его физиологическая роль состоит в поддержании обратной связи, с помощью которой центральная нервная система получает информацию о состоянии энергетических запасов в организме. При ожирении отмечается «лептинорезистентность», в связи с чем надежда на использование его для лечения ожирения не оправдались. Однако четкой связи между инсулинорезистентностью и секрецией лептина на настоящий момент не выявлено.
Нарушения гормональной функции жировой ткани играют важную роль в развитии инсулинорезистености и связанного с ней метаболического синдрома.
Патогенез нарушений углеводного обмена при метаболическом синдроме.
Нарушения углеводного обмена считаются большинством исследователей центральным компонентом метаболического синдрома.
Как уже упоминалось, основным интегральным механизмом, вокруг которого формируется цепь метаболических и гемодинамических нарушений при метаболическом синдроме, является инсулинорезистентность. > >> 
Под термином принято понимать снижение реакции инсулинчувствительных тканей на инсулин при его достаточной концентрации, приводящее к хронической компенсаторной гиперинсулинемией.
Гиперинсулинемия вызывает активацию симпато-адреналовой системы, которая влечет за собой вазоконстрикцию и, как следствие этого, уменьшение объемного кровотока в капиллярах скелетной мускулатуры, что является одной из причин дальнейшего прогрессирования инсулинорезистентность.
Компенсация инсулинорезистентности достигается в организме повышенной выработкой инсулина бета-клетками. Однако постоянная потребность в повышенной выработке инсулина истощает их секреторный аппарат, что приводит к нарушениям регуляции гомеостаза глюкозы. Считается, что эти нарушения преимущественно обусловлены генетическими факторами, реализуемыми как на уровне рецепторов жировой и мышечной тканей, так и самих бета-клеток поджелудочной железы.
Патогенетическая роль эндотелиальной дисфункции при метаболическом синдроме.
Под эндотелиальной дисфункцией подразумевается снижение способности эндотелиальных клеток выделять релаксирующие факторы при сохранении или увеличении уровня продукции сосудосуживающих факторов. Эндотелиальная дисфункция или нарушение функции сосудистого эндотелия - важное звено в сложном патогенетическом механизме развития атеросклероза.
Инсулинорезистентность и эндотелиальная дисфункция являются тесно ассоциированными состояниями и формируют порочный круг, приводящий к метаболической и кардиоваскулярной патологии. Однако причинно-следственные связи этих процессов до настоящего времени изучены не до конца. > >> 
Существует две точки зрения на эту проблему.
Сторонники первой считают, что дисфункция эндотелия вторична по отношению к имеющейся инсулинорезистентности, являясь следствием гипегликемии, артериальной гипертензии, дислипидемии. Их противники утверждают, что эндотелиальная дисфункция является не следствием, а причиной развития инсулинорезистентности и связанных с ней состояний, препятствуя попаданию инсулина в межклеточное пространство. Однако значительная роль эндотелиальной дисфункции в порочном круге формирования метаболического синдрома бесспорна.
Патогенетические аспекты некоторых заболеваний, ассоциированных с метаболическим синдромом.
Неалкогольный стеатогепатит(НАСГ). > >> 
Неалькогольный стеатогепатит многофакторно связан с компонентами метаболического синдрома. Гиперинсулинемия усиливает липогенез и подавляет окисление свободных жирных кислот способствуя таким образом накоплению в печени токсичных свободных жирных кислот; сам же жировой гепатоз, в свою очередь, усугубляет инсулинорезистентность, снижая клиренс инсулина. При этом активируется каскад перекисного окисления липидов (ПОЛ); взаимодействуя, эти процессы способствуют структурным изменениям ткани печени. Кроме того, цитокины, включая фактор некроза опухоли-α,также вовлечены в патогенез неалкогольного стеатогепатита и его возможных осложнений.
Синдром поликистозных яичников (СПКЯ, синдром гиперандрогении). > >> 
Одним из ведущих механизмов возникновения гиперандрогении (ГА) в настоящее время считается гиперинсулинемия, обусловленная инсулинрезистентностью. Инсулинрезистентность является единственной уникальной характеристикой синдрома поликистозных яичников, отличающей его от других состояний, сопровождающихся артериальной гипертензией и нарушениями овуляторной функции. Считается, что существует ген или группа генов, которые делают яичники части женщин с метаболическим синдромом более чувствительными к стимуляции инсулином продукции андрогенов – именно у этих пациенток развивается синдром поликистозных яичников (около 26%).
Подагра. > >> 
Механизмы, объясняющие повышение уровня мочевой кислоты при инсулинорезистентности, пока полностью не ясны. Предполагается, что основным патогенетическим звеном формирования подагры при метаболическом синдроме является уменьшения секреции уратов при гиперинсулинемии (в том числе эугликемической) за счет усиления реасорбции не только натрия, хлоридов и гидрокарбонатов, но и органических анионов, к которым и отсносятся ураты.
Канцерогенез. > >> 
В настоящее время признана роль инсулинрезистентности в создании предиспозиции к развитию ряда онкологических заболеваний, а также выявлены общие черты патогенеза метаболического синдрома и канцерогенеза. В реализации данной предиспозиции патогенетически задействованы инсулинрезистентность, ожирение, дислипидемия и нарушения углеводного обмена. При инсулинрезистентности изменения в основных гомеостатических системах способны создавать условия, благоприятствующие опухолевому росту. Это происходит, в частности, посредством усиления пролиферации и угнетения клеточного иммунитета под влиянием формирующегося при инсулинрезистентности набора гормонально-метаболических сдвигов. Часто характерные для метаболического синдрома локальное эстрогенообразование и гиперандрогенизация способствуют увеличению риска возникновения таких заболеваний, как рак молочной железы, эндометрия, толстой кишки, простаты, а также многих других локализаций.
тактики проводимой терапии трудно переоценить, тем более что интегральный потенциал коронарного риска во многом определяется выраженностью основных компонентов этого синдрома, определяемых по уровню артериального давления, холестерина ЛПВП и ЛПНП , триглицеридов , глюкозы , которые относятся к корригируемым факторам риска сердечно-сосудистых заболеваний, наряду с некорригируемыми факторами.
Состояния, ассоциированные с синдромом инсулинорезистентности
Гипертрофия левого желудочка с нарушением диастолической функции.
Апноэ во сне (синдром обструктивного апноэ сна).
Гиперурикемия и подагра.
Остеопороз.
Неалкогольный стеатогепатит.
Синдром поликистозных яичников.
Микроальбуминурия.
Гиперкоагуляционный синдром и др.
Преждевременный атеросклероз/ИБС, который является основной причиной смерти рассматриваемой категории больных.
Факторы, способствующие развитию метаболического синдрома.
Избыточное питание.
В основе накопления избыточного количества жира в организме лежит переедание животных жиров, содержащих насыщенные жирные кислоты (ЖК). Их избыток провоцирует структурные изменения фосфолипидов клеточных мембран и нарушения экспрессии генов, контролирующих проведение сигнала инсулина в клетку. Кроме того, очевидно, что высокая калорийность жиров способствует накоплению их избытка при переедании.
Гиподинамия
Снижение физической активности – второй по значимости после переедания фактор внешней среды, способствующий развитию ожирения и инсулинорезистентности. При гиподинамии замедляются липолиз и утилизация триглицеридов (триглицеридов) в мышечной и жировой тканях и снижается транслокация транспортеров глюкозы в мышцах, что приводит к развитию инсулинорезистентности.
Артериальная гипертензия
В ряде случаев артериальная гипертензия может быть первичным звеном в патогенезе метаболического синдрома. Длительная плохо контролируемая артериальная гипертензия вызывает нарушения периферического кровообращения, что приводит к снижению чувствительности тканей к инсулину и, как следствие, к относительной гиперинсулинемии и инсулинорезистентности.
Синдром обструктивного апноэ сна (СОАС)
Синдром обструктивного апноэ сна сопутствует метаболическому синдрому столь часто, что в настоящее время их сочетание получило название «синдрома Z». Ожирение – основной фактор развития синдром обструктивного апноэ сна; им страдает около 50% тучных людей. С другой стороны, метаболический синдром может развиваться вследствие наличия синдром обструктивного апноэ сна, не связанного с ожирением (любые нарушения, приводящие к расстройствам дыхания во время сна). В результате хронической гипоксии во время сна отсутствуют ночные пики выделения соматотропного гормона, что способствует развитию инсулинорезистентности.
Патогенез метаболического синдрома
В патогенезе метаболического синдрома неокончательно установленными являются не только его отправная точка, но и механизмы взаимодействия основных компонентов его структуры и патогенеза. Однако большинство исследователей сходятся во мнении, что в основе развития метаболического синдрома лежит инсулинорезистентность.
Ведущие патогенетические механизмы в развитии метаболического синдрома
Патогенез артериальной гипертензии в структуре метаболического синдрома.
Большинство авторов сходятся во мнении о существовании нескольких механизмов, обусловливающих наличие связи артериальной гипертензии и инсулинорезистентности.
Схема развития артериальной гипертензии в рамках метаболического синдрома

> >> 
Еще в 80-х годах прошлого века ученые пришли к выводу, что сочетание артериальной гипертензии с метаболическими факторами риска – это не механическое скопление, а закономерное проявление единой цепи целого ряда сложных биохимических нарушений на тканевом уровне. В 1985 г. Было высказано предположение, что гиперинсулинемия может служить связывающим звеном между артериальной гипертензией, ожирением и нарушением толерантности к глюкозе (НТГ). В ряде исследований по прямому определению инсулинорезистентности было показано, что больные с артериальной гипертензией в среднем утилизируют на 40% меньше глюкозы, чем лица с нормальным артериальным давлением.
В эпидемиологических исследованиях продемонстрировано также, что 64% больных с артериальной гипертензией имели инсулинорезистентности и только у половины пациентов она клинически манифестировала с нарушением углеводного обмена. С другой стороны, у 36% больных, имевших гиперлипопротеидемию (ГЛП) или избыточную массу тела (ИМТ), не было выявлено инсулинорезистентности. Таким образом, даже на фоне имеющегося в настоящее время огромного интереса к метаболическому синдрому было бы ошибочным связывать каждый случай эссенциальной артериальной гипертензии с проявлениями тканевой инсулинорезистентности.
Хроническая гиперинсулинемия как проявление тканевой инсулинорезистентности способствует задержке в организме натрия путем ускорения его реабсорбции, что приводит к увеличению объема жидкости и общего периферического сосудистого сопротивления. Повышение активности Na-K-, H- и Ca-Mg-АТФазы под непосредственным воздействием инсулина вызывает увеличение содержания внутриклеточного натрия и кальция, что способствует вазоконстрикции гладкой мускулатуры сосудов. При этом усиливается и чувствительность сосудов к прессорным агентам, таким как адреналин и ангиотензин.
Гиперинсулинемия также способствует активации симпатической нервной системы (СНС), в результате чего возрастает сердечный выброс и стимулируется вазоконстрикция периферических кровеносных сосудов. Симпатическая стимуляция почек запускает мощный механизм развития артериальной гипертензии – ренин-ангиотензин-альдостероновую систему. Исследования показывают, что при сочетании артериальной гипертензии с инсулинорезистентностью активность АПФ является достоверно более высокой по сравнению с больными артериальной гипертензией без проявлений инсулинорезистентности. Ангиотензин 11 – главный действующий компонент ренин-ангиотензин-альдостероновой системы – прямо и косвенно (опосредованно через активацию симпатической нервной системы) повышает давление в клубочковом аппарате, вызывает пролиферацию гладкомышечных стенок артерий, гипертрофию кардиомиоцитов и нарушает функцию эндотелия, что способствует системной артериальной и венозной вазоконстрикции.
Особую роль в ассоциации артериальной гипертензии и инсулинорезистентности играет ожирение абдоминального типа, характерное для метаболиского синдрома. В адипоцитах брыжейки и сальника идет синтез метаболически активных веществ, ингибирующих выработку эндогенного оксида азота, соответственно стимулируя вазоконстрикцию. В последние годы также активно обсуждается роль лептина в усилении активности симпатической нервной системы. Артериальная гипертензия развивается примерно у 60% больных ожирением.
В последнее десятилетие получило развитие учение о роли функции эндотелия в формировании и прогрессировании артериальной гипертензии. Показано, что в патогенезе артериальной гипертензии, связанном с метаболическими нарушениями, эндотелиальная функция является интегральным аспектом синдрома инсулинорезистентности и способствует ее углублению, увеличению реактивности сосудов и дальнейшему формированию артериальной гипертензии.
Методы оценки инсулинорезистентности
Существуют прямые и непрямые методы оценки влияния инсулина.
Прямые методы оценки влияния инсулина
Прямые методы подразумевают инфузию инсулина и анализ его эффектов на метаболизм глюкозы. К ним относятся эугликемический гиперинсулинемический клэмп-тест (ЭГК-тест), инсулиновый супрессивный тест (ИСТ), инсулиновый тест толерантности(ИТТ). ИСТ и ИТТ в настоящее время не актуальны.
«Золотым стандартом» определения инсулинорезистентности является ЭГК-тест, описанный еще в 1979году R.A. DeFronzo. > >> 
В его основе лежит прерывание физиологической взаимосвязи уровня глюкозы и инсулина в организме путем контролируемого поддержания концентрации глюкозы крови на заданном нормо- или гипергликемическом уровне. Методика этого теста представляет собой постоянную в\в инфузию инсулина со скоростью 1 МЕ/мин на 1кг массы тела и повторные инфузии глюкозы. При этом каждые 5 минут определяют уровень глюкозы крови для оценки необходимой скорости ее инфузии, требуемой для поддержания эугликемии. Через определенный период времени, но не менее 120 мин., устанавливается равновесие, когда скорость инфузии глюкозы равна скорости её периферической утилизации. В настоящее время это делается с помощью компьютерной программы, встроенной в специальную систему для инфузий (Биостатор).
Для характеристики чувствительности тканей к инсулину осуществляется расчет общего потребления глюкозы организмом в мл/мин/кг на 1 мкМЕ инсулина. Чем больше глюкозы необходимо вводить за единицу времени для поддержания стабильного уровня гликемии, тем больше пациент чувствителен к действию инсулина. Если количество введенной глюкозы невелико, значит, пациент резистентен к инсулину.
Согласно критериям ВОЗ, инсулинорезистентность диагностируется по результатам ЭГК-теста в тех случаях, когда захват глюкозы ниже нижней квартили для исследуемой популяции.
Однако данный тест является инвазивным, трудоемким и дорогостоящим.
Непрямые (косвенные) методы оценки инсулинорезистентности определяют
Непрямые (косвенные) методы оценки инсулинорезистентности определяют эффекты эндогенного инсулина. К ним относятся:
Измерение концентрации инсулина в плазме крови (ИРИ) натощак > >> 
считается наиболее простым способом оценки инсулинорезистентности, удобным для использования в клинике. Гиперинсулнемия при нормогликемии, как правило, свидетельствует о наличии инсулинорезистентности и является предвестником развития сахарного диабета 2-го типа. Недостатком метода являе
|
из
5.00
|
Обсуждение в статье: Эпидемиология метаболического синдрома |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

