 |
Главная |
Сущность окислительно-восстановительных процессов
|
из
5.00
|
В 1913 году Л.В. Писаржевский выступил с электронной теорией окислительно-восстановительных процессов, которая является в настоящее время общепринятой. Этот тип реакций осуществляется за счет перераспределения электронной плотности между атомами реагирующих веществ (переходом электронов), что проявляется в изменении степени окисления.
Реакции, в результате которых изменяются степени окисления атомов, входящих в состав реагирующих веществ вследствие переноса электрона между ними, называются окислительно-восстановительными реакциями.
Окислительно-восстановительный процесс состоит из 2 элементарных актов или полуреакций: окисления и восстановления.
Окисление - это процесс потери (отдачи) электронов атомом, молекулой или ионом. При окислении степень окисления частиц повышается:

Частица, отдающая электроны, называется восстановителем. Продукт окисления восстановителя называется его окисленной формой:
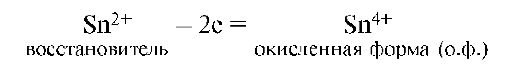
Восстановитель со своей окисленной формой составляют одну пару окислительно-восстановительной системы (Sn2+/Sn4+).
Мерой восстановительной способности того или иного элемента является потенциал ионизации. Чем меньше потенциал ионизации элемента, тем более сильным восстановителем он является, s-элементы и элементы в низшей и промежуточной степени окисления - сильные восстановители. Способность частицы отдавать электроны (донорная способность) определяет ее восстановительные свойства.
Восстановление - это процесс присоединения электронов частицей. При восстановлении степень окисления понижается:

Частица (атомы, молекулы или ионы), присоединяющая электроны, называется окислителем. Продукт восстановления окислителя называется его восстановленной формой:

Окислитель со своей восстановленной формой составляет другую пару (Fe3+/Fe2+) окислительно-восстановительной системы. Мерой окислительной способности частиц является сродство к электрону. Чем больше сродство к электрону, т.е. электроноакцепторная способность частицы, тем более сильным окислителем он является.Окисление всегда сопровождается восстановлением, и, наоборот, восстановление связано с окислением.
Рассмотрим взаимодействие FeCl3 с SnCl2. Процесс состоит из двух полуреакций:

Окислительно-восстановительную реакцию можно представить в виде сочетания двух сопряженных пар.
В ходе реакций окислитель превращается в сопряженный восстановитель (продукт восстановления), а восстановитель в сопряженный окислитель (продукт окисления). Их рассматривают как окислительно-восстановительные пары:

Поэтому окислительно-восстановительные реакции представляют единство двух противоположных процессов окисления и восстановления, которые в системах не могут существовать один без другого. В этом мы видим проявление универсального закона единства и борьбы противоположностей. Реакция произойдет, если сродство к электрону окислителя больше, чем потенциал ионизации восстановителя. Для этого введено понятие электроотрицательности - величины, характеризующей способность атомов отдавать или принимать электроны.
Составление уравнений окислительно-восстановительных реакций проводится методом электронного баланса и методом полуреакций. Методу полуреакций необходимо отдать предпочтение. Применение его связано с применением ионов, реально существующих, видна роль среды. При составлении уравнений необходимо выяснить, какие из веществ, вступающих в реакцию, выполняют роль окислителя, а какие - восстановителя, влияние на ход реакции pH среды и каковы возможные продукты реакции. Окислительно-восстановительные свойства проявляют соединения, которые содержат атомы, имеющие большое число валентных электронов, обладающих различной энергией. Такими свойствами обладают соединения d-элементов (IB, VIIB, VIIIB групп) и р-элементов (VIIA, VIA, VA групп). Соединения, которые содержат элемент в высшей степени окисления, проявляют только окислительные свойства(КМnО4, H2SO4), в низшей - только восстановительные свойства(H2S), в промежуточной - могут вести себя двояко(Na2SO3). После составления уравнений полуреакций, ионного уравнения составляют уравнение реакции в молекулярной форме:

Проверка правильности составления уравнения: число атомов и зарядов левой части уравнения должно быть равно числу атомов и зарядов правой части уравнения для каждого элемента.
|
из
5.00
|
Обсуждение в статье: Сущность окислительно-восстановительных процессов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

