 |
Главная |
Механизм действия ферментов
|
из
5.00
|
Механизм действия простого и сложного ферментов одинаков, так как активные центры в их молекулах выполняют сходные функции.
Основы механизма действия ферментов были изучены в начале XX в. В 1902 г. английский химик А.Браун высказал предположение о том, что фермент, воздействуя на субстрат, должен образовать с ним промежуточный фермент — субстратный комплекс. Одновременно и независимо от А. Брауна это же предположение высказал французский ученый В. Анри. В 1913 г. Л. Михэлис и М. Ментэн подтвердили и развили представления о механизме действия ферментов, который можно представить в виде схемы:

где Е — фермент, S — субстрат, Р — продукт.
На первой стадии ферментативного катализа происходит образование фермент-субстратного комплекса, где фермент и субстрат могут быть связаны ионной, ковалентной или иной связью. Образование комплекса ES происходит практически мгновенно.
На второй стадии субстрат под воздействием связанного с ним фермента видоизменяется и становится более доступным для соответствующей химической реакции. Эта стадия определяет скорость всего процесса.
На третьей стадии происходит химическая реакция, в результате которой образуется комплекс продукта реакции с ферментом.
Заключительным процессом является высвобождение продукта реакции из комплекса.
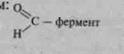

Эту схему можно проиллюстрировать конкретным примером. Рассмотрим механизм действия аминотрансфераз, катализирующих процесс переаминирования амино- и кетокислот. Аминотрансфе-раза — холофермент, коферментом которого является пиридок-сальфосфат, связанный ковалентно с апоферментом. Активной группой, принимающей участие в катализе, является альдегидная группа кофермента, поэтому для простоты изображения механизма действия фермента обозначим холофермент cледующим образом.
На первой стадии ферментативного катализа происходит образование ферментсубстратного комплекса [ES], в котором фермент и субстрат связаны ковалентной связью:
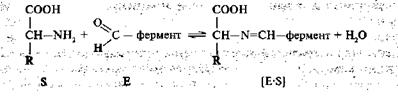
На второй стадии происходит преобразование субстрата, выражающееся в таутомерной перегруппировке, что приводит к образованию комплекса [E-S]':
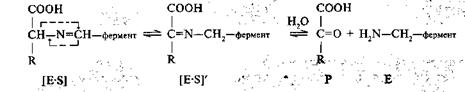
В результате химической реакции (в данном случае происходит гидролиз) образуется кетокислота, а фермент высвобождается из комплекса в виде пиридоксаминфермента. Чтобы не нарушался один из основных принципов катализа, в данном процессе принимает участие кетокислота. Последующий процесс можно представить следующей схемой:
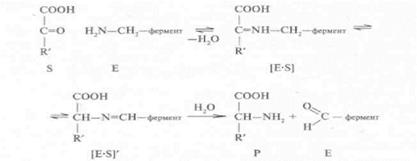
Данный пример не только иллюстрирует механизм действия фермента, но и дает представление о том, что биохимический процесс можно выразить в виде цепи простых химических превращений субстрата.
|
из
5.00
|
Обсуждение в статье: Механизм действия ферментов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

