 |
Главная |
Это основное уравнение кинетики ферментативной реакции - Михаэлиса-Ментен
|
из
5.00
|
КИНЕТИКА ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ
1. Влияние концентрации фермента на скорость ферментативной реакции.
2. Влияние концентрации субстрата на скорость ферментативной реакции.
I. Кинетика – наука, изучающая закономерности изменения скорости химических реакций во времени. Кинетической закономерности подчиняются и ферментативные реакции. Особенностью их является образование фермент-субстратного комплекса, насыщение фермента субстратом.
Под скоростью ферментативной реакции понимают активность фермента. Её можно измерить либо по количеству превращаемого субстрата, либо по нарастанию концентрации продукта реакции в единицу времени.
Зависимость скорости ферментативной реакции от концентрации фермента описывается уравнением:
 v = k[E],
v = k[E],
где v - скорости ферментативной реакции; k – константа пропорциональности; [E] – концентрация фермента. Величина k зависит от химической природы фермента и субстрата.
Графически это уравнение представляет собой прямую линию. Однако такая зависимость наблюдается только в начальный период реакции, когда концентрация субстрата [S] находится в избытке по отношению к концентрации фермента [E]: [S] >> [E].
|

 [E] + [S] [ES] + P,
[E] + [S] [ES] + P,
где [S] – концентрация субстрата; [ES] – концентрация фермент-субстратного комплекса; k1 – константа скорости образования [ES]; k-1 – константа скорости распада [ES]; Р – продукты реакции.
Обозначим: [E0] – общая концентрация фермента; ([E0] – [ES]) – концентрация свободного фермента. Согласно закону действия масс можно записать:
([E0] – [ES]) × [S] × k1 = [ES] × k-1
Разделив обе части на уравнения на k1, обозначим отношении k-1/k1 = ks. ks – константа диссоциации комплекса ES; она представляет собой обратную величину химического сродства фермента к субстрату: чем < ks, тем > ES.
([E0] – [ES]) × [S] = [ES] × ks
[ES] – величина, трудно определяемая экспериментально, от неё необходимо избавиться:
[E0] [S] - [ES] [S] = ks [ES]
[E0] [S] = [ES] (ks + [S])
[E0]×[S]
[ES] = ---------- (1)
kS + [S]
Следовательно скорость ферментативной реакции в общем случае определяется величиной [ES].
Максимальная скорость реакции (Vmax) будет наблюдаться, когда весь фермент будет участвовать в образовании комплекса ES. Следовательно:
Vmax [ES]
v = ---------- (2)
[E0]
подставив в уравнение (2) значение [ES] (1) получим:

 Vmax [S]
Vmax [S]
v = ----------
KS + [S]
Это основное уравнение кинетики ферментативной реакции - Михаэлиса-Ментен
Данное уравнение имеет несколько решений:
1. [S] >> KS; тогда величиной KS можно пренебречь и v = Vmax, пока концентрация субстрата велика, скорость реакции близка к максимальной и практически мало изменяется до тех пор, пока уменьшение концентрации субстрата не будет значительным. Реакция будет иметь нулевой порядок (n = 0).
2. [S] << KS; тогда практически скорость реакции будет описываться уравнением
Vmax
v = ------ [S],
KS
где Vmax и KS – кинетические константы и данное уравнение – уравнение прямой линии; скорость ферментативной реакции пропорциональна концентрации субстрата. Это реакция первого порядка (n = 1).
3. Величина [S] – промежуточная; пусть [S] = KS, v = 1/2Vmax. В данном случае порядок реакции будет дробный (0 < n <1).
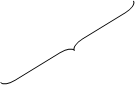
Графическое решение уравнения

|
|
|
|


|
|
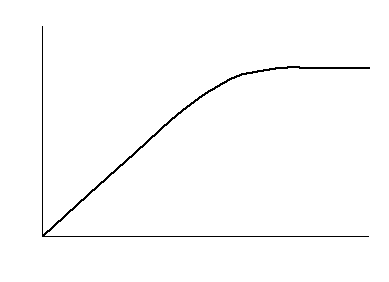
Таким образом, в ферментативных реакциях порядок реакции меняется в ходе самой реакции. При n = 0 не наблюдается дальнейшего увеличения скорости ферментативной реакции, т.к. произошло насыщение фермента субстратом. В неферментативных химических реакциях порядок от её начала до конца практически не меняется.
Уравнение Михаэлиса-Ментен справедливо для начала ферментативной реакции, когда в реагирующей смеси мало продуктов реакции. Дж. Бриггс и Дж. Холдейн модифицировали уравнение Михаэлиса-Ментен, они исходили из следующего уравнения ферментативной реакции:
k1 k2


 E + S ES Е + P
E + S ES Е + P
k-1
В этом ранении учитывается распад комплекса ES на Е и P, введя константу распада k2. Тогда
Vmax [S]
v = ----------
Km + [S]
Кm = (k-1 + k2)/ k1 – константа Михаэлиса – это концентрация субстрата, при которой скорость реакции составляет половину максимальной. Величина Кm характеризует фермента к субстрату. Чем меньше величина Кm тем больше сродство фермента к данному субстрату.
|
из
5.00
|
Обсуждение в статье: Это основное уравнение кинетики ферментативной реакции - Михаэлиса-Ментен |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

