 |
Главная |
Физические взрывы и их характеристика
|
из
5.00
|
Одним из примеров физического взрыва является взрыв парового котла. Явление связано с быстрым переходом перегретой воды в парообразное состояние. При атмосферном давлении вода кипит при температуре 100 °С в открытом сосуде. В закрытом сосуде (котле) начало кипения происходит также при 100 °С, но образующийся при этом пар производит давление на поверхность воды и кипение прекращается. Чтобы вода в котле продолжала кипеть, необходимо её нагревать до температуры, соответствующей давлению пара (при 588,4 кПа – 169 °С; при 784,5 кПа – 171 °С; при 1176,8 кПа – 189 °С).
Если после нагрева воды, например до 189 °С, прекратить подачу тепла в топку котла и нормально расходовать пар, то вода будет кипеть до тех пор, пока её температура не станет ниже 100 °С. При этом, чем скорее будет убывать давление в котле, тем интенсивнее будет кипение и парообразование за счет избытка тепловой энергии, содержащейся в воде.
Этот избыток тепловой энергии при падении давления от максимального до атмосферного целиком расходуется на парообразование.
В случае механического разрыва стенок котла нарушается внутреннее равновесие в котле и происходит внезапное падение давления до атмосферного. Перегретая вода с той же скоростью превращается в пар. При этом из 1 м3 воды образуется 1700 м3 пара, что приводит к разрушению котла, к несчастным случаям. Аналогичные явления происходят и при упуске воды (пламенем перегреты стенки), которая мгновенно превращается в пар, если её добавляют.
Подобные физические явления могут происходить и при эксплуатации компрессоров.
Температура сжимаемого газа в компрессорах повышается:
 ; (4.3)
; (4.3)
где 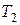 - температура газа после сжатия, К;
- температура газа после сжатия, К;
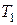 - температура газа до сжатия, К;
- температура газа до сжатия, К;
 - давление газа до сжатия, Па;
- давление газа до сжатия, Па;
 - давление газа после сжатия, Па;
- давление газа после сжатия, Па;
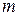 - показатель политропы (для воздуха
- показатель политропы (для воздуха 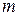 = 1,41).
= 1,41).
В таблице 4.1 представлены величины давления сжимаемого газа (воздуха) при различных температурах.
Таблица 4.1 – Давление воздуха после сжатия в зависимости от температуры
| Температура, оС | Давление, кПа |
Рассматривая причины взрывов (для компрессоров: повышение температуры сжимаемого воздуха, повышение давления сжатого воздуха сверх установленного, вспышка смазочных масел; для баллонов со сжатыми и сжиженными газами: удары, падение, особенно в условиях низких температур, переполнение баллонов, повышение температуры от нагрева солнечными лучами или отопительными приборами), приходим к тому, что, в любом случае, взрыв возникает вследствие преодоления сопротивления стенок резервуара, а его разрушительный эффект зависит от давления, под которым пары или газы находились в резервуаре.
Взрывы возникают и при мощных искровых разрядах или при пропускании электрического тока высокого напряжения через тонкие металлические нити.
При мощных разрядах разность потенциалов выравнивается за время от 10-6 до 10-7 секунд. Благодаря чему в зоне разряда достигается колоссальная плотность энергии и температура сотни тысяч градусов, что, в свою очередь, приводит к сильному подъему давления воздуха.
Химическим взрывом называется самораспространяющееся с большой скоростью химическое превращение газа или пыли, протекающее с выделением большого количества тепла и образованием большого объема газообразных продуктов.
Условия, которым должна удовлетворять химическая реакция, протекающая в форме взрыва:
- экзотермичность;
- образование газов или паров;
- большая скорость (крайне быстрое протекание явления);
- способность к самораспространению.
Каждое их этих условий играет немалую роль и не может быть исключено, иначе процесс не будет взрывом.
Взрыв происходит за стотысячные и даже миллионные доли секунды. Большая скорость выделения энергии определяет преимущества взрывчатых веществ по сравнению с обычным горючими. В то же время по общему запасу энергии, отнесенной к весовым количествам, даже наиболее богатые энергией взрывчатые вещества не превосходят обычные горючие системы, однако, при взрыве достигается несравненно более высокая объемная концентрация, или плотность энергии. Горение обычных горючих веществ протекает сравнительно медленно, что приводит к значительному расширению продуктов реакции в ходе процесса и существенному рассеиванию выделяемой энергии путем теплопроводности и излучения. По этим причинам в данном случае достигается лишь относительно низкая плотность энергии в продуктах горения.
Взрывные процессы, наоборот, протекают столь быстро, что можно считать, что вся энергия практически успевает выделиться в объеме, занятом самим взрывчатым веществом, что приводит к таким высоким концентрациям энергии, которые недостижимы в условиях обычного протекания химической реакции.
Взрывчатые вещества
В настоящее время известно большое число взрывчатых веществ, отличающихся большим разнообразием как по составу, так и по своим физико-химическим и взрывчатым свойствам. Это вызывает необходимость их рациональной классификации.
Все взрывчатые вещества делятся на две основные группы:
- взрывчатые химические соединения;
- взрывчатые смеси.
Химические соединения представляют собой относительно неустойчивые химические системы, способные под влиянием внешних воздействий к быстрым экзотермическим превращениям, в результате которых происходит полный разрыв внутримолекулярных связей и последующие рекомбинации свободных атомов (или ионов) в термодинамические и устойчивые продукты. Большинство взрывчатых веществ этой группы представляет собой кислородосодержащие органические соединения, способные к частичному или полному горению. Имеется, однако, достаточное количество взрывчатых эндотермических соединений, не содержащих кислорода, которые в условиях взрыва разлагаются на свои составные элементы. Примером такого соединения может служить азид свинца, разлагающийся при взрыве на азот и свинец с выделением энергии, равной теплоте образования этого соединения из элементов.
Подобные соединения обладают недостаточно прочной молекулярной структурой и повышенной чувствительностью к внешним воздействиям, что сильно ограничивает, а часто вовсе исключает возможность их практического использования. Примером таких особенно непрочных соединений могут служить галоидные и сернистые соединения азота:  ,
,  ,
,  , которые легко взрываются от ничтожных механических воздействий.
, которые легко взрываются от ничтожных механических воздействий.
Неустойчивость взрывчатых соединений обусловливается присутствием в их молекулах особых, так называемых эксплофорных, атомных комплексов, к числу которых относятся:
- 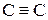 присутствует в производных ацетилена;
присутствует в производных ацетилена;
-  в галоидных соединениях азота;
в галоидных соединениях азота;
- 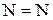 в азидах, азотосоединениях;
в азидах, азотосоединениях;
- 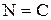 в солях гремучей кислоты;
в солях гремучей кислоты;
-  в нитратах и нитросоединениях;
в нитратах и нитросоединениях;
-  в перекисях и озонитах;
в перекисях и озонитах;
- 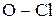 в хлоратах и перхлоратах.
в хлоратах и перхлоратах.
Взрывные смеси представляют собой системы, состоящие по крайней мере из двух химически не связанных между собой компонентов обычно один из компонентов смеси представляет собой вещество, относительно богатое кислородом, а второй компонент, наоборот - горючее вещество, совсем не содержащее кислорода, либо содержащее его в количестве, недостаточном для полного внутримолекулярного окисления. Смеси бывают:
- газообразные;
- жидкие;
- твердые (гетерогенные).
Горючими компонентами жидких взрывчатых смесей обычно являются вещества, сгорающие с большим тепловым эффектом (бензол, толуол, мононитросоединения). В качестве окислителя часто используется дымящая азотная кислота ( 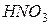 ) и тетранитрометан. Подобные жидкие смеси являются достаточно мощными взрывчатыми веществами, однако, в практике применяются редко вследствие их высокой чувствительности и неудобства использования.
) и тетранитрометан. Подобные жидкие смеси являются достаточно мощными взрывчатыми веществами, однако, в практике применяются редко вследствие их высокой чувствительности и неудобства использования.
С конца XIX века ведутся большие работы в области создания для угольных шахт безопасных взрывчатых веществ. В начале 20-х годов ХХ века в отечественную промышленность стали внедряться аммониты, ставшие основным взрывчатым веществом, применяемым в хозяйственных целях. Интересно, что первые тысячи тонн аммонитов были извлечены из снарядов и авиабомб со времен первой мировой войны.
С 30-х годов ХХ века в СССР, значительно раньше других государств, стали применять аммониты для промышленных целей. Широкому внедрению аммонитов способствовали значительно меньшая (по сравнению с динамитом) чувствительность к механическим воздействиям и, следовательно, меньшая опасность в обращении, меньшая скорость детонации, которая снизила затраты энергии взрыва на излишнее переизмельчение породы. Во время Великой Отечественной войны угольные шахты получили взрывчатые вещества типа аммонитов, в состав которых были введены пламегасители.
Твердые взрывчатые смеси весьма многочисленны и находят широкое применение, как в гражданской, так и в военной технике. В зависимости от химической природы окислителя, входящего в их состав, эти смеси подразделяются на соответствующие подгруппы, из которых наиболее важными являются аммонито-селитренные взрывчатые вещества или аммониты. Основными компонентами этих составов является аммиачная селитра  , содержание которой в различных составах колеблется от 40 до 95 %. В качестве горючего компонента применяются различные нитроароматические взрывчатые соединения (тротил, динитробензол и др.), содержащие недостаточное количество кислорода для получения продуктов полного сгорания.
, содержание которой в различных составах колеблется от 40 до 95 %. В качестве горючего компонента применяются различные нитроароматические взрывчатые соединения (тротил, динитробензол и др.), содержащие недостаточное количество кислорода для получения продуктов полного сгорания.
Аммиачная селитра - бесцветное кристаллическое вещество, содержащее 60 % кислорода, 5 % водорода и 35 % азота, причем половина азота находится в виде азота аммиака, а половина в виде азота азотной кислоты. Температура плавления (  ) от 145 до 166 оС, при нагревании выше 300 оС взрывается. Разложение происходит по уравнениям:
) от 145 до 166 оС, при нагревании выше 300 оС взрывается. Разложение происходит по уравнениям:


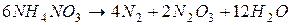
Взрывчатые свойства селитры увеличиваются при смешивании ее с органическими веществами и материалами (соломой, древесными опилками, стружкой и т. п.).
При повышении температуры селитра разлагается с выделением кислорода, который увеличивает интенсивность и распространение пламени.
Но даже без добавки примесей селитра способна к детонации. Это подтверждается примерами взрывов, происшедших в разных странах мира при попытке разрыхления селитры.
Аммиачная селитра не считалась взрывчатой до трагического случая, происшедшего в 1921 г. на немецком химическом заводе в Оппау. Для дробления слежавшейся смеси там был применен взрывной способ. В результате на воздух взлетели склад и весь завод. В несчастье нельзя было упрекнуть инженеров завода: примерно двадцать тысяч подрывов прошло нормально и лишь один раз создались условия, благоприятные для детонации. Аммиачная селитра к удару не чувствительна, взрывается только при достижении так называемой критической массы, методы определения которой еще не разработаны. При температуре взрыва аммиачной селитры (1230 оС) объем выдавливаемых газов составляет 976 л/кг и теплота взрыва - 350 ккал/кг.
В простейших аммонитах горючими компонентами являются такие вещества, как уголь, древесная мука, различные смолы. Примерами аммонитов может служить гудронит (95 % аммиачной селитры и 20 % тротила). Аммониты находят широкое применение в гражданской технике, а в военное время являются удобными заменителями основных взрывчатых веществ.
Особое место среди взрывчатых систем занимают динамиты, пороха и взрывчатые сплавы. До изобретения Альфредом Нобелем новой взрывчатой смеси, которую он назвал «динамит» и получил в 1867 г. патент на ее производство, из взрывчатых веществ был известен только черный порох. Основным компонентом динамита является нитроглицерин 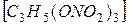 . Это взрывчатое вещество, прозрачная масляная жидкость, из группы нитроэфиров (сложные эфиры глицерина и азотной кислоты). Брикеты из кизельгура, пропитанного нитроглицерином, были совершенно безопасны в обращении, хотя сохраняли свою разрушительную силу. И с конца ХIX столетия динамит завоевал славу лучшего взрывчатого вещества.
. Это взрывчатое вещество, прозрачная масляная жидкость, из группы нитроэфиров (сложные эфиры глицерина и азотной кислоты). Брикеты из кизельгура, пропитанного нитроглицерином, были совершенно безопасны в обращении, хотя сохраняли свою разрушительную силу. И с конца ХIX столетия динамит завоевал славу лучшего взрывчатого вещества.
Взрывчатые вещества и взрывчатые системы в соответствии с областями их применения разбиваются на 4 группы:
- инициирующие;
- бризантные;
- метательные взрывчатые вещества, пороха, ракетные топлива;
- пиротехнические составы.
Инициирующие взрывчатые вещества применяются в качестве инициаторов взрывных процессов, для возбуждения детонации основных взрывчатых веществ (снарядах, минах, авиабомбах).
Вещества, которые взрываются лишь под действием ударной волны, а при обычных условиях существуют и даже не боятся огня, весьма удобны для взрывного дела. Такие вещества можно производить и хранить в больших количествах. Однако для приведения этих инертных взрывчатых веществ в действие нужны инициаторы взрыва, необходимые для возникновения ударных волн. Примером таких инициирующих взрывчатых веществ могут служить азид свинца  или гремучая ртуть
или гремучая ртуть  . Если крупинку такого вещества положить на лист жести и поджечь, то происходит взрыв, пробивающий в жести отверстие. Взрыв таких веществ в любых условиях детонационный.
. Если крупинку такого вещества положить на лист жести и поджечь, то происходит взрыв, пробивающий в жести отверстие. Взрыв таких веществ в любых условиях детонационный.
Если немного азида свинца поместить на заряд вторичного взрывчатого вещества и поджечь, то взрыв инициатора дает ударную волну, достаточную для детонации вторичного взрывчатого вещества. На практике взрыв производится при помощи капсюля-детонатора, содержащего от 1 до 2 г инициирующего вещества.
К отличительным свойствам инициирующих взрывчатых веществ относятся:
- способность взрываться в форме детонации под влиянием незначительных тепловых или механических воздействий;
- малое время нарастания скорости взрывчатого превращения до максимального (этот период очень мал, несравненно меньше, чем у взрывчатых веществ других типов).
Инициирующие взрывчатые вещества преимущественно применяют в виде капсюлей-детонаторов. Инициирующие взрывчатые вещества вследствие их способности детонировать непосредственно под влиянием внешних воздействий иногда называют первичными взрывчатыми веществами.
Бризантные взрывчатые вещества применяются в качестве разрывных зарядов в различных боеприпасах и в подрывных средствах. В отличие от инициирующих взрывчатых веществ они обладают значительно большей устойчивостью к детонации. Их детонация вызывается влиянием относительно больших внешних воздействий обычно инициирующих взрывчатых веществ. Поэтому иногда бризантные взрывчатые вещества называют вторичными взрывчатыми веществами.
Наиболее важными представителями взрывчатых смесей этой группы являются аммониты, динамиты, а так же некоторые сплавы, например, тротила с гексогеном. Пороха применяются, главным образом, для метательных целей. Основным видом взрывчатого превращения их является быстрое горение. Они подразделяются на две группы:
- пороха - механические смеси;
- пороха нитроцеллюлозные (бездымные пороха).
Дымный порох, который состоит из калийной селитры (75 %), древесного угля (15 %) и серы (10 %), является представителем первой группы.
Пороха нитроцеллюлозные подразделяются на группы в зависимости от природы растворителя (пирокселиновые, баллиститы).
Служебным видом взрывчатого превращения ракетных топлив в ракетных двигателях является горение. К категории взрывчатых веществ относится и большинство пиротехнических составов, обладающих высокой чувствительностью к внешним воздействиям.
Кислородный баланс
Химические превращения взрывчатых веществ при взрыве в газообразные продукты происходят за счёт реакции окисления без доступа кислорода воздуха. Поэтому в своём составе взрывчатые вещества содержат компоненты, необходимые для такой реакции, т.е. горючие - водород и углерод, и компоненты, богатые кислородом.
Кислородным балансом называют разность между количеством кислорода, находящегося в составе данного взрывчатого вещества, и тем количеством кислорода, которое необходимо для полного окисления всего углерода в углекислый газ, соединения водорода с образованием паров воды, а также для превращения других компонентов в газы.
В практике взрывных работ кислородный баланс взрывчатых веществ имеет большое значение. Может быть: нулевым, положительным и отрицательным.
Нулевой кислородный баланс имеют взрывчатые вещества, количество кислорода в составе которых точно соответствует количеству, необходимому для полного окисления всех горючих компонентов.
Взрывчатые вещества, имеющие нулевой кислородный баланс, при взрыве выделяют максимальное количество тепла (теплота взрыва), а, следовательно, и энергии.
Положительный кислородный баланс имеют взрывчатые вещества, количество кислорода в составе которых превышает дозу, необходимую для окисления горючих компонентов. Например, аммиачная селитра имеет положительный кислородный баланс (+ 20 %). При взрыве взрывчатых веществ с таким балансом образуются вредные газы (окислы азота).
Отрицательный кислородный баланс имеют взрывчатые вещества, в состав которых входит количество кислорода, недостаточное для окисления всех горючих компонентов. Например, тротил имеет отрицательный кислородный баланс (- 74 %). При взрыве таких взрывчатых веществ образуется много ядовитой окиси углерода.
|
из
5.00
|
Обсуждение в статье: Физические взрывы и их характеристика |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

