 |
Главная |
РАСЧЕТЫ ПО ХИМИЧЕСКИМ ФОРМУЛАМ И УРАВНЕНИЯМ
|
из
5.00
|
ЗАДАЧА № 1
Какое количество вещества (моль) составляют:
I вариант 2,4 · 1024 молекул углекислого газа
II вариант 12,8 кг железа
III вариант 3,36 л газообразного азота
IV вариант 9 г оксида азота (II) NO
V вариант 5,4 ·1025 молекул оксида меди (II) CuO
ЗАДАЧА № 2
Вычислить относительную молекулярную и молярную массу вещества:
I вариант Cu(NO3)2
II вариант Ba(OH)2
III вариант H2SiO3
IV вариант Ag2SO4
V вариант Fe(OH)3
ЗАДАЧА № 3
Вычислите, где больше массовая доля
I вариантСерыв сероводороде или оксиде серы (IV)
II вариантУглеродав метане СН4 или в углекислом газе
III вариантЖелеза в оксиде железа (II) или оксиде железа(III)
IV вариантВодорода в этане С2Н6 или в сероводороде H2S
V вариантКислородав оксиде натрия или в оксиде алюминия
ЗАДАЧА № 4
1. Установите простейшую формулу муравьиной кислоты, если известно, что массовые доли в ней водорода, углерода и кислорода 4,35%, 26,09%, 69,56% соответственно.
2. В натуральном жемчуге массовые отношения кальция, кислорода и углерода равны 10:12:3. Какова химическая формула жемчуга?
3. В производстве хрусталя используется поташ. Какова его формула, если массовый состав его равен: калия – 56,6%, углерода – 8,7%, кислорода – 34,8%?
4. Определите формулу гидросульфида калия, если его состав следующий: калия – 54,2%, серы – 44,4%, водорода – 1,4%.
5. Определите формулу медицинского препарата, состоящего из кислорода, марганца и калия, если их массовые доли соответственно 40,5%, 34,8%, 24,7%.
ЗАДАЧА № 5
1. На одну чашку весов поместили серу количеством вещества 0,5 моль, а на другую чашку – 20 г железа. Будут ли весы в состоянии равновесия?
2. На одной чашке весов находится 75,25·1023 атомов магния. Какова масса меди, находящаяся на другой чашке весов, если весы в состоянии равновесия?
3. На одну чашку весов поместили 5 моль серы. Вычислите количество вещества оксида железа (III), которое нужно положить на другую чашку весов, чтобы весы были в состоянии равновесия?
4. На одну чашку весов поместили герметичный сосуд, в котором находится 56 л кислорода. Какое количество вещества воды нужно поместить на другую чашку весов, чтобы они находились в состоянии равновесия?
5. На одной чашке весов находится образец хрома, содержащий 4,8·1026атомов металла. На другой чашке находится 4 моль оксида меди (II). Находятся ли эти весы в состоянии равновесия?
ЗАДАЧА № 6
1. Хватит ли 1 тонны кислорода для сжигания 500 кг угля?
2. Можно ли разложением 7,5 г пероксида водорода получить 4,5 г кислорода?
3. Какой объем аммиака (при н.у.) может прореагировать с серной кислотой массой 4,9 г до ее полной нейтрализации?
4. Какой объем водорода (при н. у.) выделится при взаимодействии алюминия массой 10,8 г с избытком хлороводородной кислоты?
5. Хватит ли 12 г гидроксида кальция для полной нейтрализации раствора бромоводородной кислоты, содержащего 25 г HBr ?
ДОПОЛНИТЕЛЬНАЯ ЗАДАЧА
В избытке соляной кислоты растворили 6 г магния, 4 г меди и 1,5 · 1023атомов цинка. Можно ли выделившийся водород поместить в сосуд объемом 12л? (при н. у.)
ЗАНЯТИЕ 3
ПЕРИОДИЧЕСКИЙ ЗАКОН И ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д.И. МЕНДЕЛЕЕВА. ЗАКОНОМЕРНОСТИ ИЗМЕНЕНИЯ СВОЙСТВ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
Свойства химических элементов, а также их соединений, находятся в периодической зависимости от заряда ядра атомов химических элементов. (Современная формулировка Периодического закона Д.И. Менделеева).
Физический смысл Периодического закона(ПЗ) – периодически повторяется электронная конфигурация валентных электронов.
Группа– вертикальный столбец элементов, атомы которых имеют одинаковое число валентных электронов. У элементов главных подгрупп валентные электроны являются внешними, эти элементы относятся к s- илиp-элементам. Элементы побочных подгрупп (d- или f-элементы) содержат валентные электроны на внешнем слое и d-подуровне предвнешнего слоя.
Период – горизонтальный ряд элементов, атомы которых имеют равное число энергетических уровней.
Элементы одной подгруппы называются электронными аналогами, так как имеют сходную конфигурацию электронных слоев. Например,
+13Al …3s2 3p1 +31Ga …4s2 4p1 +49In …5s2 5p1 +81Tl 6s2 6p1
План характеристики элемента по положению в периодической системе химических элементов Д.И. Менделеева
- Название и символ элемента.
- Период, ряд, группа и подгруппа, в которых расположен химический элемент. Относительная атомная масса.
- Строение атома: заряд ядра, число протонов и нейтронов в ядре, общее число электронов, число энергетических уровней, на которых расположены электроны, число завершенных и незавершенных энергетических уровней.
- Электронографическая схема строения электронных оболочек, электронная формула атома. Число электронов на внешнем уровне, число валентных электронов.
- Возможные степени окисления и валентности в основном и возбужденном состояниях атома.
- Высшая и низшая степень окисления. Формула высших оксида и гидроксида, их характер, летучее водородное соединение.
- Окислительно-восстановительный характер атома в соединениях.
- Сравнение окислительно-восстановительных свойств атома, металлических или неметаллических свойств простого вещества, основного или кислотного характера кислородных соединений с ближайшими соседями по периоду и подгруппе.
Задание 1. Составьте характеристику химического элемента № 74.
- Элемент № 74 – вольфрам, символ W.
- Расположен в периодической системе в 6 периоде (большой период), в 8 ряду, в VI группе, в побочной подгруппе. Относительная атомная масса равна 184.
- Заряд ядра равен + 74. В ядре атома 74 протона, 110 нейтронов. Общее число электронов равно 74. Электроны расположены на 6 энергетических уровнях, из них завершенных уровней – 4, незавершенных – 2. Распределение электронов: 2, 8, 18,32,12, 2.
- Электронная формула атома: 1s2 2s22p63s23p64s23d104p65s24d105p66s24f145d4 . На внешнем уровне находится 2 электрона, следовательно, вольфрам – металл. Валентных электронов 6 - …5d46s2(поэтому вольфрам расположен в 6 группе). Металл переходный, так как валентные электроны расположены на внешнем и предвнешнем уровнях. Элемент d-семейства.
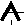
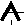
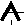
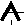

- +




 74 W … 5d 6s 6p
74 W … 5d 6s 6p
Возможные валентности II, IV, VI. Возможные степени окисления +2 (возбужденное состояние), +4, +6. Отрицательных значений степеней окисления не имеет, так как элемент – металл.
- Высший оксид W+6O3 – кислотный; высший гидроксид – кислотаH2WO4 Летучее водородное соединение не образует, так как элемент расположен в побочной подгруппе.
- В химических реакциях атом проявляет восстановительный характер, при этом степень окисления атома повышается.
- Вольфрам более активный металл по сравнению с танталом и менее активный по сравнению с рением (соседи по периоду). По сравнению с марганцем наблюдается повышение металлических свойств, усиление основного характера высшего оксида и высшего гидроксида.
Таблица 1
|
из
5.00
|
Обсуждение в статье: РАСЧЕТЫ ПО ХИМИЧЕСКИМ ФОРМУЛАМ И УРАВНЕНИЯМ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

