 |
Главная |
S, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d
|
из
5.00
|
Задание 2. Построить графическую схему и составить электронную формулу атома углерода.

 2s 2p
2s 2p
+6С

 1s
1s
Так как углерод расположен во втором периоде, электроны располагаем на двух энергетических уровнях. В итоге на первом завершенном уровне расположили 2 электрона. А на втором (внешнем), незавершенном уровне расположили 4 электрона, что соответствует IV группе ПС.
Электронная формула атома 1s2 2s22p2
Определим возможные валентные состояния и степени окисления атома в соединениях. Так как на 2р-подуровне (в основном состоянии) находятся 2 неспаренных электрона, валентность атома II. Степень окисления возможна +2 (р-подуровень будет пустым). На р-подуровне имеется одна пустая орбиталь, поэтому возможно «возбужденное» состояние. При этом один из спаренных электронов с 2s-подуровня перейдет на свободную 2р-орбиталь. В итоге на внешнем уровне окажется 4 неспаренных электрона. На последующей схеме показан только внешний энергетических уровень, содержащий валентные электроны.
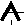
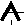
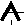 +6С* … 2s 2p
+6С* … 2s 2p
Так как в возбужденном состоянии 4 неспаренных электрона, возможна валентность IV и степень окисления +4 или -4 (энергетически равнозначно удаление 4 электронов и присоединение еще 4 электронов до завершения энергетического уровня).
Задание 3. Составьте электронную формулу атома с атомным
номером 23, определите его возможные валентности и степени окисления, укажите положение элемента в ПС, составьте формулы высшего оксида и гидроксида.
Электронная формула показывает размещение 23 электронов:
1s2 2s2 2p6 3s2 3p6 4s2 3d3
Валентные электроны расположены на 4s и 3d подуровнях. Внешних электронов - 2 (4s – подуровень). Следовательно, атом образует простое вещество – металл, химический элемент расположен в 4 периоде, в Vгруппе, побочной подгруппе (незавершен d-подуровень) – это ванадий. Элемент относится к семейству d-элементов (последний электрон поместили на d-подуровень).
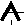
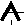




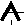

 +23V 3d 4s 4p
+23V 3d 4s 4p
Валентные возможности II, III, V
Степени окисления 0, +2, +3, +5
Высший оксид V2O5 кислотный оксид
Высший гидроксид HVO3
Обратите внимание! Высшая степень окисления равна номеру группы в ПС. Низшая степень окисления у металлов - 0, а у неметаллов – число электронов, недостающее до завершения электронного уровня (рассчитываем по формуле «8 - №группы»).
Задание 4. Определите положение элементов в ПС, назовите их высшую и низшую степень окисления:
а) … 2s2 б) … 3d10 4s2 4p3 в) … 3d5 4s2
| а | б | в | |
| Электронная формула | … 2s2 | …3d10 4s24p3 | … 3d5 4s2 |
| Период | |||
| Группа, подгруппа | II - А | V -А | VII-В |
| Символ элемента | Ве | Аs | Mn |
| Высшая степень окисления | +3 | +5 | +7 |
| Низшая степень окисления | -3 |
Номер периода определяем по значению наибольшего энергетического уровня. Номер группы - сумма валентных электронов (еа внешнем уровне и на незавершенном предвнешнем). В побочной подгруппе расположены элементы с незавершенными d и f-подуровнями.
|
из
5.00
|
Обсуждение в статье: S, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

