 |
Главная |
Массовая доля компонента
|
из
5.00
|
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ЗДРАВООХРАНЕНИЮ И СОЦИАЛЬНОМУ РАЗВИТИЮ
ГОСУДАРСТВЕННОЕ УНИТАРНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
«КАЗАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
КАФЕДРА ОБЩЕЙ И ОРГАНИЧЕСКОЙ ХИМИИ
РУКОВОДСТВО
К ПРАКТИЧЕСКИМ ЗАНЯТИЯМ
ПО ОБЩЕЙ ХИМИИ
(часть I)
КАЗАНЬ 2006
ББК 24я73
К 24
Печатается по решению Центрального координационно-методического совета Казанского государственного медицинского университета
Составители:
ст.преподаватель кафедры общей и органической химии Галеева С.И.,
доцент кафедры общей и органической химии Ситдиков И.Б.,
доцент кафедры общей и органической химии Хисамеев Г. Г.,
ст.преподаватель кафедры общей и органической химии Сагдеев К.А.
Под редакцией д.х.н. Никитиной Л.Е.
Рецензенты:
доцент кафедры Технологии неорганических веществ КГТУ Порфирьева Р.Т., доцент кафедры общей химии КГАСУ
Бойчук В.А.
Руководство к практическим занятиям по общей химии (часть I)/Галеева С.И., Ситдиков И.Б., Хисамеев Г.Г., Сагдеев К.А. Под ред. Никитиной Л.Е. - Казань: КГМУ, 2006. - 102 с.
Учебное пособие составлено в соответствии с Государственным образовательным стандартом высшего и профессионального образования и программой преподавания общей химии. В пособии приведены краткое изложение теоретического материала, примеры решения задач, вопросы и задачи для самоподготовки, описание лабораторных работ и контрольно-измерительные материалы в виде тестов по различным темам.
Предназначено для студентов I курса лечебного, педиатрического, стоматологического и медико-профилактического факультетов КГМУ.
ã Казанский государственный медицинский университет, 2005
ОГЛАВЛЕНИЕ
Занятие 1. Тема: Способы выражения концентрации растворов..….................4
Задачи с решениями……………………………………………………..….……....7
Вопросы и задачи для самоподготовки………………………………………....13
Лабораторная работа……………………………...……………………………...15
Занятие 2.Тема:Растворы сильных и слабых электролитов……....……….16
Задачи с решениями…………………………………………………………….18
Вопросы и задачи для самоподготовки………………………………………...20
Занятие 3.Тема: Автопротолиз воды. Ионное произведение воды.
Водородный и гидроксильный показатели. Гидролиз солей……………...23
Задачи с решениями…………………………………………………………...….25
Вопросы и задачи для самоподготовки……………………………….……...….27
Занятие 4.Тема: Буферные растворы. Гетерогенное равновесие.…………..30
Буферные растворы…………………………………………………………......30
Задачи с решениями……………………………………………………………....31
Вопросы и задачи для самоподготовки……………………………….………....33
Гетерогенное равновесие…………………………………………………….....34
Задачи с решениями…………………………………………………………..…..35
Вопросы и задачи для самоподготовки……………………………….………....36
Лабораторные работы……………………………..………………………….….38
Занятие 5.Тема: Коллигативные свойства растворов неэлектро-
литов………………………………………………………………………………...40
Задачи с решениями……………………………………………………………....42
Вопросы и задачи для самоподготовки……………………………….………...46
Занятие 6.Тема: Обобщение знаний по объёмному анализу. Контрольная работа по разделам «Учение о растворах», «Объёмный анализ».Образец билета контрольной работы…………………………………………………….....52
Занятие 7.Тема: Элементы химической термодинамики и биоэнергетики. Термохимия.……………………………………………………………………….52
Задачи с решениями……………………………………………………………...55
Вопросы и задачи для самоподготовки……………………………………..….57
Занятие 8.Тема: Химическая кинетика и катализ.……………………….….62
Задачи с решениями…………………………………………………………..….64
Вопросы и задачи для самоподготовки……………………………………..….67
Лабораторные работы……………..…………………………………………….70
Занятие 9.Тема: Химическое равновесие.………………..…………………….73
Задачи с решениями……………………………………………………………....75
Вопросы и задачи для самоподготовки……………………………….………....78
Лабораторные работы………………………………………………..…………..83
Экзаменационные вопросы…………………………………..………..………....85
Приложение………………………………………………..…………..………....91
Литература……………………………………………………………..…….….102
ЗАНЯТИЕ 1
Тема: Способы выражения концентрации растворов.
Под концентрацией раствора понимают содержание растворённого вещества (в г или моль) в единице массы или объёма раствора или растворителя.
Различают приближённые и точные способы. К приближённым относятся понятия разбавленный, концентрированный, ненасыщенный, насыщенный и пересыщенный растворы. К точным способам выражения концентрации относятся:
1. Массовая доля растворённого вещества w(Х) представляет собой отноше-ние массы растворённого вещества (m(X)) к массе раствора (m(p-p)); это безразмерная величина, выражаемая в долях единицы, в сотых долях или процентах (%), в тысячных долях или промилле (%о), в миллионных долях или в млн-1. Например, w(Х) = 0,005 = 0,5% = 5 %о = 5000 млн-1.
В медицинской литературе массовую долю принято выражать в грамм-процентах (г%) (равнозначно процентам), миллиграмм-процентах (мг% или 10-3 г%) и в микрограмм-процентах (мкг%или 10-6 г%). Таким образом, w(Х) = 0,005 = 0,5% = 0,5 г% = 500 мг% = 500000 мкг%. Например, 5%-ный раствор - это пятипроцентный раствор или раствор с массовой долей растворённого вещества, равной 5% или 0,05.
2. Молярная доля c(X) представляет собой отношение количества вещества компонента раствора n(Xi) к общему количеству всех компонентов Sn(Xi), составляющих раствор. Это безразмерная величина, выражаемая в долях единицы или процентах.
3. Объёмная доля j(X) представляет собой отношение объёма компонента раствора (жидкости) V(X) к общему объёму раствора (смеси жидкостей) V(р-р). И эта безразмерная величина может выражаться как в долях единицы, так и в процентах.
4. Молярная концентрация С(Х) представляет собой отношение количества вещества компонента раствораn(X) к объёму раствора V(р-р); размерность - моль/л. Например, 0,1 М раствор означает децимолярный раствор или раствор с молярной концентрацией растворённого вещества, равной 0,1 моль/л.
5. Молярная концентрация эквивалента (или нормальная концентрация)  представляет собой отношение количества вещества эквивалента в растворе n(
представляет собой отношение количества вещества эквивалента в растворе n(  ) к объёму раствора; размерность - моль/л.
) к объёму раствора; размерность - моль/л.
Понятие «эквивалент вещества» связано с конкретной реакцией, в которой вещество участвует. Эквивалент (  ) - это условная или реальная частица вещества Х, которая в данной кислотно-основной реакции эквивалентна одному иону водорода или одному электрону - в данной окислительно-восста-новительной реакции. Эквивалент одноосновной кислоты или однокислотного основания - это всегда реальная частица, молекула Х. В случае многоосновных кислот и многокислотных оснований эквивалентом может быть реальная молекула Х или её какая-то часть (доля) -
) - это условная или реальная частица вещества Х, которая в данной кислотно-основной реакции эквивалентна одному иону водорода или одному электрону - в данной окислительно-восста-новительной реакции. Эквивалент одноосновной кислоты или однокислотного основания - это всегда реальная частица, молекула Х. В случае многоосновных кислот и многокислотных оснований эквивалентом может быть реальная молекула Х или её какая-то часть (доля) -  . Число, показывающее долю реальной частицы, эквивалентной одному иону водорода в реакциях кислотно-основного типа или одному электрону - в окислительно-восстановительных реакциях, называется фактором эквивалентности (fэкв.(Х) или
. Число, показывающее долю реальной частицы, эквивалентной одному иону водорода в реакциях кислотно-основного типа или одному электрону - в окислительно-восстановительных реакциях, называется фактором эквивалентности (fэкв.(Х) или  ).
).
Примеры определения эквивалентов различных веществ в различных реакциях приведены в таблицах 1 и 2 Приложения.
Если в химической реакции участвуют два вещества Х1 и Х2, то по закону эквивалентов количество эквивалента одного вещества n(  1) равно количеству эквивалента второго вещества n(
1) равно количеству эквивалента второго вещества n(  2), т.е.:
2), т.е.:
n(  1) = n(
1) = n(  2).
2).
Если кислотно-основная реакция протекает до конца, то при нахождении фактора эквивалентности кислот, оснований и солей следует учесть, что Z - это основность кислоты или кислотность основания, а в случае солей - произведение числа атомов металла, образующего соль, на его валентность.
Один моль эквивалентов вещества Х содержит число Авогадро частиц (6,02.1023 эквивалентов Х). Молярная масса вещества эквивалента 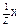 определяется произведением фактора эквивалентности на молярную массу вещества: М(
определяется произведением фактора эквивалентности на молярную массу вещества: М(  ) =
) =  .
.
Растворы с той или иной нормальной концентрацией С(  )* растворённого вещества используются для вполне конкретных реакций. Например, 0,01 н раствор или сантинормальный раствор, раствор с нормальной концентрацией растворённого вещества, равной 0,01 моль/л; 0,001 N раствор или миллинормальный раствор.
)* растворённого вещества используются для вполне конкретных реакций. Например, 0,01 н раствор или сантинормальный раствор, раствор с нормальной концентрацией растворённого вещества, равной 0,01 моль/л; 0,001 N раствор или миллинормальный раствор.
6. Моляльность (моляльная концентрация) раствора в(Х) представляет собой отношение количества растворённого вещества v (X) к массе растворителя
m(р-тель); размерность - моль/кг.
* - допускаются следующие обозначения: нормальной концентрации N(Х) вместо С(  ), моляльной концентрации Сm(Х) вместо в(Х).
), моляльной концентрации Сm(Х) вместо в(Х).
7. Титр (или массовая концентрация) t(X) представляет собой отношение массы растворённого вещества к объёму раствора; размерность - г/мл.
Формулы, позволяющие производить расчёт массовых, объёмных и молярных долей, титра, а также различных видов концентраций раствора приведены в таблице 3 Приложения.
По закону эквивалентов, если взаимодействуют растворы двух веществ V(p-р X1) и V(p-p X2) с нормальной концентрацией  и
и  , cоответ-ственно и титром t(X1) и t(X2) , то:
, cоответ-ственно и титром t(X1) и t(X2) , то:
 ;
;  .
.
Задачи с решениями.
Массовая доля компонента.
1. Глауберова соль Na2SO4.10H2O применяется при лечении желудочно-кишечных заболеваний как слабительное. Сколько (г) Na2SO4.10H2O нужно для приготовления 250 г раствора, с массовой долей Na2SO4, равной 5%.
| Дано: m(p-p) = 250 г. w(Na2SO4) = 5% = 0,05 m(Na2SO4.10H2O) = ? M(Na2SO4) = 142 г/моль M(Na2SO4.10H2O)=322 г/моль | Решение:
1) m(Na2SO4 = 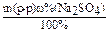 =
250.0,05 = 12,5 г;
2) по стехиометрической схеме:
Na2SO4 ® Na2SO4.10H2O
n(Na2SO4) = n(Na2SO4.10H2O) =
250.0,05 = 12,5 г;
2) по стехиометрической схеме:
Na2SO4 ® Na2SO4.10H2O
n(Na2SO4) = n(Na2SO4.10H2O)
 m(Na2SO4.10H2O) = 12,5.322/142 = 28,4 г.
Ответ: 28,4 г. m(Na2SO4.10H2O) = 12,5.322/142 = 28,4 г.
Ответ: 28,4 г.
|
2. Сульфат цинка ZnSO4 применяется в виде раствора с массовой долей, равной 0,25%, в качестве глазных капель. Сколько (г) воды нужно добавить к 25 г раствора с массовой долей ZnSO4, равной 2%, чтобы приготовить глазные капли?
      Дано:
m(p-p) = 25 г
w1(ZnSO4) = 2%
w2(ZnSO4) = 0,25%
m(H2O) = ? Дано:
m(p-p) = 25 г
w1(ZnSO4) = 2%
w2(ZnSO4) = 0,25%
m(H2O) = ?
| Решение:
В соответствии с «правилом креста» составим схему:
2% 0,25
0,25%
0% 1,75
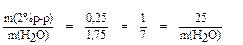 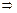
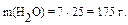 Ответ: 175 г. Ответ: 175 г.
|
3. Для компенсации недостатка соляной кислоты в желудочном соке применяют её растворы как лекарственные формы. Сколько (мл) 24%-ного раствора HCl с плотностью 1,12 г/мл необходимо для приготовления 500 г раствора с массовой долей 5%.
| Дано: r(p-p1) = 1,12 г/мл w1%(HCl) = 24% m(p-p 2) = 500 г w2%(HCl) = 5% V(p-p 1) = ? | Решение:
m(HCl) =  = 500.0,05 = 25 г.
w1%(HCl) = = 500.0,05 = 25 г.
w1%(HCl) =  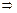 V(p-p 1) =
V(p-p 1) = 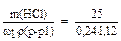 = 93 (мл).
Ответ: 93 мл. = 93 (мл).
Ответ: 93 мл.
|
4. Определите массовую долю (в %) HCl в растворе, полученном при смешивании 50 мл раствора с массовой долей 20% и 20 мл раствора, с массовой долей 10%.
| Дано: V(p-p1) = 50 мл r(p-p1)=1,1г/мл w1%(HCl)= 20% V(p-p 2) = 20 мл | Решение: 1) m1(HCl)=m(p-p1).w1(HCl)=V(p-p1).r(p-р1).w1(HCl) = 50.1,1.0,2 = 11 (г) 2) m2(HCl) = V(p-p 2).r(p-p2).w2(HCl) = 20.1,05.0,1= 2,1 (г) |
| r(p-p2)=1,05 г/мл w2%(HCl) = 10% w3%(HCl) = ? | 3) w3%(HCl)=  = 17,2%.
Ответ: 17,2%.
= 17,2%.
Ответ: 17,2%.
|
Молярная концентрация
5. Для определения времени рекальцификации кровяной плазмы применяется раствор CaCl2 с молярной концентрацией 0,025 моль/л. Сколько (г) CaCl2 необходимо для приготовления 250 мл этого раствора?
| Дано: C(CaCl2) = 0,025 моль/л V(p-p) = 250 мл m(CaCl2) = ? | Решение: V(p-p) = 250 мл = 0,25 л m(CaCl2) = C(CaCl2).М(CaCl2).V(p-p) = 0,025.111.0,25 = 0,6938 (г). Ответ: 0,6938 г. |
6. Сколько (мл) раствора H2SO4 с плотностью 1,26 г/мл (34,6%) нужно для приготовления 3 л 0,12 М раствора?
| Дано: r(p-p1) = 1,26 г/мл w1%(H2SO4) = 34,6% V(p-p 2) = 3 л C2(H2SO4)=0,12моль/л V(p-p 1) = ? | Решение:
m1(H2SO4) = m2(H2SO4)
1) V(p-p1).r(p-p1).w1(H2SO4) = C2(H2SO4).M(H2SO4).V(p-p 2);
2) V(p-p 1).1,26.0,346 = 0,12.98.3 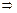 V(p-p1) =
V(p-p1) =  = 81 (мл)
Ответ: 81 мл. = 81 (мл)
Ответ: 81 мл.
|
7. Раствор NaCl с массовой долей 0,85% (r = 1,005 г/мл), называемый физиологическим раствором, применяется для внутривенных вливаний. Определите молярную концентрацию этого раствора.
| Дано: w1%(NaCl) = 0,85% r(p-p) = 1,005 г/мл C(NaCl) = ? | Решение: I вариант:
Пусть V(p-p) = 1000 мл = 1 л; тогда:
m(р-р) = r(p-p).V(p-p) = 1,005.1000 = 1005 (г);
w1(NaCl) = 0,0085;
C(NaCl) =  = =
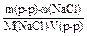 = =  = 0,146 моль/л;
II вариант: В соответствии с формулой, приведённой в таблице 3 Приложения:
C(NaCl) = = 0,146 моль/л;
II вариант: В соответствии с формулой, приведённой в таблице 3 Приложения:
C(NaCl) = 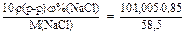 = 0,146 (моль/л).
Ответ: 0,146 моль/л или 0,146 М. = 0,146 (моль/л).
Ответ: 0,146 моль/л или 0,146 М.
|
|
из
5.00
|
Обсуждение в статье: Массовая доля компонента |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

