 |
Главная |
СОПОЛИМЕРИЗАЦИЯ МЕТИЛМЕТАКРИЛАТА СО СТИРОЛОМ
|
из
5.00
|
Лабораторные работы
ЛАБОРАТОРНАЯ РАБОТА  №1
№1
ИЗУЧЕНИЕ КИНЕТИКИ РАДИКАЛЬНОЙ ПОЛИМЕРИЗАЦИИ МЕТИЛМЕТАКРИЛАТА (СТИРОЛА) В МАССЕ ДИЛАТОМЕТРИЧЕСКИМ МЕТОДОМ
Задание. Напишите схему реакции элементарных стадий процесса радикальной полимеризации метилметакрилата (стирола) в присутствии азо-бис-изомасляной кислоты.
Построить график зависимости степени превращения от времени реакции на основании данных дилатометрии.
Цель работы: изучить кинетику радикальной полимеризации метилметакрилата или стирола в массе в присутствии инициатора динитрила азо-бис-изомасляной кислоты (ДАК) дилатометрическим методом; .
Реактивы: метилметакрилат (стирол), динитрил азо-бис-изомасляной кислоты (ДАК) – 0.5% от массы мономера, метанол 25 см3 растворители (бензол, ацетон, толуол).
Приборы и посуда: термостат, дилатометр со шкалой, секундомер, колба коническая со шлифом, пипетка на 10 см3. , цилиндр мерный на 25 см3 ,вискозиметр Оствальда или Убеллода.
Методика работы: Приготовить 10 см3 раствора ДАК в ММА. Установить в термостате температуру 60 °С, заполнить предварительно продутый аргоном дилатометр приготовленным раствором с помощью воронки с капилляром так, чтобы мениск слегка возвышался над ячейкой дилатометра. Продуть дилатометр аргоном с помощью длинной иглы в течении 15 мин., закрыть пробкой, укрепить шкалу и поместить в термостат. Через 5 мин. зафиксировать уровень мениска на шкале. Последующие измерения делать через 5 мин. в течение 40 – 60 мин. По истечении указанного времени содержимое дилатометра осадить метиловым спиртом. Полимер выделить и сушить в сушильном шкафу до постояннои массы, определить выход.
Обработка результатов
В основе метода дилатометрии лежит изменение объема реакционной системы в результате полимеризации. Образование полимера связано с увеличением плотности, а следовательно, с уменьшением объема реакционной смеси. Степень превращения вычисляют из соотношения :
Степень превращения = 
 ;
; 
где 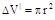
 - первоначальный объем мономера;
- первоначальный объем мономера;
 - изменение объема;
- изменение объема;
r - радиус капилляра, см;
 - изменение мениска по шкале капилляра, см
- изменение мениска по шкале капилляра, см
 ;
;
 - удельный объем мономера;
- удельный объем мономера;
 - удельный объем полимера;
- удельный объем полимера;
где:  и
и 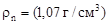 соответственно плотности мономера и полимера
соответственно плотности мономера и полимера
На основании полученных данных построить график зависимости степени превращения А от продолжительности реакции.Для нескольких измерений рассчитать значение скорости полимеризации и вычислить среднюю величину. Скорость полимеризации вычисляется из соотношения:

где:  - изменение объема за время
- изменение объема за время  ,
, 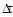 - время в течение которого произошло изменение объема равное
- время в течение которого произошло изменение объема равное  ;
;
 - первоначальный объем мономера
- первоначальный объем мономера 
m – молекулярная масса мономера.
Основная литература: 9[36-38]
Дополнительная литература: 19[4-11]
Контрольные вопросы
1.В чем суть дилатометрического метода исследования кинетики радикальной полимеризации?
2.Напишите реакции разложения наиболее часто применяемых химических инициаторов?
3.Как зависит скорость радикальной полимеризации от концентрации инициатора и мономера?
4.Назовите наиболее часто применяемые инициаторы и мономеры радикальной полимеризации.

ЛАБОРАТОРНАЯ РАБОТА  №2
№2
ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОЙ МАССЫ ПОЛИМЕРОВ ВИСКОЗИМЕТРИЧЕСИМ МЕТОДОМ.
Задание. Приготовить растворы полиметилметакрилата (полистирола) различной концентрации. Измерить время истечения каждого раствора. Построить график зависимости ηуд/c от С.Рассчитать молекулярную массу полимера по значению характеристической вязкости.
 Цель работы: определить молекулярную массу полимеров вискозиметрическим методом.
Цель работы: определить молекулярную массу полимеров вискозиметрическим методом.
Реактивы: полиметилметакрилат или полистирол , бензол, толуол или ацетон, 50см3 раствор полимера С=1г/100см3.
Приборы и посуда: термостат, секундомер, колба коническая со шлифом, пипетка на 10см3, мерный цилиндр на 25см3.
Методика работы. Для приготовления раствора полимера на аналитических весах взвешивают 0,3 г полимера и растворяют в 30  чистом растворителе. После полного растворения полимера раствор отфильтровывают через стеклянный фильтр. Из 1% раствора постепенно разбавлением готовят следующие растворы. Для этого во вторую колбу наливают 10
чистом растворителе. После полного растворения полимера раствор отфильтровывают через стеклянный фильтр. Из 1% раствора постепенно разбавлением готовят следующие растворы. Для этого во вторую колбу наливают 10  1%-ного раствора и, добавив туда 10
1%-ного раствора и, добавив туда 10  растворителя, получают 20
растворителя, получают 20  0,5%-ного раствора. Далее, подобным образом разбавляя 2 раза, приготавливают 0,25 и 0,125%-ные растворы. Первоначально измеряют время истечения чистого растворителя. Для этого чистый сухой вискозиметр устанавливают вертикально в термостат и через широкое колено вискозиметра заливают 10
0,5%-ного раствора. Далее, подобным образом разбавляя 2 раза, приготавливают 0,25 и 0,125%-ные растворы. Первоначально измеряют время истечения чистого растворителя. Для этого чистый сухой вискозиметр устанавливают вертикально в термостат и через широкое колено вискозиметра заливают 10  растворителя. После10 -минутного термостатирования, пользуясь резиновой грушей, капилляр и измерительный шарик два раза промывают путем всасывания и выдавливания растворителя. Время истечения растворителя определяют путем заполнения капилляра и измерительного шарика выше верхней метки над шариком до нижней под ним. Время истечения определяют три раза и берут среднее значение. Определив время истечения чистого растворителя, вискозиметр извлекают из термостата, сливают растворитель, промывают ацетоном и сушат. Затем определяют время истечения растворов полимера, начиная с меньшей концентрации. В вискозиметр, установленный в термостате, наливают 10
растворителя. После10 -минутного термостатирования, пользуясь резиновой грушей, капилляр и измерительный шарик два раза промывают путем всасывания и выдавливания растворителя. Время истечения растворителя определяют путем заполнения капилляра и измерительного шарика выше верхней метки над шариком до нижней под ним. Время истечения определяют три раза и берут среднее значение. Определив время истечения чистого растворителя, вискозиметр извлекают из термостата, сливают растворитель, промывают ацетоном и сушат. Затем определяют время истечения растворов полимера, начиная с меньшей концентрации. В вискозиметр, установленный в термостате, наливают 10  раствора и после термостатирования определяют время истечения не менее трех раз. После измерений вискозиметр промывают 2-3 раза следующим по порядку раствором. Берут среднее значение из трех измерений. Результаты измерений оформляют в виде таблицы.1. Затем строят график зависимости
раствора и после термостатирования определяют время истечения не менее трех раз. После измерений вискозиметр промывают 2-3 раза следующим по порядку раствором. Берут среднее значение из трех измерений. Результаты измерений оформляют в виде таблицы.1. Затем строят график зависимости  от концентрации полимера (С) и полученную прямую экстраполируют до пересечения с осью ординаты (С = 0). Отрезок, отсекаемый на оси ординат в точке, соответствующей нулевой концентрации, равняется значению характеристической вязкости [
от концентрации полимера (С) и полученную прямую экстраполируют до пересечения с осью ординаты (С = 0). Отрезок, отсекаемый на оси ординат в точке, соответствующей нулевой концентрации, равняется значению характеристической вязкости [  ].
].
Таблица 1. Форма записи результатов:

Концентрация
раствора, 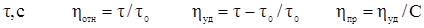 С, г/
С, г/ 
|
Определив значение [  ], по известным значениям К и α (см. таблица.2) по уравнению Марка-Куна-Хаувинга определяют средневязкостную молекулярную массу полимера.
], по известным значениям К и α (см. таблица.2) по уравнению Марка-Куна-Хаувинга определяют средневязкостную молекулярную массу полимера.
Таблица 2. Значения К и α в уравнении Марка-Куна-Хаувинга.
| Полимер | Растворитель | t, C | 
| α |
| Полиметилме- такрилат | Бензол | 0.468 | 0,77 | |
| Ацетон | 0,575 | 0,70 | ||
| Толуол | 0,71 | 0,73 | ||
| Полистирол | Бензол | 1,23 | 0,72 | |
| Бензол | 1,06 | 0,74 | ||
| Толуол | 1,70 | 0,69 |
Обработка результатов
Молекулярная масса полимера, определенная с помощью вискозиметрического метода, носит название средневязкостной молекулярной массы. Зависимость характеристической вязкости [η] раствора от молекулярной массы полимера описывается уравнением Марка-Куна-Хаувинга:
[η]=КМα
где: К и α- парометы, зависящие от природы полимера, растворителя и температуры.Значение К характеризует взаимодействие между полимером и растворителем и в зависимости от условий находится в пределах
К=10-2-10-5.
Параметр α зависит от формы макромолекул и колеблется от 0.5 до 1.
Для определения характеристической вязкости готовят растворы полимера разной концентрации (1,0; 0,5; 0,25 и 0,125 см3/г) и измеряют время истечения чистого растворителя (τ) равных объемов через капилляр вискозиметра при заданной температуре. На основании полученных значений τ0 и τ для различных концентратции растворов полимеров определяют относительную, удельную и приведенную вязкость.
Относительная вязкость представляет собой величину, равную отношению времени истечения раствора ко времени истечения растворителя;
ηотн=τ/τ0
Удельной вязкостью называют отношение разности вязкости раствора и растворителя к вязкости растворителя:
ηуд=τ-τ0/τ0=ηотн-1
Приведенная вязкость- это отношение удельной вязкость раствора к его концентрации:
ηпр=ηуд/С
Характеристической вязкость называют предельное отношение значения ηуд/C при концентрации раствора полимера, стремящейся к нулю:
[η]=(ηуд/C)c  0
0
Для расчета молекулярной массы уравнение Марка-Куна-Хаувинга применяют в логарифмической форме:

Основная литература: 9 [36-38]
Дополнительная литература: 19 [4-11]
Контрольные вопросы
- Что такое средняя молекулярная масса?
- Какими методами определяются средчисловая и среднемассовая молекулярные массы?
- Опишите метод определения средневязкостной молекулярной массы?
- В чем физический смысл констант К и α в уравнении Марка-Куна-Хаувинга
 ?
?
ЛАБОРАТОРНАЯ РАБОТА  №3
№3
СОПОЛИМЕРИЗАЦИЯ МЕТИЛМЕТАКРИЛАТА СО СТИРОЛОМ
Задание. Написать схему реакции сополимеризации ММА с СТ в присутствии азобисизобутиронитрила. Определить выход сополимеров и на основании их сделать выводы о влянии исходного состава мономерной смеси на скорость реакции. По данным содержания углерода (данные анализа выдаются преподавателем ) оределить состав сополимеров и рассчитать константы сополимеризации различными методами.
Цель работы: провести радикальную сополимеризацию метилметакрилата (ММА) со стиролом (СТ) в массе и выделить полученные сополимеры для определение их состава.
Реактивы: метилметакрилат (  =0.936 г/см3) стирол (
=0.936 г/см3) стирол (  =0.906 г/см3), азобисизобутиронитрил 0.5% от массы смеси мономеров, метанол (изооктан или бензин).
=0.906 г/см3), азобисизобутиронитрил 0.5% от массы смеси мономеров, метанол (изооктан или бензин).
Приборы и посуда: термостат, ампулы 3 шт, мерный цилиндр или пипетка на 10 см3, стаканы на 100 см3.
Методика работы. Рассчитывают необходимые количества ММА и СТ для приготовления 5см3 растворов при трех исходных соотношениях мономеров. Результаты расчета сводят в таблицу.
Таблица- Данные сополимеризации ММА (М1) с СТ (М2)
| Исх.соотношение мономеров, мол,% | Колич-во реакцион. смеси, см3 | Количество мономеров | Содержа-ние С, % | Состав полимеров, мол,% | |||||||
| [М1] | [М2] | ММА 
| СТ | [m1] | [m2] | ||||||
| Г | см3 | г | см3 | ||||||||
Чистые и высушенные ампулы нумеруют, заливают в каждую рассчитонное количество смеси ММА-СТ, в которой предварительно растворен инициатор в количестве 0,5% от сумарнной массы смеси мономеров. Ампулы, закрытие пробками или запаянные, помещают в термостат на 1,5 часа (t=600С). По истечении времени ампулы охлаждают до комнатной температуры и выливают содержимое при перемешивании в стакан с осадителем (метанол, бензин или изооктан,30-50 см3 ). Осадок полимера промывают декантацией, доводят до постоянной массы в сушильном шкафу и взвешивают для определения выхода. Состав сополимеров определяют по данным элементного анализа на содержание углерода, значения которых также вносят в таблицу.На оснований состава исходной мономерной смеси и состава сополимеров по управлениям Майо-Льюиса и Файнмана и Росса расчитывают константы сополимеризации r1 и r2 .
Обработка результатов
Определение состава сополимеров. Содержание мономеров М1 и М2 в сополимере [m1] и [m2] определяют по уравнению:
[m1]=
[m2]=100-[m1] , мол. %
где m1 и m2 –молекулярные массы мономеров М1 и М2, г
С1 и С2-содержание углерода в мономерах М1 и М2, вес.%
С- содержание углерода в сополимере,вес.% (данные элементного анализа).
Определение констант сополимеризации.Метод Майо-Льюиса. Преобразуя уравнение Майо-Льюса
 ,
,
где [m1] и [m2] –содержание мономеров М1 и М2 в сополимер, мол. .%
[M1]и [M2] – содержание мономеров М1 и М2 в исходной мономерной смеси, мол.%
можно получить следующие выражение:
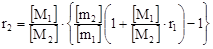
Подставляя в это выражение экспериментальные величины [ M1], [M2], [m1] и [m2] и задаваясь произвольными значениями r1, строят прямую в координатах r2 - r1. Для каждого соотношения получается одна прямая линия, а прямые для различных соотношений пересекаются в одной точке или образуют многоугольник, центр которого соответствует истинным значениям контакт сополимеризации r1 и r2.
Метод Файнмана-Росса. Уравнение Майо-Льюиса можно преобразить в такой вид:



 ,
,
где F= [M1] / [M2] : f = [m1] / [m2]
грифическое решение которого дает для всех соотношений мономеров одну прямую линию. Из опытных данных строится график зависимости у=f(x),
где  , а х =
, а х = 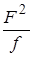 .
.
Тангенс угла наклона полученной прямой равен r1, а отсекаемый на оси ординат отрезок соответствует r2 с обратным знаком
Основная литература: 9[42-44]
Контрольные вопросы
- В чем физический смысл констант сополимеризации r2 и r1?
- Напишите уравнение Майо-Льюиса.
- Какие типы сополимеров существуют? Опишите их по диаграмме составов.
- Роль реакции сополимеризации?
|
из
5.00
|
Обсуждение в статье: СОПОЛИМЕРИЗАЦИЯ МЕТИЛМЕТАКРИЛАТА СО СТИРОЛОМ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

