 |
Главная |
Опыт 5. Взаимное усиление гидролиза соли слабого
|
из
5.00
|
основания солью слабой кислоты
Описание опыта
Гидролиз соли усиливается, если связать один из ионов, образующийся в результате гидролиза, в слабый электролит. В результате гидролиза соли слабого основания в растворе образуются свободные ионы Н+ (рН < 7), а в результате гидролиза соли слабой кислоты - ионы ОН- (рН > 7). Но ионы Н+ и ОН- связывают друг друга в слабый электролит Н2О. Поэтому степень гидролиза солей увеличивается, то есть гидролиз одной соли усиливает гидролиз другой и наоборот. В результате гидролиз таких солей доходит до конца. Так если смешать растворы Al2(SO4)3 и Na2CO3, то в результате образуется осадок Al(ОН)3 и выделится СО2, но не образуется Al2(CO3)3.
| В растворе Al2(SO4)3 | |||
| Аl2(SO4)3 + 2НОН = 2AlОНSO4 + Н2SO4 | |||
| Al3+ + НОН = AlОН2+ + Н+ В растворе Na2CO3 Na2CO3 + НОН = NaНCO3 +NaОН CO32- + НОН = НCO3- + OН-
| |||
В соответствии с принципом Ле Шателье это усиливает гидролиз обеих солей: AlОН2+ + НОН = Al(ОН)2+ + Н+
Al(ОН)2+ + НОН = Al(ОН)3¯ + Н+
НCO3- + НОН = Н2CO3 + ОН-
¯ ¯
СО2 Н2О
В результате всех этих процессов:
Al2(SO4)3 + 3Na2CO3 + 3Н2О = 2Al(ОН)3¯ + 3СО2+ 3Na2SO4
Порядок выполнения.
1. Смешать в пробирке по 5-6 капель сульфата алюминия и карбоната натрия.
Задание
1. Напишите уравнения и признаки реакций при смешивании растворов сульфата алюминия и карбоната натрия.
2. Напишите уравнения реакций, которые доказывают, что образовался осадок гидроксида алюминия, а не карбоната алюминия.
3. Докажите, что образовавшийся осадок Al(ОН)3.
4. Рассчитайте, при каком рН начинается образование осадка Al(ОН)3, если концентрация [Al3+] в растворе равна 0,1 моль/л.
5. Оформите отчет о лабораторной работе №4.
ЛАБОРАТОРНАЯ РАБОТА №5
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
Цель работы: ознакомление со способами получения и наиболее характерными свойствами комплексных соединений.
Оборудование: Растворы: AgCl, CuSO4, NiCl2, Zn(NO3)2, NH4OH, CdCl2, HgCl2, Na2SO4, NaOH, AlCl3, SnCl2, PbCl2, CrCl3, H2C2O4, FeCl2, FeCl3, KCSN, K4[Fe(CN)6], K3[Fe(CN)6], NH4Fe(SO4)2, Na3[Co(NO2)6].
Литература: Р.Л.Глинка. Общая химия. §§203-208.
.
Теоретическая часть
Комплексными (координационными) соединениями называются сложные соединения, образование которых из более простых частиц, молекул, ионов не связано с возникновением новых электронных пар. Примеры комплексных соединений:
К3[Co(СN)6] – комплексное соединение анионного типа;
[Ag(NH3)2]NO3 – комплексное соединение катионного типа;
[Pt(NH3)2Cl2] – электронейтральное комплексное соединение.
Комплексные соединения состоят из центрального атома (или иона) (в приведенных примерах – ионы Co3+, Ag+, Pt2+) и связанных с ним молекул или ионов (NH3, CN-, Cl-) – лигандов. Центральный атом комплексообразователь – акцептор, а лиганды - доноры электронов. При образовании комплекса между ними возникает донорно-акцепторная (координационная) связь.
Число атомов лигандов, координированных центральным атомом, называется координационным числом (к.ч.). В соединении [Ag(NH3)2]NO3 координационное число Ag+ равно 2. Лиганды, связанные с центральным атомом, образуют внутреннюю координационную сферу комплексного соединения (например, в комплексе [Ag(NH3)2]NO3 внутренней сферой является [Ag(NH3)2]+). В растворе комплекс сохраняет индивидуальность, хотя имеет место и диссоциация:
[Ag(NH3)2]+ D [Ag(NH3)]+ + NH3
[Ag(NH3)]+ D Ag+ + NH3
Каждому из рассмотренных процессов соответствует константа нестойкости:
К1нестойкости =  ;
;
К2нестойкости = 
К1-2нестойкости = К1нестойкости × К2нестойкости
К1-2нестойкости = 
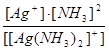
Константа суммарного процесса – общая константа нестойкости комплексного иона – равна произведению последовательных констант всех его ступеней. Чем меньше величина константы нестойкости, тем прочнее данный комплекс. Величина обратная константе нестойкости, называется константой устойчивости.
Кустойчивости = 1/Кнестойкости
Анионы и катионы (противоионы), входящие вместе с комплексом в состав координационного соединения образуют внешнюю сферу.
Катионные и анионные комплексные соединения обычно являются сильными электролитами и в водных растворах диссоциируют по типу сильного электролита, на ионы внутренней и внешней сфер. Электронейтральные комплексы не являются электролитами и в водных растворах не диссоциируют. Заряды внутренней и внешней сфер равны между собой по величине и противоположны по знакам. Заряд комплексного иона равен сумме зарядов комплексообразователя и лигандов. Пример:
К3[Co3+(СN-)6] D 3K+ + [Co(СN)6]3-
[Ag+(NH30 )2]NO3 D [Ag(NH3)2]+ + NO3-
В зависимости от числа донорных атомов лиганда, способных к координации, различают моно-, би- и …полидентатные лиганды. Например, оксалат-ион С2О42- является бидентатным лигандом. Лиганды, координирующиеся через два и более донорных атомов к одному центральному атому, называется хелатным. Примером хелатного лиганда является двунатриевая соль этилендиаминтетрауксусной кислоты (ЭДТА) – трилон Б.
|
из
5.00
|
Обсуждение в статье: Опыт 5. Взаимное усиление гидролиза соли слабого |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

