 |
Главная |
Физико-химические свойства
|
из
5.00
|
Министерство образования и науки Российской Федерации
РОССИЙСКИЙ ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ УНИВЕРСИТЕТ
Имени Д.И. Менделеева
Кафедра композиционных материалов и технологий защиты от коррозии
РЕФЕРАТ
«Цирконий. История элемента, металла и сплавов на его основе.»
Выполнила: студентка
3 курса, группа ЗДО-32
Трегубова М.А.
Зачетная книжка № 0-08172
Проверил: Жуков А.П.
Москва 2014
Содержание.
1. Введение. Стр.2
2. История и происхождение названия. Стр.3
3. Нахождение в природе. Стр.4
4. Получение. Стр.6
4.1 Двуокись циркония. Стр.10
5. Физико-химические свойства. Стр.11
5.1 История физико-химических свойств Zr. Стр.13
6. Цирконий, воздух и вода. Cтр.18
7. Цирконий и металлургия. Стр.20
7.1 Проблема циркония «реакторной чистоты». Стр. 22
8. Применение Zr и его сплавов. Стр.24
9. Заключение. Стр.27
10. Список использованной литературы. Стр.28
Введение.
Данная работа дает возможность проанализировать цирконий во всех аспектах, изучить историю этого металла, посмотреть с точки зрения материаловедения на сам элемент, и сплавы на его основе.
Цирко́ний (лат. Zirconium; обозначается символом Zr) — элемент побочной подгруппы четвёртой группы пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 40. Простое вещество цирконий— блестящий металл серебристо-серого цвета. Обладает высокой пластичностью, устойчив к коррозии. Существует в двух кристаллических модификациях: α-Zr с гексагональной решёткой типа магния, β-Zr с кубической объёмноцентрированной решёткой типа α-Fe, температура перехода α↔β 863 °C.[1, с. 384]
Чистый, не содержащий примесей цирконий легкостью поддается холодной и горячей обработке. Чистый цирконий — один из лучших конструкционных материалов для атомных реакторов — становится совершенно непригодным для этой цели, если в нем содержится даже незначительная примесь гафния, который не имеет собственных минералов и в природе обычно сопутствует цирконию [3,1]. Металл цирконий применяют при выплавке стали для удаления окислов и нитритов, а диоксид циркония применяется в огнеупорной керамике, в производстве фарфора и глазурей [2,13].

История и происхождение названия.
В 1789 году немецкий химик Мартин Генрих Клапрот, анализируя одну из разновидностей минерала циркона, обнаружил новый элемент, который он назвал цирконием. Благодаря красивой окраске - золотистой, оранжевой, розовой - циркон еще в эпоху Александра Македонского считался драгоценным камнем. Название минерала происходит, по-видимому, от персидского слова "заргун" - золотистый.
Циркон (в литературе встречаются и другие названия этого минерала: гиацинт, яцинт, яргон, джаргон) использовали в старину не только как украшение, но и как амулет, который "сердце обвеселит, и кручину и неподобные мысли отгоняет, разум и честь умножает". Один из древнерусских эскулапов с профессиональной осведомленностью утверждал в своем труде о медицине, что тот "кто яхонт червленый при себе носит, снов страшных и лихих не увидит, скрепит сердце свое и в людях честен будет". (Яхонтом на Руси называли многие драгоценные камни, в том числе и цейлонский гиацинт).
В свободном виде цирконий впервые выделил в 1824 году шведский химик Йенс Якоб Берцелиус. Однако получить чистый цирконий в те времена не представлялось возможным, и физические свойства этого металла долгое время не были изучены. В течение десятков лет цирконий, подобно многим новым металлам, не мог найти себе занятие по душе, в то время как такие давно известные металлы, как железо, медь, свинец, умели показать товар лицом и потому не страдали от отсутствия предложений.
Только в начале нашего века ученым удалось получить свободный от примесей цирконий и тщательно исследовать свойства этого металла. Оказалось, что у него есть постоянный спутник - гафний. Более 130 лет химики не замечали, что гафний присутствует (причем иногда в довольно
больших количествах) в цирконии. Объясняется это поразительным сходством их химических свойств.[4,c.137]
Нахождение в природе.
Соединения циркония широко распространены в литосфере. По разным данным кларк циркония от 170 до 250 г/т. Концентрация в морской воде 5·10−5 мг/л. Цирконий — литофильный элемент. В природе известны его соединения исключительно с кислородом в виде окислов и силикатов. Несмотря на то, что цирконий рассеянный элемент, насчитывается около 40 минералов, в которых цирконий присутствует в виде окислов или солей. В природе распространены главным образом циркон (ZrSiO4)(67,1 % ZrO2), бадделеит (ZrO2) и различные сложные минералы (эвдиалит (Na, Ca)5(Zr, Fe, Mn)[O,OH,Cl][Si6O17] и др.). Во всех земных месторождениях цирконию сопутствует Hf, который входит в минералы циркона благодаря изоморфному замещению атома Zr.
Циркон является самым распространенным циркониевым минералом. Он встречается во всех типах пород, но главным образом в гранитах и сиенитах. В графстве Гиндерсон (штат Северная Каролина) в пегматитах были найдены кристаллы циркона длиной в несколько сантиметров, а на Мадагаскаре были обнаружены кристаллы, вес которых исчисляется килограммами.
Бадделеит был найден Юссаком в 1892 году в Бразилии, основное месторождение находится в районе Посус-ди-Калдас. Там была найдена глыба бадделеита весом около 30 т, а в водных потоках и вдоль обрыва бадделеит встречается в виде аллювиальной гальки диаметром до 7,5 мм, известной под названием фавас (от португ. fava — боб). Фавас обычно содержит свыше 90 % двуокиси циркония[5, c. 36].
Наиболее крупные месторождения циркония расположены на территории США, Австралии, Бразилии, Индии.
В России, на долю которой приходится 10 % мировых запасов циркония (3 место в мире после Австралии и ЮАР), основными месторождениями являются: Ковдорское коренное бадделит-апатит-магнетитовое в Мурманской области, Туганское россыпное циркон-рутил-ильменитовое в Томской области, Центральное россыпное циркон-рутил-ильменитовое в Тамбовской области, Лукояновское россыпное циркон-рутил-ильменитовое в Нижегородской области, Катугинское коренное циркон-пирохлор-криолитовое в Читинской области и Улуг-Танзекское коренное циркон-пирохлор-колумбитовое.
Более 40% разведанных запасов диоксида циркония страны находится в рудах коренных комплексных редкометальных (с танталом, ниобием и другими металлами) месторождений, где минерал циркония – тот же, что и в россыпях, – циркон. Около 10% запасов циркония заключено в карбонатитовых рудах с бадделеитом – природным диоксидом циркония, являющимся наиболее дешевым циркониевым сырьём, используемым в производстве огнеупоров, абразивов, пигментов и тонкой технической керамики. За рубежом бадделеитовые руды в настоящее время не разрабатываются.
Государственным балансом запасов РФ учитывается 14 месторождений циркония, в том числе пять коренных и девять россыпных, из которых одно россыпное и два коренных – только с забалансовыми запасами. Наиболее перспективные объекты находятся в распределенном фонде недр. Относящееся к нераспределенному фонду крупное коренное Улуг-Танзекское месторождение циркон-пирохлор-колумбитовых руд в Республике Тыва находится в труднодоступном высокогорном районе.
В 2007 г. подготавливались к освоению пять месторождений циркониевых руд, на которые приходится почти половина (48%) разведанных запасов, в том числе коренное редкометальное Катугинское в Читинской области и четыре россыпных титан-циркониевых: Лукояновское в Нижегородской, Центральное в Тамбовской, Туганское в Томской, Тарское в Омской области. На Тарском и Туганском месторождениях продолжается опытно-промышленная отработка.[6,1]
Получение.
Выделенное когда-то Клапротом вещество не было новым элементом, но было окислом нового элемента, который впоследствии занял в таблице Д.И. Менделеева сороковую клетку. Пользуясь современными символами, формулу вещества, полученного Клапротом, записывают так: ZrO2.
Через 35 лет после опытов Клапрота известнейшему шведскому химику Йенсу Якобу Берцелиусу удалось получить металлический цирконий. Берцелиус восстановил фторцирконат калия металлическим натрием: К2[ZrF6] + 4Na → Zr + 2KF + 2NaF
и получил серебристо-серый металл.Цирконий, образовавшийся в результате этой реакции, был хрупким из-за значительного содержания примесей. Металл не поддавался обработке и не смог найти практического применения. Но можно было предположить, что очищенный цирконий, подобно многим другим металлам, окажется достаточно пластичным.
В XIX и начале XX в. многие ученые пытались получить чистый цирконий, но все попытки долгое время заканчивались неудачей. Не помог испытанный алюмотермический метод, не привели к цели опыты, авторы которых стремились получить металлический цирконий из растворов его солей. Последнее объясняется в первую очередь высоким химическим сродством циркония к кислороду.
Для того чтобы можно было получить какой-либо металл электролизом из раствора его соли, этот металл должен образовывать одноатомные ионы. А цирконий таких ионов не образует. Сульфат циркония Zr(SO4)2, например, существует только в концентрированной серной кислоте, а при разбавлении начинаются реакции гидролиза и комплексообразования. В конечном счете получается:
Zr(SO4)2 + Н2О → (ZrO)SO4 + H2SO4.
В водном растворе гидролизуется и хлористый цирконий:
ZrCl4 + Н2О → ZrOCl2 + 2HCl.
Некоторые исследователи считали, что им удалось-таки получить цирконий электролизом растворов, но они были введены в заблуждение видом продуктов, осевших на электродах. В одних случаях это были действительно металлы, но не цирконий, а никель или медь, примеси которых содержались в циркониевом сырье; в других – внешне похожая на металл гидроокись циркония.
Лишь в 20-х годах нашего столетия (через 100 лет после того, как Берцелиус получил первые образцы циркония!) был разработан первый промышленный способ получения этого металла.
Это метод «наращивания», разработанный голландскими учеными ван Аркелем и де Буром. Суть его заключается в том, что летучее соединение (в данном случае тетрайодид циркония ZrI4) подвергается термическому распаду в вакууме и на раскаленной нити вольфрама откладывается чистый металл.
Этим способом был получен металлический цирконий, поддающийся обработке – ковке, вальцовке, прокатке – примерно так же легко, как медь.
Позже металлурги обнаружили, что пластические свойства циркония зависят главным образом от содержания в нем кислорода. Если в расплавленный цирконий проникнет свыше 0,7% кислорода, то металл будет хрупким из-за образования твердых растворов кислорода в цирконии, свойства которых сильно отличаются от свойств чистого металла.
Метод наращивания получил сначала некоторое распространение, но высокая стоимость циркония, полученного этим методом, сильно ограничивала области его применения. А свойства циркония оказались интересными. (О них ниже.) Назрела необходимость в разработке нового, более дешевого способа получения циркония. Таким методом стал усовершенствованный метод Кролля.
Метод Кролля позволяет получать цирконий при вдвое меньших затратах, чем по методу наращивания. Схема этого производства предусматривает две основные стадии: двуокись циркония хлорируется, а полученный четыреххлористый цирконий восстанавливается металлическим магнием под слоем расплавленного металла. Конечный продукт – циркониевая губка переплавляется в прутки и в таком виде направляется потребителю.
В современной промышленности исходным сырьем для производства циркония являются циркониевые концентраты с массовым содержанием диоксида циркония не менее 60-65 %, получаемые обогащением циркониевых руд.
Основные методы получения металлического циркония из концентратов — хлоридный, фторидный и щелочной процессы.
Хлоридный процесс основан на перевод циркония в летучий тетрахлорид ZrCl4 (Tсублимации 331 °C) с дальнейшей его очисткой и последующим металлотермическим восстановлением магнием в циркониевую губку. Используются два варианта хлорирования концентратов: прямое хлорирование смеси циркониевых концентратов с коксом хлорируют при 900—1000 °С и хлорирование предварительно полученных спеканием концентратов с коксом смеси карбидов и карбонитридов циркония при 400—900 °С:

При фторидном методе на первой стадии циркониевый концентрат спекают с гексафторсиликатом калия при 600—700 °С:

Образовавшийся гексафторцирконат калия выщелачивают горячей водой и очищают фракционной перекристаллизацией от примеси гексафторгафната K2HfF6, после чего металлический цирконий получают электролизом расплава смеси гексафторцирконата калия и хлоридов калия и натрия.
Щелочной процесс является методом получения технически чистого диоксида циркония ZrO2, из которого металлический цирконий получают хлоридным или фторидным методом. В этом процессе цирконий переводится в растворимую форму спеканием концентрата с гидроксидом натрия при 600—650 °С, карбонатом натрия при 900—1100 °С либо со смесью карбоната и хлорида кальция при 1000—1300 °С, после чего образовавшиеся цирконаты натрия Na2ZrO3 или кальция CaZrO3 выщелачиваются соляной либо серной кислотами:

Водные растворы хлорида или сульфата цирконила далее очищаются и гидролизуются, осадок ZrO(OH)2 прокаливают и получают технический диоксид циркония ZrO2.
Двуокись циркония.
Пока ученые искали способ получения металлического циркония, практики уже начали применять некоторые из его соединений, в первую очередь двуокись циркония. Свойства двуокиси циркония в значительной мере зависят от того, каким способом она получена. ZrO2, образующаяся при прокаливании некоторых термически нестойких солей циркония, нерастворима в воде. Слабо прокаленная двуокись хорошо растворяется в кислотах, но, сильно прокаленная, она становится нерастворимой в минеральных кислотах, исключая плавиковую.
Еще одно интересное свойство: сильно нагретая двуокись циркония излучает свет настолько интенсивно, что ее можно применять в осветительной технике. Этим ее свойством воспользовался известный немецкий ученый Вальтер Герман Нернст. Стержни накаливания в лампе Нернста были изготовлены из ZrO2. В качестве источника света раскаленная двуокись циркония иногда и сейчас служит при лабораторных опытах.
В промышленности двуокись циркония первыми применили силикатные производства и металлургия. Еще в начале нашего века были изготовлены цирконовые огнеупоры, которые служат в три раза дольше обычных. Огнеупоры, содержащие добавку ZrO2, позволяют провести до 1200 плавок стали без ремонта печи. Это много.
Цирконовые кирпичи потеснили шамот (широко распространенный огнеупорный материал на основе глины или каолина) при выплавке металлического алюминия, и вот почему. Шамот сплавляется с алюминием, и на его поверхности образуются наросты шлака, которые надо периодически счищать. А цирконовые кирпичи расплавленным алюминием не смачиваются. Это позволяет печам, футерованным цирконом, непрерывно работать в течение десяти месяцев.
Значительные количества двуокиси циркония потребляют производства керамики, фарфора и стекла.
Список отраслей промышленности, нуждающихся в двуокиси циркония, можно было бы продолжить еще и еще. Но посмотрим, на что пригодился металлический цирконий, который так долго не удавалось получить.[7, 6]

Физико-химические свойства.
Цирконий — блестящий серебристо-серый металл. Существует в двух кристаллических модификациях:
- α-Zr — с гексагональной решёткой типа магния (а = 3,231 Å; с = 5,146 Å; z = 2; пространственная группа P63/mmc)
- β-Zr — с кубической объёмноцентрированной решёткой типа α-Fe (a = 3,61 Å; z = 2; пространственная группа Im3m). Переход α ↔ β происходит при 863 °C, ΔH перехода 3,89 кДж/моль. Добавки Al, Sn, Pb, Cd повышают, а Fe, Cr, Ni, Mo, Cu, Ti, Mn, Co, V и Nb понижают температуру перехода[2,1].
Плотность α-циркония при 20 °C равна 6,5107 г/см³; температура плавления Tпл — 1855 °C[2,1]; температура кипения Tкип — 4409 °C; удельная теплоёмкость (25-100 °C) 0,291 кДж/(кг·К) или 0,0693 кал/(г·°C), коэффициент теплопроводности (50 °C) 20,96 Вт/(м·К) или 0,050 кал/(см·сек·°C); температурный коэффициент линейного расширения (20-400 °C) 6,9·10−6; удельное электрическое сопротивление циркония высокой степени чистоты (20 °C) 44,1 мкОм·см. температура перехода в состояние сверхпроводимости 0,7 К[5, c. 48].
Цирконий парамагнитен; удельная магнитная восприимчивость увеличивается при нагревании и при −73 °C равна 1,28·10−6, а при 327 °C — 1,41·10−6. Сечение захвата тепловых нейтронов 0,18·10−28 м² (0,18 барн), примесь гафния увеличивает это значение, поэтому для изготовления твэлов применяется цирконий, хорошо очищенный от гафния. Чистый цирконий пластичен, легко поддаётся холодной и горячей обработке (прокатке, ковке, штамповке). Наличие растворённых в металле малых количеств кислорода, азота, водорода и углерода (или соединений этих элементов с цирконием) вызывает хрупкость циркония. Модуль упругости (20 °C) 97 ГН/м² (9700 кгс/мм²); предел прочности при растяжении 253 МН/м² (25,3 кгс/мм²); твёрдость по Бринеллю 640—670 МН/м² (64-67 кгс/мм²); на твёрдость очень сильное влияние оказывает содержание кислорода: при концентрации более 0,2 % цирконий не поддаётся холодной обработке давлением.
Внешняя электронная конфигурация атома циркония 4d25s2. Для циркония характерна степень окисления +4. Более низкие степени окисления +2 и +3 известны для циркония только в его соединениях с хлором, бромом и иодом.
Компактный цирконий медленно начинает окисляться в пределах 200—400 °C, покрываясь плёнкой циркония двуокиси ZrO2; выше 800 °C энергично взаимодействует с кислородом воздуха. Порошкообразный металл пирофорен — может воспламеняться на воздухе при обычной температуре. Цирконий активно поглощает водород уже при 300 °C, образуя твёрдый раствор и гидриды ZrH и ZrH2; при 1200—1300 °C в вакууме гидриды диссоциируют и весь водород может быть удалён из металла. С азотом цирконий образует при 700—800 °C нитрид ZrN. Цирконий взаимодействует с углеродом при температуре выше 900 °C с образованием карбида ZrC. Карбид и нитрид циркония — твёрдые тугоплавкие соединения; карбид циркония — полупродукт для получения хлорида ZrCl4. Цирконий вступает в реакцию со фтором при обычной температуре, а с хлором, бромом и иодом при температуре выше 200 °C, образуя высшие галогениды ZrHal4 (где Hal — галоген).
Цирконий устойчив в воде и водяных парах до 300 °C, при более высоких температурах (начиная с примерно 700 °C) начинается экзотермическая пароциркониевая реакция
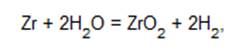
которая имеет важное значение при развитии аварий в ядерных реакторах с водным теплоносителем и/или замедлителем[8, c. 201].
Не реагирует с соляной и серной (до 50 %) кислотами, а также с растворами щелочей (цирконий — единственный металл, стойкий в щелочах, содержащих аммиак). С азотной кислотой и царской водкой он взаимодействует при температуре выше 100 °C. Растворяется в плавиковой и горячей концентрированной (выше 50 %) серной кислотах. Из кислых растворов могут быть выделены соли соответствующих кислот разного состава, зависящего от концентрации кислоты. Так, из концентрированных сернокислых растворов циркония осаждается кристаллогидрат Zr(SO4)2·4H2O; из разбавленных растворов — основные сульфаты общей формулы xZrO2·ySO3·zH2O (где х : y > 1). Сульфаты циркония при 800—900 °C полностью разлагаются с образованием двуокиси циркония. Из азотнокислых растворов кристаллизуется Zr(NO3)4·5H2O или ZrO(NO3)2·xH2O (где x = 2-6), из солянокислых растворов — ZrOCl2·8H2O, который обезвоживается при 180—200 °C.
|
из
5.00
|
Обсуждение в статье: Физико-химические свойства |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

