 |
Главная |
Определяем тепловой эффект для температур 298К и 600К
|
из
5.00
|
Ая часть курсовой работы
РАСЧЕТНО-ГРАФИЧЕСКОЕ ЗАДАНИЕ
по дисциплине "Физика и естествознание. Часть 2"
Термодинамический анализ физико-химической системы
Вариант 13
Студент гр. Э-01:
Шарифулина В. В.
Преподаватель :
к.т.н., доц. Снежко А. А.
Красноярск 2013
Краткие теоретические сведения
Закон Гессадля стандартных условий (температура 298 К и давление 101325 Па):
 (1)
(1)
Для расчетов теплового эффекта реакции при любой температуре (  ) применяют интегральную форму закона Кирхгофа:
) применяют интегральную форму закона Кирхгофа:
 (2)
(2)
Где  - разность сумм теплоемкостей конечных и начальных веществ с их стехиометрическими коэффициентами:
- разность сумм теплоемкостей конечных и начальных веществ с их стехиометрическими коэффициентами:
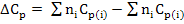 (3)
(3)
кон. нач.
Для проведения точных расчетов надо учитывать зависимости теплоемкости веществ от температуры, например:
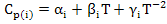 (4)
(4)
Где  – коэффициенты, имеющие определенное численное значение для каждого вещества. В результате осуществления реакции изменение теплоемкости системы:
– коэффициенты, имеющие определенное численное значение для каждого вещества. В результате осуществления реакции изменение теплоемкости системы:
 (5)
(5)
А уравнение закона Кирхгофа приобретает вид:
 (6)
(6)
Изменение энтропии системы, в которой протекает реакция, находя по следующей формуле (для стандартных условий):
 (7)
(7)
кон. нач.
При температуре, отличающейся от стандартной, изменение энтропии рассчитывают по уравнению:
 (8)
(8)
При любой температуре и стандартных давлениях газообразных веществ изменение энергии Гиббса реакции рассчитывают с учетом температурных зависимостей теплового эффекта и энтропии по уравнению Гиббса-Гельмгольца:
 (9)
(9)
А для равновесной температуры находят изменение энергии Гиббса по уравнению:
 (10)
(10)
Константу равновесия для данной температуры вычисляют по величине изменения энергии Гиббса, используя следующее уравнение термодинамики:
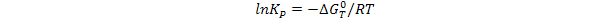 (11)
(11)
Исходные данные
Таблица 1. Химические реакции для термодинамических расчетов
| Номер задания | Уравнение реакции | T, К |
| ZnO + CO = Zn +CO2 |
Таблица 2. Термодинамические свойства веществ
| № п/п | Вещество |  ,
Дж/моль ,
Дж/моль
|  ,
Дж/моль·К ,
Дж/моль·К
| 
| ||

| β | γ | ||||
| ZnO | 43,5 | 48.99 | 5,1·10-3 | -912000 | ||
| CO | 197.4 | 28.41 | 4.1·10-3 | -46000 | ||
| Zn | 41,59 | 22,38 | 10,04·10-3 | |||
| CO2 | 213.6 | 44.14 | 9.04·10-3 | -853000 |
Расчетная часть
Определяем тепловой эффект для температур 298К и 600К.
По уравнению (1) находим:
 (∆H0zn + ∆H0CO2 ) – (∆H0ZnO+∆H0CO)
(∆H0zn + ∆H0CO2 ) – (∆H0ZnO+∆H0CO)
Подставим справочные данные о теплотах образования из таблицы 2:
 0-393500-(-349000-110500) =66000Дж/моль
0-393500-(-349000-110500) =66000Дж/моль
Вывод: так как полученный тепловой эффект – положительная величина, то в результате протекания этой реакции в прямом направлении поглощается теплота.
Выпишем уравнения температурной зависимости теплоемкости реагентов (используя таблицу 2):
СР(ZnO)=48,99+5,1·  T-9,12·
T-9,12· 
CP(CO)=28,41+4,1·  T-0,46·
T-0,46· 
CP(Zn)=22,38+10,04·  T
T
CP(CO2)=44,14+9,04·  T-8,53·
T-8,53· 
Определим изменение теплоемкости системы по уравнению (3):
∆CP=CP(Zn)+CP(CO2)-CP(CO)-СР(ZnO)=(22,38+44,14-48,99-28,41)+(10,04+9,04-4,1-5,1)·  T +(-8,53+0,46+9,12)·
T +(-8,53+0,46+9,12)·  = -10,88+9,88
= -10,88+9,88  T +1,05·
T +1,05·  , Дж/K
, Дж/K
Тепловой эффект реакции при 600К определим, интегрируя уравнение (6) с подстановкой рассчитанной зависимости для  :
:
 =66000+(-6528+3242,24)+(1778,4-438,692)+ +(-175+352,35) = 64231,3 Дж/моль
=66000+(-6528+3242,24)+(1778,4-438,692)+ +(-175+352,35) = 64231,3 Дж/моль
Вывод: изменение энтальпии при 600 К относительно теплового эффекта при стандартных условиях имеет меньшее значение, следовательно при температуре 600 К протекание процесса в прямом направлении сопровождается выделением теплоты.
|
из
5.00
|
Обсуждение в статье: Определяем тепловой эффект для температур 298К и 600К |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

