 |
Главная |
Обработка результатов эксперимента
|
из
5.00
|
Отчёт по лабораторной работе № 1.
| Химия элементов и их соединений |
По дисциплине:
(наименование учебной дисциплины согласно учебному плану)
Тема: Определение эквивалентной массы металла.
Выполнили: студент гр. РГГ-15 ______________ /Мавроммати К.А./
(подпись) (Ф.И.О.)
студент гр. РГГ-15 ______________ /Сабитов И.А./
(подпись) (Ф.И.О.)
ПРОВЕРИЛ:
Руководитель: ______________ /Жадовский И.В./
(подпись) (Ф.И.О.)
Санкт-Петербург
2015 год
Цель работы – усвоить одно из основных химических понятий – понятие об эквиваленте – и научиться определять его количественное значение.
Общие сведения.
Эквивалентной массой вещества называется такое его количество, которое соединяется с одним молем атомов водорода, замещает то же количество атомов водорода в химических реакциях или реагирует без остатка с одним эквивалентом любого другого вещества.
Один из основных законов химии гласит: “Массы веществ, вступивших в реакцию, пропорциональны их химическим эквивалентам”.
При проведении расчетов обычно эквиваленты вычисляют по формуле: , где М- молярная масса вещества, z- число эквивалентов в моле.
, где М- молярная масса вещества, z- число эквивалентов в моле.
Эквивалентным объемом называют объем, занимаемый при данных условиях эквивалентной массой вещества.
Схема экспериментальной установки.
 Схема установки:
Схема установки:
1 – штатив;
2 – чашка с водой;
3 – бюретка;
4 – колба Вюрца;
Порядок выполнения работы:
1) Перед началом опыта проверить сосуд на герметичность.
2) Наполнить водой бюретку и закрепить её в штативе;
3) Закрыв верхнее отверстие бюретки, перевернуть её и опустить в чашу с водой;
4) Вставить присоединенную к боковому отводу колбы резиновую трубку в опущенный в воду конец бюретки;
5) В колбу Вюрца налить 10 мл серной кислоты и вытереть насухо горло колбы фильтром;
6) Расположив колбу горизонтально, поместить в её горло навеску металла, закрыть колбу пробкой;
7) Отметить уровень жидкости в бюретке;
8) Перевернув колбу в вертикальное положение, сбросить навеску металла в кислоту;
9) Когда выделится весь водород, ещё раз отметить уровень воды;
10) Миллиметровой линейкой измерить высоту столба воды в бюретке над уровнем воды в чашке.
11) По показаниям барометра и термометра определить атмосферное давление и температуру в лаборатории.
Порядок вычислений.
1) записать атмосферное давление и температуру в лаборатории;
2) записать массу навески металла;
3) рассчитать давление водорода в бюретке:
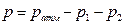 , где
, где 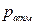 - атмосферное давление в лаборатории, Па;
- атмосферное давление в лаборатории, Па;  - давление столба воды в бюретке, Па;
- давление столба воды в бюретке, Па; 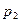 - давление насыщенного водяного пара, Па ( находим его по таблице);
- давление насыщенного водяного пара, Па ( находим его по таблице);
4) вычислить массу выделившегося водорода: 
 , где:
, где:  - молярная масса водорода;
- молярная масса водорода; 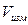 - объем водорода,
- объем водорода, 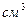 ;
; 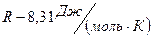 - универсальная газовая постоянная. Найти эквивалент металла по закону эквивалентов:
- универсальная газовая постоянная. Найти эквивалент металла по закону эквивалентов: 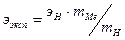 , где
, где  =1- эквивалент водорода. По заданной степени окисления металла определить его молекулярную массу и провести его идентификацию.
=1- эквивалент водорода. По заданной степени окисления металла определить его молекулярную массу и провести его идентификацию.
5) Вычислить точное значение эквивалента металла: 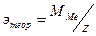 , где z- степень окисления металла,
, где z- степень окисления металла, 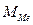 - молярная масса металла(по таблице Д.И. Менделеева);
- молярная масса металла(по таблице Д.И. Менделеева);
6) Определить относительную погрешность вычисления:  .
.
Обработка результатов эксперимента.
Pатм=750мм.рт.ст.
t=23°C
mМе=0,0107г.
h=172мм.
Vизм=10.6мл.
Pатм=750/760*101325=99991,77Па.
P1=9,8*h*daq=9,8*172*1=1685,6
| T, K | ||||||
 , Па , Па
| 1226,4 | 1706,2 | 2332,7 | 3172,5 | 4328,9 | 5625,3 |

Т=296К;
 Т= 298К-293К= 5К;
Т= 298К-293К= 5К;
 p= 3172,5-2332,7= 859,8 Па;
p= 3172,5-2332,7= 859,8 Па;
839,8:5=167,96;
p2=2836,58Па;

p= 95469,59Па;
mH=(MH*p*Vизм*10-6)/RT;
mH=2*95469,39*10,6*10-6/8,314*296=0,0008г.
Эм(Ме)=1*0,0107/0,0008=13,375г/экв.
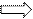 М(Ме)= Эм(Ме)*z=13,375*2=26,75г/моль. Mg = магний
М(Ме)= Эм(Ме)*z=13,375*2=26,75г/моль. Mg = магний
 ∆=│13,375 – 12,155│ 12,155*100%=10%
∆=│13,375 – 12,155│ 12,155*100%=10%
Вывод:с помощью данной лабораторной работымы усвоили понятие эквивалента и научились определять его количественное значение.
|
из
5.00
|
Обсуждение в статье: Обработка результатов эксперимента |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

