 |
Главная |
А. Определить тип оксида и написать формулу соответствующего гидроксида
|
из
5.00
|
- Если оксид образован металлом, то в зависимости от степени окисления тип оксида может быть: основным, амфотерным или кислотным
Основные оксиды образуют металлы со степенями окисления +1, +2: кроме BeO, ZnO, SnO, PbO. Таким оксидам соответствуют гидроксиды – основания, в которых число групп OH равно степени окисления металла.
Например, 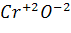 – оксид хрома (II), основный оксид
– оксид хрома (II), основный оксид
и соответствующий гидроксид – основание: 
Амфотерные оксиды образуют металлы со степенями окисления +3, +4, а также BeO, ZnO, SnO, PbO. Таким оксидам соответствуют амфотерные гидроксиды, т.е. и основания и кислородсодержащие кислоты.
Например, а) ZnO – оксид цинка, амфотерный
и соответствующий гидроксид ---- амфотерный: 
б) 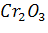 - оксид хрома (III), амфотерный
- оксид хрома (III), амфотерный
и гидроксид амфотерный: 
ортохромистая кислота, но чаще существуют метакислоты
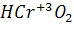 метахромистая кислота
метахромистая кислота
Кислотные оксиды образуют металлы со степенями окисления +5, +6, +7, +8. Таким оксидам соответствуют кислотные гидроксиды, т.е. кислородсодержащие кислоты, формулу которой можно получить, прибавив к оксиду воду.
Например,  – оксид хрома (VI), кислотный
– оксид хрома (VI), кислотный
И соответствующий гидроксид --- кислота: 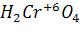 хромовая кислота
хромовая кислота
- Если оксид образован неметаллом, то он может быть или несолеобразующим (это N2O, NO, CO,SO,SiO) или кислотным.
Несолеобразующим оксидам не соответствуют ни основания, ни кислоты.
Кислотным оксидам соответствуют кислотные гидроксиды, т.е. кислородсодержащие кислоты.
Например,  оксид хлора (I), кислотный, т.к. образован неметаллом
оксид хлора (I), кислотный, т.к. образован неметаллом
И соответствующий гидроксид – кислота: ( 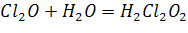 все индексы делим на 2, получаем
все индексы делим на 2, получаем  ).
).
Пример задания 3а.
Даны оксиды: MnO, Mn2O3, Mn2O7, P2O3, Cl2O5, SiO2, SnO, PbO2.
Указать тип и написать формулу гидроксида.
Решение.
а) 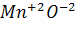 – оксид образован металлом, степень окисления которого +2, оксида в исключениях нет, → оксид основный.
– оксид образован металлом, степень окисления которого +2, оксида в исключениях нет, → оксид основный.
Гидроксид: основание – 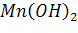
б) 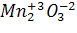 - оксид металла со ст. окисления +3, → оксид амфотерный.
- оксид металла со ст. окисления +3, → оксид амфотерный.
Гидроксид амфотерный : 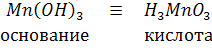
в) 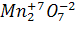 – оксид металла со ст. ок-ия +7 → оксид кислотный,
– оксид металла со ст. ок-ия +7 → оксид кислотный,
гидроксид – кислота: (  делим на 2, получаем
делим на 2, получаем 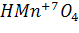 ).
).
г)  – оксид образован неметаллом, в несолеобразующих нет, → оксид кислотный.
– оксид образован неметаллом, в несолеобразующих нет, → оксид кислотный.
Гидроксид – кислота:  делим индексы на 2, получаем HPO2 , но для фосфора, мышьяка и некоторых других элементов чаще применяются ортокислоты:
делим индексы на 2, получаем HPO2 , но для фосфора, мышьяка и некоторых других элементов чаще применяются ортокислоты:
HPO2 + H2O = H3PO4
метафосфористая ортофосфористая
кислота кислота
д) 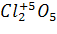 – оксид образован неметаллом, в несолеобразующих нет → оксид кислотный. Гидроксид - кислота: (
– оксид образован неметаллом, в несолеобразующих нет → оксид кислотный. Гидроксид - кислота: (  или
или 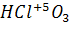 ).
).
е) 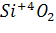 – оксид образован неметаллом, в несолеобразующих нет, → оксид кислотный. Гидроксид – кислота: (
– оксид образован неметаллом, в несолеобразующих нет, → оксид кислотный. Гидроксид – кислота: (  .
.
ж) 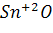 – оксид образован металлом со ст. ок-ия +2, есть в исключениях, → оксид амфотерный и гидроксид амфотерный:
– оксид образован металлом со ст. ок-ия +2, есть в исключениях, → оксид амфотерный и гидроксид амфотерный: 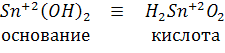 .
.
з)  – оксид образован металлом со ст. ок-ия +4, → оксид амфотерный.
– оксид образован металлом со ст. ок-ия +4, → оксид амфотерный.
Гидроксид -- амфотерный:
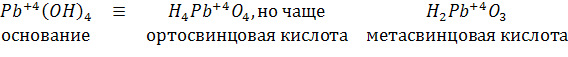
3б. Указать, какие кислоты образуют кислые соли и составить формулы солее:
а) HClO; б)H2Se; в) HNO3; г) H2CO3; д) H3AsO4.
Решение.
Кислые соли образуют многоосновные кислоты (это те, в состав которых входят 2 или больше атомов Н) при частичном замещении атомов Н в кислоте на катион металла.
а) HClO: одноосновная кислота, не может образовать кислых солей
б) H2Se: двухосновная кислота,частично может заместить 1 атом H → 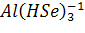
в) HNO3: одноосновная кислота, не может образовать кислых солей
г) H2CO3: двухосновная кислота,частично может заместить 1 атом H → Ca(HCO3)2
д) H3AsO4: трехосновная кислота частично может заместить 1 или 2 атома H:
1 атом H → Fe3+(H2AsO4)3 -1 или Fe(H2AsO4)3
2 атома H → 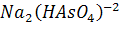 или Na2(HAsO4).
или Na2(HAsO4).
|
из
5.00
|
Обсуждение в статье: А. Определить тип оксида и написать формулу соответствующего гидроксида |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

