 |
Главная |
А концентрация ацетата натрия – по формуле
|
из
5.00
|
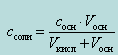
Например, при добавлении 9,0 мл 0,1 М NaOH
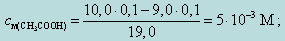


Значение рН в начале скачка на кривой титрования (добавлено 9,99 мл 0,1 М NaOH) рассчитывается по формуле

Таблица 13.1.1
Расчет кривой титрования 10,0 мл 0,1 М СH3COOH раствором 0,1 М NaOH
| № | V(NaOH),мл | 
| 
| 
| [OH-],моль/л | pH |
| 1. | 0,00 | 0,10 | - | - | - | 2,88 |
| 2. | 2,50 | 0,06 | 0,020 | 3,000 | - | 4,28 |
| 3. | 5,00 | 0,03 | 0,030 | 1,000 | - | 4,76 |
| 4. | 9,00 | 5 · 10 -3 | 0,047 | 0,100 | - | 5,76 |
| 5. | 9,90 | 5 · 10 -4 | 0,050 | 0,010 | - | 6,76 |
| 6. | 9,99 | 5 · 10 -5 | 0,050 | 0,001 | - | 7,76 |
| 7. | 10,00 | - | 0,050 | - | - | 8,76 |
| 8. | 10,01 | - | 0,050 | - | 5 ·10 - 5 | 9,7 |
| 9. | 10,10 | - | 0,050 | - | 5 ·10 - 4 | 10,7 |
| 10. | 11,00 | - | 0,047 | - | 5 ·10 - 3 | 11,7 |
| 11. | 15,00 | - | 0,040 | - | 0,02 | 12,3 |
В общем случае рН в начале скачка на кривой титрования слабой одноосновной кислоты можно вычислить по формуле
pH = pK + 3
Эта формула получается с учетом того факта, что логарифм отношения количества неоттитрованной кислоты (0,1 %) к количеству полученной соли (99,9 %) в данном случае 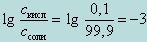
В точке эквивалентности (добавлено 10,0 мл 0,1 М NaOH) рН рассчитывается для гидролизующейся соли CH3COONa по формуле

За точкой эквивалентности расчет рН ведется аналогичным образом, как и в случае титрования сильной кислоты щелочью. Внешний вид кривой титрования приведен на рис.13.1.1.
Анализ кривой титрования
Характерной особенностью кривых титрования слабых одноосновных кислот является несовпадение точки эквивалентности с точкой нейтральности и расположение точки эквивалентности в щелочной области. Величина скачка на кривой титрования значительно меньше, чем в случае титрования сильной кислоты щелочью. Так, в данном случае рН = рН конца скачка - рН начала скачка = 9,7 - 7,76 = 1,94 вместо 5,4 единиц при титровании 0,1 М HCl раствором 0,1 М NaOH. В данном случае в качестве индикатора можно использовать только фенолфталеин, метиловый оранжевый применять нельзя.
Величина скачка уменьшается с уменьшением концентрации кислоты, с возрастанием температуры, с уменьшением константы диссоциации слабой кислоты. При Kкисл < 10 - 6 скачок исчезает вообще.

Рис.13.1.1. Кривая титрования 10 мл 0,1 М CH3COOH раствором 0,1 М NaOH
Кривая титрования слабого основания сильной кислотой/strong>
При построении кривой титрования слабого основания сильной кислотой исходят из тех же соображений, что и в случае титрования слабой кислоты щелочью. В первоначальный момент рН раствора определяется диссоциацией слабого основания. До точки эквивалентности в растворе будет присутствовать буферная смесь, состоящая из неоттитрованного слабого основания и его соли. В точке эквивалентности находится только соль слабого основания и сильной кислоты, которая подвергается гидролизу и создает кислую среду. За точкой эквивалентности рН определяется избыточным содержанием в растворе сильной кислоты.
Пример.
Построить кривую титрования 10,0 мл 0,1 М NH4OH раствором 0,1 М HCl.
Решение.
Расчетные данные приведены в табл. 13.2.1.
В первоначальный момент (кислота не добавлена) рН раствора определяется по формуле

Таблица 13.2.1
Расчет кривой титрования 10,0 мл 0,1 М NH4OH раствором 0,1 М HCl
| № | V(HCl),мл | 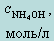
| 
| 
| [H+],моль/л | pH |
| 1. | 2,50 | 0,06 | 0,020 | 3,000 | - | 11,12 |
| 2. | 0,00 | 0,10 | - | - | - | 9,72 |
| 3. | 5,00 | 0,03 | 0,030 | 1,000 | - | 9,24 |
| 4. | 0,00 | 5 · 10 - 3 | 0,047 | 0,100 | - | 8,24 |
| 5. | 9,90 | 5 · 10 - 4 | 0,050 | 0,010 | - | 7,24 |
| 6. | 9,99 | 5 · 10 - 5 | 0,050 | 0,001 | - | 6,24 |
| 7. | 10,00 | - | 0,050 | - | - | 5,27 |
| 8. | 10,01 | - | 0,050 | - | 5 · 10- 5 | 4,30 |
| 8. | 10,01 | - | 0,050 | - | 5 · 10- 5 | 4,30 |
| 9. | 10,10 | - | 0,050 | - | 5 · 10- 4 | 3,30 |
| 10. | 11,00 | - | 0,047 | - | 5 · 10- 3 | 2,30 |
| 11. | 15,00 | - | 0,040 | - | 0,02 | 1,70 |
При добавлении 9,0 мл 0,1 М HCl концентрация неоттитрованного слабого основания и его соли рассчитывается следующим образом:

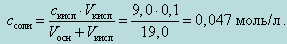
|
из
5.00
|
Обсуждение в статье: А концентрация ацетата натрия – по формуле |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

