 |
Главная |
Характерные степени окисления
|
из
5.00
|
V группа, главная подгруппа.
| Общая электронная формула | ns2np3 |
| Азот, фосфор, мышьяк - | неметаллы |
| Электроотрицательности: | N - 3 P - 2,2 As - 2,1 |
| Наиболее характерные степени окисления: | +5, +3, 0, -3. |
| Оксиды Э2O5 и Э2O3 | Кислотные оксиды. |
| Водородное соединение: | ЭН3 |
Азот.
Простое вещество.
| :NºN: В молекуле имеются одна s- и две p- связи. | Свойства: 1) из-за тройной связи очень мало активен. При обычных условиях с кислородом не реагирует. Реагирует с кислородом только при высокой температуре, электрическая дуга, 30000С: N20 + O2 ⇄ 2N+2O (в природе - во время грозы); 2) Реагирует с металлами: литием при комнатной температуре, кальцием и магнием при нагревании: N2 + 6Li = 2Li3N – нитрИД лития. N2 + 3Ca -t→ Ca3N2 3)с водородом – при высоком давлении и в присутствии катализатора: N2 + ЗН2-(t,p,кат)→ 2NH3 |
| Получение: NH4NO2 -t→ N2 + 2H2O (разложение нитрита аммония) 4NH3 + 3O2 = 2N2 + 6H2O (горение аммиака). |
Соединения азота(‑3)
1. Нитриды металлов: твёрдые, легко гидролизующиеся вещества.
| Получение: N2 + 6Li = 2Li3N | Свойства: гидролизуются водой и кислотой. Ca3N2 + 6H2O =3Са(OH)2 +2NH3 Li3N + 4HCl = 3LiCl + NH4Cl |
Аммиак NH3:
Бесцветный газ с резким запахом.
Аммиак очень хорошо растворим в воде, что объясняется образованием каждой молекулой аммиака четырех водородных связей с молекулами воды.


Способы собирания газов:
А) Вытеснением воздуха для газов легче воздуха;
Б) Вытеснением воды
В) Вытеснением воздуха для газов тяжелее воздуха.

Аммиак можно собирать только по методу (А), т.к. он легче воздуха и хорошо растворим в воде.
Получение аммиака:
В промышленности:
N2 + 3Н2 (t, p, кат) ⇄ 2NH3
В лаборатории:
а) вытеснение щелочами из солей аммония:
2NH4Cl + Са(OH)2 -t→ CaCl2 + 2NH3 + 2Н2O
б) гидролиз нитридов: Ca3N2 + 6H2O = ЗСа(OH)2 + 2NH3
Свойства аммиака:
| 1.Молекула аммиака – частица-основание. Принимая протон она превращается в ион аммония. Реакция может протекать как в водном растворе, так и в газовой фазе: | 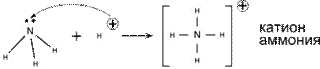 :NH3 + H2O ⇄ NH4+ + OH- (в растворе);
:NH3 + H+ = NH4+ (в растворе);
:NH3(г) + HCl(г) = NH4Cl(кр) (в газ. фазе).
:NH3 + H2O ⇄ NH4+ + OH- (в растворе);
:NH3 + H+ = NH4+ (в растворе);
:NH3(г) + HCl(г) = NH4Cl(кр) (в газ. фазе).
|
| 2.Реагирует с кислотами, образуя СОЛИ АММОНИЯ: | NH3 + H2SO4 = NH4HSO4 – гидросульфат аммония 2NH3 + H2SO4 = (NH4)2SO4 – сульфат аммония. |
| 3. Реагирует с солями тяжелых металлов, образуя нерастворимые гидроксиды: | FeSO4 + NH3 + H2O = Fe(OH)2 + (NH4)2SO4 |
| 4. Соли и гидроксиды меди, никеля, серебра растворяются в избытке аммиака, образуя комплексные соединения – амминокомплексы: | 4NH3 + CuSO4 = [Cu(NH3)4]SO4 2NH3 • H2O + AgCl = [Ag(NH3)2]Cl + 2H2O 4NH3•H2O+Ag2O =2[Ag(NH3)2]OH+3H2O |
| 5. Аммиак горит на воздухе, образуя азот и воду. Если реакцию проводить в присутствии катализатора (Pt), то образуется NO: | 4NH3 + 3O2 = 2N2 + 6H2O (горение аммиака), 4NH3 + 5O2 = 4NO + 6H2O (каталитическое окисление). |
| 6. Аммиак способен восстанавливать не очень активные металлы из их оксидов: | 3CuO + 2NH3 = 3Cu + N2 + 3H2O |
СОЛИ АММОНИЯ
Получение:
Аммиак (или гидроксид аммония) + кислота à
NH3 + HNO3 ® NH4NO3(нитрат аммония)
2NH4OH + H2SO4 ® (NH4)2SO4(cульфат аммония) + 2Н2O
Химические свойства.
| 1. Сильные электролиты (диссоциация) | NH4Cl ⇄ NH4+ + Cl- |
| 2. Разложение при нагревании. a) если кислота летучая b) если анион проявляет окислительные свойства | а)NH4Cl ⇄NH3 + HCl NH4HCO3 ® NH3 + Н2O + CO2 b) NH4NO3 –t°® N2O + 2Н2O NH4NO2 –t°® N2 + 2Н2O (NH4)2Cr2O7 –t°® N2 + Cr2O3 + 4Н2O |
| 3. Реакции обмена с кислотами, основаниями и другими солями (если выделяется осадок, газ. | a) (NH4)2CO3 +2НCl ®2NH4Cl + Н2O + CO2↑ CO32- + 2H+ ® Н2O + CO2 b) (NH4)2SO4+Ba(NO3)2®BaSO4¯ +2NH4NO3 Ba2+ + SO42- ® BaSO4¯ с) NH4NO3 + KOH à KNO3 + NH3↑ + H2O NH4+ + OH ¯ à NH3↑ + H2O |
| 4.Соли аммония подвергаются гидролизу (как соль слабого основания и сильной кислоты) – среда кислая: | NH4Cl + Н2O ⇄ NH4OH + HCl NH4+ + Н2O ⇄ NH4OH + H+ |
ОКСИДЫ АЗОТА
| N2+1O ОКСИД АЗОТА (I) ЗАКИСЬ АЗОТА, "ВЕСЕЛЯЩИЙ ГАЗ" | N+2O ОКСИД АЗОТА (II) ОКИСЬ АЗОТА | N2+3O3 ОКСИД АЗОТА (III) АЗОТИСТЫЙ АНГИДРИД | N+4O2 ОКСИД АЗОТА (IV), ДИОКСИД АЗОТА, «ЛИСИЙ ХВОСТ» | N2+5O5 ОКСИД АЗОТА (V) АЗОТНЫЙ АНГИДРИД |
| бесцветный | бесцветный | темно-синяя жидкость (при низких температурах). | бурый газ | крист. вещество |
| несолеобра-зующий | несолеобра-зующий | кислотный | кислотный* (даёт 2 кислоты) | кислотный |
N2O – Несолеобразующий оксид.
| Получение: NH4NO3 –t°® N2O + 2Н2O | Химические свойства: 1. Разлагается при 700°C с выделением кислорода: 2N2O –t°® 2N20 + O20 2. Окислитель, поддерживает горение, как кислород. С водородом: N2O + H2 ® N2 + Н2O, с углеродом: N2O + C à N2 + CO |
NO- Несолеобразующий
| Получение: 1. Каталитическое окисление аммиака (промышленный способ) 4NH3 +5O2 ® 4NO + 6H2O 2. 3Cu + 8HNO3(разб.)®3Cu(NO3)2 +2NO+4H2O 3. N2 + O2 ® 2NO (в природе, во время грозы) | Химические свойства: 1. Легко окисляется кислородом и галогенами 2NO + O2 ® 2NO2 2NO + Cl2 ® 2NOCl (хлористый нитрозил) 2.Окислитель 2NO + 2SO2 ® 2SO3 + N20 |
N2O3 - азотистый ангидрид – кислотный оксид.
| Получение: NO2 + NO ⇄ N2O3 (при охлаждении) | Химические свойства: 1)Выше t°кип. разлагается на NO и NO2 2)N2O3 + 2NaOH ® 2NaNO2(нитрит натрия) + H2O 3) N2O3 + H2O ® 2НNO2(азотистая кислота) |
NO2 -бурый газ, ядовит.
Получение:1. 2NO + O2 ® 2NO2
2. Cu + 4HNO3(конц.) ® Cu(NO3)2 + 2NO2 + 2H2O
Химические свойства
| 1. Кислотный оксид, образует две кислоты сразу: | А)с водой: 2NO2 + H2O ® HNO3 + HNO2 4NO2 + 2H2O + O2 ® 4HNO3 Б) со щелочами: 2NO2 +2NaOH ®NaNO2+NaNO3 +H2O |
| 2. Окислитель: | N+4O2 + S+4O2 ® S+6O3 + N+2O |
| 3. Димеризация: | 2NO2(бурый газ)⇄ N2O4(бесцветная жидкость) – димер. |
N2O5 - азотный ангидрид
| Получение: 1. Окисление диоксида азота: 2NO2 + O3®N2O5 + O2 2. Обезвоживание азотной кислоты: 2HNO3 +P2O5 ® 2HPO3 + N2O5 | Химические свойства: 1. Кислотный оксид: a) С водой: N2O5 + H2O ® 2 HNO3 b) С основаниями: N2O5 + КОН = KNO3 + H2O c) С оксидами металлов: N2O5 + CaO = Ca(NO3)2 2. Сильный окислитель: 2N2O5 +S ® SO2 +4NO2 3. Легко разлагается (при нагревании - со взрывом): 2N2O5 ® 4NO2 + O2 |
АЗОТИСТАЯ КИСЛОТА HNO2
Получение: Вытеснение из нитритов сильной кислотой:
AgNO2 + HCl ® HNO2 + AgCl¯
Химические свойства:
1. Слабая неустойчивая кислота; ее соли (нитриты) – устойчивы:
HNO2 + NaOH ® NaNO2 + H2O
2. Разлагается при нагревании: 3HNO2 ® HNO3 + 2NO + H2O
3. Слабый окислитель (окислительные свойства проявляет только в реакциях с сильными восстановителями)
2KNO2 + 2KI + 2H2SO4 ® 2K2SO4 + I2 + 2NO + 2H2O
4. Сильный восстановитель: HNO2 + Cl2 + H2O ® HNO3 + 2HCl
АЗОТНАЯ КИСЛОТА HNO3
Получение:
| 1. Лабораторный способ | KNO3 + H2SO4(конц) –t°® KHSO4 + HNO3 |
| 2. Промышленный способ. Осуществляется в три этапа: | |
| a) Окисление аммиака на платиновом катализаторе до NO: | 4NH3 + 5O2 –500°,Pt® 4NO + 6H2O |
| b) Окисление кислородом воздуха NO до NO2 | 2NO + O2 ® 2NO2 |
| c) Поглощение NO2 водой в присутствии избытка кислорода | 4NO2 + О2 + 2H2O ⇄ 4HNO3 |
ХИМИЧЕСКИЕ СВОЙСТВА:
| 1. Очень сильная кислота. Диссоциирует в водном растворе практически нацело: | HNO3 ⇄ H+ + NO3- |
| 2. Реагирует с основными оксидами | CuO + 2HNO3 ® Cu(NO3)2 + H2O или CuO + 2H+ ® Cu2+ + H2O |
| 3. Реагирует с с основаниями | HNO3 + NaOH ® NaNO3 + H2O или H+ + OH- ® H2O |
| 4. Вытесняет слабые кислоты из их солей | 2HNO3 + Na2CO3 ®2NaNO3 + H2O+CO2 2H+ + СO32- ® H2O + CO2 |
| СПЕЦИФИЧЕСКИЕ СВОЙСТВА АЗОТНОЙ КИСЛОТЫ | |
| 1. Разлагается на свету и при нагревании | 4HNO3 –t°,hn® 2H2O + 4NO2 + O2 |
| 2. Окрашивает белки в оранжево-желтый цвет (при попадании на кожу рук - "ксантопротеиновая реакция") | |
| 3. При взаимодействии с металлами никогда не выделяется водород! | металл + HNO3 à соль азотной кислоты + вода + газ (или соль аммония) |
| 4. С неметаллами: Азотная кислота превращается в NO (или в NO2); неметаллы окисляются до соответствующих высших кислот: | S+ 6HNO3(конц) ® H2SO4 + 6NO2 + 2H2O B + 3HNO3 ® H3BO3 + 3NO2 3P + 5HNO3 + 2H2O ® 5NO + 3H3PO4 |
| HNO3 | ||||
| концентрированная | разбавленная | |||
| ¯ | ¯ | ¯ | ¯ | ¯ |
| Fe, Al, Cr- пассивирует (без нагревания) Au, Pt – не реагирует. | с тяжелыми металлами NO2 | со щелочными и щел.зем. металлами N2O | с тяжелыми металлами NO | со щелочными и щел.зем. металлами, а также Sn и Fe N2(cред. разб) NH4NO3(оч.разб) |
РАЗЛОЖЕНИЕ НИТРАТОВ
| 1. Металлы левее магния кроме лития. | KNO3 –tà КNO2 + O2 нитрит металла + кислород |
| 2. От магния до меди + литий | Mg(NO3) 2–tà MgO + NO2 + O2 оксид металла + NO2 + O2 |
| 3. После меди | AgNO3 –tàAg + NO2 + O2 металл + NO2 + O2 |
| 4. Нитрат аммония и нитрит аммония | NH4NO3 –tà N2O + 2H2O NH4NO2 –tà N2 + 2H2O |
ФОСФОР.
Электронная конфигурация Р 1S22S22P63S23P3
S 2s 2p 3s 3p 3d
| ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑ | ↑ | ↑ |

образование возбужденного состояния.
Возможные валентности: -в невозбужденном состоянии: III
- в возбужденном состоянии: V
Характерные степени окисления.
| +5 | +3 | +1 | -3 |
| Оксид: P2O5 Кислоты: HPO3 (метафосфорная кислота) H4P2O7 (пирофосфорная кислота) H3PO4 (ортофосфорная кислота) Соли: фосфаты Ca3(PO4)2 Гидрофосфаты К2НРО4 Дигидрофосфаты КН2РО4 Галогенангидриды:PОCl3,PCl5 | Оксид: P2O3 Кислота: H3PO3 - двухосновная фосфористая Соли: фосфиты Na2HPO3 Галогенангидрид: PCl3 | Кислота: H3PO3 - одноосновная фосфорноватистая Соль: гипофосфит NaH2PO2 | Фосфиды металлов: Ca3P2 Водородное соединение: фосфин PH3 |
|
из
5.00
|
Обсуждение в статье: Характерные степени окисления |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

