 |
Главная |
Химическая кинетика и катализ
|
из
5.00
|
21.1.Выражение закона действующих масс для скорости элементарной гомогенной реакции аА + вВ = сС имеет вид
 ; u = k∙[C]c; u = k∙[A]∙[B]; u = k∙[A]a∙[B]b;
; u = k∙[C]c; u = k∙[A]∙[B]; u = k∙[A]a∙[B]b;
21.2. Если температурный коэффициент скорости равен 2, то при увеличении температуры от 120°С до 170°С скорость химической реакции _______раз(а).
Уменьшится в 32; уменьшится в 10; увеличится в 32; увеличится в 10.
21.3. Увеличение скорости химической реакции при введении катализатора происходит в результате …
Уменьшения энергии активации; уменьшения энтальпии реакции; увеличения энергии Гиббса; увеличения энергии активации.
21.4. Для увеличения скорости элементарной гомогенной реакции
2NO + Cl2 = 2NOCl в 64 раза необходимо увеличить давление в ___ раз(а).
32; 4; 16; 8.
21.5. При увеличении давления в реакционной смеси в 2 раза скорость элементарной гомогенной реакции 2NO + Cl2 = 2NOCl _____ раз.
Увеличится в 6; увеличится в 8; уменьшится в 8; уменьшится в 6.
21.6. Если температурный коэффициент скорости равен γ, то при увеличении температуры на 30°С скорость химической реакции __________ раз.
Уменьшится в g3; увеличится в g3; уменьшится в 3g; увеличится в 3g.
21.7. Выражение закона действующих масс для скорости элементарной гомогенной реакции 2A(г) + B(г) = A2B(г) имеет вид …
r = k∙[A]2∙[B]; 
r = k∙[A]∙[B]; r = k∙[A3B].
21.8. Выражение закона действующих масс для скорости прямой реакции
Fe2O3(т) + 3CO(г) = 2Fe(т) + 3CO2(г) при условии ее элементарности имеет вид …
u = k∙[CO]3; u = k∙[Fe2O3]∙[CO]3;
u = k∙[Fe]2∙[CO2]3; u = k∙[CO2]3;
21.8. Единицей измерения скорости гомогенной химической реакции является …
Моль∙с∙л-1; л∙с∙моль-1; моль2∙л-2∙c-1; моль∙л-1∙c-1.
Химическое равновесие
22.1.Уравнение реакции, в которой при изменении давления не происходит смещения равновесия, имеет вид …
C(графит) + 2H2O(g) ↔ 2H2(g) + CO2(g);
FeO(кр) + C(графит) ↔ Fe(кр) + CO(g);
Fe2O3(кр) + 3CO(g) ↔ 2Fe(кр) + 3CO2(g);
C(графит) + 2CO2(g) ↔ CO(g).
22.2.Согласно принципу Ле Шателье, понижение температуры вызывает смещение равновесия в системе в сторону …
Уменьшения объема; увеличения объема;
экзотермической реакции; эндотермической реакции.
22.3. Величина, значение которой количественно характеризует состояние химического равновесия при заданных условиях, называется …
Энергией активации; константой Больцмана;
внутренней энергией; константой равновесия.
22.4. Для увеличения выхода продуктов реакции в равновесной системе
C(графит) + 2H2O(г) ↔ 2H2(г) + CO2(г); DrH0 > 0;необходимо …
Увеличить концентрацию оксида углерода (IV); ввести катализатор;
повысить температуру; повысить давление.
22.5. Уравнение константы равновесия гетерогенной химической реакции MgCO3(т) ↔ MgO(т) + CO2(г) имеет вид …
K = [CO2];  ;
;  ;
; 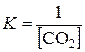
22.6.Уравнение константы равновесия гетерогенной химической реакции PCl5(ж)  PCl3(ж) + Cl2(г) имеет вид …
PCl3(ж) + Cl2(г) имеет вид …
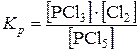 ; Kp = [Cl2];
; Kp = [Cl2]; 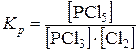 ;
; 
22.6. Если в колонне синтеза аммиака при 450 0С установилось равновесие
N2(г) + 3H2(г) ↔ 2NH3(г), ΔrH < 0, то для увеличения выхода продукта необходимо …
Уменьшить концентрацию азота; уменьшить давление;
увеличить давление; увеличить температуру.
22.7. Влияние изменений, которые происходят в равновесной химической системе под влиянием внешних воздействий, определяется …
Принципом Ле Шателье; принципом квазистационарности;
правилом фаз Гиббса; правилом Вант-Гоффа.
|
из
5.00
|
Обсуждение в статье: Химическая кинетика и катализ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

