 |
Главная |
Диазо- и азосоединения
|
из
5.00
|
Ароматические диазосоединения. Реакция диазотирования. Строение, кислотно-основные свойства и таутомерия диазосоединений.
Реакции с выделением азота: замещение диазогруппы на водород, гидроксил, галогены, цианогруппу, металлы. Реакции без выделения азота: образование фенилгидразина, сочетание с ароматическими аминами и фенолами.
Азосоединения. Понятие об амино- и гидроксиазокрасителях. Связь между строением и цветностью. Современные представления о хромофоре. Роль системы сопряжения и ауксохромов. Метилоранж и его индикаторные свойства.
Методические указания
Ароматические диазосоединения по своему строению делятся на:
1. Собственно диазосоединения соответствующие формуле Ar – N = N –X, где Х – остаток минеральной кислоты или группа ОН;
2. Соли диазония, которые построены аналогично солям ммония [Ar – N ≡ N]+Х–. Эти две группы соединений тесно связаны между собой, между ними возможны таутомерные превращения. Соли диазония, имеющие наибольшее практическое применение получают реакцией диазотирования– взаимодействием первичных ароматических аминов с азотистой кислотой в присутствии избытка минеральной кислоты при охлаждении.
Все превращения солей диазония можно разделить на два типа: 1) реакции с выделением азота, которые используются для получения различных ароматических соединений из ариламинов; 2) реакции без выделения азота. Основной реакцией второго типа является реакция азосочетания, которая используется для получения азокрасителей. Азокрасители, изменяющие свой цвет от реакции среды, применяются в качестве индикаторов.
Вопросы для самопроверки
1. Напишите уравнение реакции диазотирования n-толуидина в солянокислой среде. Назовите полученную соль диазония.
2. Из анилина получите бромбензол, фенол, бензонитрил, этилфеноловый эфир.
3. Напишите уравнение реакции азосочетания хлористого 4-сульфофенилдиазония с диметиланилином. Какое строение имеет полученное соединение в кислой и щелочной среде?
Оксокислоты, гидроксикислоты, оптическая изомерия
Альдегидо- и кетокислоты. Общие методы получения. Пировиноградная и ацетоуксусная кислоты. Кето-енольная таутомерия ацетоуксусного эфира.
Классификация гидроксикислот (спирто- и фенолокислоты).
Алифатические гидроксикислоты. Классификация, изомерия, номенклатура. Получение гидроксикислот: гидролизом галогенозамещенных кислот, из оксинитрилов и по реакции Реформатского. Физические и химические свойства. Особенности a-, b- и g-гидроксикислот.
Оптическая активность органических соединений. Удельное вращение. Асимметрический атом углерода. Оптические антиподы (энаптиомеры), рацематы. Зависисимость числа оптических изомеров от числа асимметрических атомов углерода в молекуле. Диастереоизомеры.
Молочная, яблочная и винные кислоты. Стереоизомерия этих кислот. Замещение у асимметрического атома углерода. Методы разделения рацематов на оптически активные компоненты. Лимонная и изолимонная кислоты.
Ароматические гидроксикислоты. Салициловая кислота, синтез ее из фенола (Кольбе — Шмидт). Салицилат натрия, ацетилсалициловая кислота, салол. Галловая кислота. Танины. Дубители.
Методические указания
Альдегидо- и кетокислоты – глиоксиловая, пировиноградная, щавелево-уксусная α-кетоглутаровая и другие кислоты являются продуктами взаимного обмена углеводов, жиров и белков. Например, пировиноградная кислота является главным конечным продуктом процесса гликолиза при катаболизме углеводов; окислительное дезаминирование аминокислот приводит к образованию α-кетокислот; глиоксиловая и щавелево-уксусная (ЩУК) кислоты являются главными участниками глиоксилатного цикла и цикла трикарбоновых кислот (ЦТК).
При изучении альдегидо- и кетокислот следует рассмотреть кето-енольную таутомерию ацетоуксусного эфира.
Гидроксикислоты разделяют на спирто- и фенолокислоты, а также на α-, β- и γ-оксикислоты. При их изучении следует рассмотреть реакции по карбоксильной и гидроксильной группам, а затем изучить свойства обусловленные их взаимным влиянием.
На примере гидроксикислот мы знакомимся с явлением оптической изомерии, которая является одним из видов пространственной изомерии (стереоизомерии) и обусловлена взаимодействием света с веществом. Оптической активностью, т.е. способностью вращать плоскость поляризации плоско-поляризованного света обладают вещества, в молекулах которых содержится асимметрический атом углерода – атом, связанный с четырьмя различными заместителями.
Представителем таких соединений является молочная кислота:
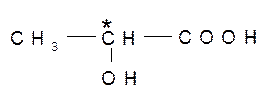
В таких соединениях возможны два различных расположения заместителей в пространстве по отношению к асимметрическому атому углерода. Это можно изобразить проекционными формулами, представляющими проекции тетраэдрических моделей на плоскость:

Образовавшиеся молекулы не могут быть совмещены и представляют собой зеркальные изображения друг друга (как правая и левая рука). Подобные пространственные изомеры называются зеркальными изомерами, энантиомерами (энантиос (греч.) – противоположный) или оптическими антиподами. Оптические антиподы имеют одинаковые физические и химические свойства, (но не биохимические) и отличаются друг от друга направлением вращения плоскости поляризованного света – вращают на один и тот же угол, но в разные стороны. При наличии в молекуле n различных асимметрических атомов углерода число оптических изомеров равно 2n.
Вопросы для самопроверки
1. Напишите структурные формулы всех изомерных гидроксимасляных кислот нормального строения. Какие соединения образуются при нагревании каждого изомера?
2. Напишите по одному уравнению реакции для кетонной и енольной форм ацетоуксусного эфира.
3. Приведите три уравнения реакций получения молочной кислоты.
4. Напишите проекционные формулы стереоизомеров для винной кислоты. Почему мезовинная кислота оптически недеятельна?
5. Напишите проекционные формулы пространственных изомеров для 2,3-дигидроксибутановой кислоты. Что такое рацемат?
Аминокислоты
Классификация и номенклатура. Получение аминокислот гидролизом белков, из галогензамещенных кислот, из оксинитрилов. Получение ароматических аминокислот восстановлением нитрокислот.
Физические свойства.
Химические свойства. Общая характеристика. Понятие о биполярном ионе. Изоэлектрическая точка. Реакция по карбоксилу и аминогруппе. Реакции, отличающие a-, b- и g-аминокислоты.
Полипептиды. Понятие о методах синтеза и гидролиза.
Методические указания
Аминокислоты являются «кирпичиками», из которых строятся белки. Аминокислоты бывают заменимые, которые синтезируются в организме человека и животных, и незаменимые, которые синтезируются только в организме растений. Они имеют амфотерный характер, обусловленный одновременным присутствием амино- и карбоксильной группы и находятся в организме в виде биполярных ионов, внутренних солей:

Для аминокислот кроме структурной изомерии известна пространственная (оптическая) изомерия, которая связана с наличием асимметрических атомов углерода. Все входящие в состав природных белков аминокислоты относятся к L-ряду.
При изучении химических свойств аминокислот следует выделить реакции по карбоксильной группе – свойства карбоновых кислот и реакции по аминогруппе – свойства аминов, а также реакции, связанные с взаимным влиянием амино- и карбоксильной групп.
Аминокислоты соединяются друг с другом ковалентной пептидной (амидной) связью, которая образуется за счет NH2-группы одной аминокислоты и СООН–группы другой аминокислоты с выделением молекулы воды. В результате такой реакции поликонденсации получают полипептиды, простейшие белки (протеины).
Вопросы для самопроверки
1. Напишите структурные формулы следующих аминокислот в виде биполярных ионов: аланина, валина, фенилаланина. Назовите их по ИЮПАК номенклатуре.
2. Напишите уравнения реакций, подтверждающие амфотерные свойства 2-аминопропановой кислоты.
3. Какие соединения образуются при нагревании следующих аминокислот: аминоуксусной, β-аминопропионовой, γ-аминомасляной?
4. Напишите структурные формулы всех дипептидов, которые могут образоваться из смеси α-аминоуксусной и α-аминопропионовой кислот.
Углеводы
Классификация углеводов.
Моносахарнды. Строение моносахаридов. Стереохимия моноз; пространственные конфигурации моносахаридов. D– и L-ряды. Циклическая структура моносахаридов, характер окисных колец; таутомерия моносахаридов в растворах; понятие о конформационной изомерии.
Способы получения моносахаридов: гидролиз ди- и полисахаридов; альдольная конденсация; оксинитрильныи синтез (метод удлинения цепи); распад по Руффу (метод укорачивания цепи).
Физические свойства моносахаридов.
Химические свойства: окисление, реакция серебряного зеркала, взаимодействие с фелинговой жидкостью, восстановление, реакция с синильной кислотой, взаимодействие с фенилгидразином, действие щелочей, алкилирование и ацилирование. Брожение гексоз. Дегидратация с циклизацией пентоз и гексоз.
Отдельные представители моносахаридов. Гексозы: глюкоза, галактоза, манноза, фруктоза. Пентозы: арабиноза, рибоза, ксилоза.
Понятие о фосфорных эфирах глюкозы и фруктозы, гликозидах и витамине С.
Дисахариды. Восстанавливающие и невосстанавливающие дисахариды. Мальтоза. Целлобиоза. Трегалоза. Лактоза. Сахароза.
Высокомолекулярные полисахариды. Крахмал. Гликоген. Целлюлоза. Понятие о пектиновых веществах. Слизи. Камеди.
Методические указания
Углеводы входят в состав клеток и тканей всех растительных и животных организмов и по массе составляют основную часть органического вещества на Земле (до 80% сухого вещества растений и около 2% сухого вещества животных организмов составляют углеводы).
Особое внимание при изучении углеводов следует обратить на строение моно-, ди- и полисахаридов: карбонильные и циклические формы моносахаридов, проекционные формулы Фишера и перспективные формулы Хеуорса, пространственная (оптическая) изомерия, отнесение моносахаридов к D- или L-ряду и др.
Характерной особенностью моносахаридов является их ярко выраженная способность к таутомерным превращениям. Различают два вида таутомерии в растворах: 1) кольчато-цепную или оксо-окси-таутомерию и 2) кето-енольную. Оба вида таутомерии являются причиной таких явлений, как мутаротация и эпимеризация.
В соответствии с химическим строением моносахариды проявляют свойства карбонильных соединений многоатомных спиртов и полуацеталей.
При изучении строения дисахаридов следует особое внимание обратить на то, с участием каких гидроксильных групп образуется эфирная связь между молекулами моносахаридов, т.е. является дисахарид восстанавливающим или невосстанавливающим.
Полисахариды являются продуктами поликонденсации моносахаридов. По строению их делят на гомополисахариды и гетерополисахариды, но те и другие играют важную биологическую роль.
Вопросы для самопроверки
1. Что такое мутаротация? Напишите уравнение реакции мутаротации для глюкозы.
2. Напишите схему реакции перехода от D-фруктозы к D-маннозе. Какой вид таутомерии имеет место при этом превращении?
3. Напишите уравнение реакции взаимодействия α-D-глюкопиранозы с пропанолом-2 (в присутствии НСl) и назовите продукт реакции.
4. Какие моносахариды образуются при гидролизе сахарозы, какой из них дает реакцию «серебряного зеркала»? Приведите уравнения реакций.
5. Получите невосстанавливающий дисахарид из молекул α- и β-D-глюкопиранозы в формулах Фишера.
6. Напишите схему ступенчатого гидролиза крахмала.
|
из
5.00
|
Обсуждение в статье: Диазо- и азосоединения |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

