 |
Главная |
Образец билета тестированного контроля. по теме: Химическая кинетика и химическое равновесие
|
из
5.00
|
по теме: Химическая кинетика и химическое равновесие.
1. Чему равна скорость реакции: 2ZnS(т) + 3O2 (г) ® 2ZnO(т) + 2SO2 (г)
a) k.C3(O2) б) k.C2(ZnS).C3(O2) в) k.C(ZnS).C(O2)
2. Как изменится скорость вышеприведённой реакции, если уменьшить объём реакционного сосуда в 2 раза? Ответ подтвердите расчётом.
а) увеличится в 8 раз; б) уменьшится в 2 раза; в) не изменится.
3. От каких факторов не зависит константа скорости реакции?
а) от температуры; б) от катализатора; в) от концентрации веществ.
4. Скорость химической реакции при 200С равна 1 моль/л.с. Вычислите скорость реакции при 600С, если температурный коэффициент равен 3.
а) 27 моль/л.с; б) 81 моль/л.с; в) 12 моль/л.с.
5. Реакция 2SO2 + O2↔ 2SO3 имеет энергию активации 60 ккал/моль и 15 ккал/моль. В каком случае она протекает в присутствии катализатора?
а) в первом случае;
б) во втором случае;
в) катализатор не участвует в реакции
6. Чему равна константа равновесия для реакции: A(ж) + 2B(т) ↔ C(ж)?
a)  б)
б)  в)
в) 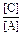
7 - 9. В каком направлении сместится равновесие реакции:
CO2 (г) + C(т) ↔ 2CO(г) , DHо298 > 0
7) при увеличении давления?
8) при уменьшении температуры?
9) при частичном удалении углерода из реакционной смеси?
a) влево; б) вправо; в) не сместится
Ответы на задания образца билета ТК:
| Номер вопроса | |||||||||
| Код ответа | а | а | в | б | б | в | а | а | в |
Лабораторные работы
по теме: Химическое равновесие.
Работа 1. Смещение химического равновесия при изменении концентрации реагирующих веществ.
Для опыта воспользуемся реакцией образования железа (III) тиоционата: FeCl3 + 3KCNS ↔ Fe(CNS)3 + 3KCl
Раствор Fe(CNS)3 - интенсивно красного цвета, раствор FeCl3 - желтоватый, а растворы KCNS и KCl - бесцветны.
При изменении концентрации Fe(CNS)3 окраска раствора изменяется, что позволяет визуально установить направление смещения равновесия.
В журнале для записи и анализа наблюдений подготовьте таблицу по следующей форме:
| Пробирка | Добавлено в пробирку | Изменение интенсивности окраски | Вывод о направлении смещения равновесия |
| FeCl3(p) KCNS(р) KCl(т) — |
Выполнение эксперимента.
К 1-2 каплям раствора FeCl3 в пробирке прилейте 1-2 капли раствора KCNS и добавьте столько воды, чтобы получился раствор, окрашенный в розовый цвет.
Полученный раствор разлейте в четыре пробирки. Затем в 1-ую пробирку прибавьте несколько капель концентрированного раствора FeCl3. Что наблюдается?
Запишите в таблицу наблюдаемое изменение окраски и укажите направление смещения равновесия (стрелка направо или налево). Затем во вторую пробирку прибавьте несколько капель концентрированного раствора KCNS. Снова отметьте и запишите в тетрадь наблюдаемое изменение окраски и укажите направление смещения равновесия. Наконец, в 3-ю пробирку прибавьте немного кристаллического KCl. Сравните окраску в 3-й пробирке после прибавления KCl с окраской раствора в 4-ой пробирке. Запишите изменение окраски и укажите направление смещения равновесия. Соответствует ли наблюдаемое смещение химического равновесия принципу Ле Шателье?
Работа 2. Смещение химического равновесия при изменении температуры.
Выполнение эксперимента.
В стакане объёмом 250 мл нагрейте воду почти до кипения. В две пробирки внесите по 5-6 капель раствора крахмала и прибавьте туда же 5 - 6 капель раствора йода. Что наблюдается? Нагрейте одну из пробирок, опустив её на несколько минут в стакан с горячей водой. Вторую пробирку оставьте для сравнения. Как изменяется окраска раствора в нагретой пробирке? Охладите нагретую пробирку. Что происходит? Запишите уравнение изученного равновесия:
I2 + крахмал ↔ [крахмал .I2]
буро-желтый бесцветный синий
Исходя из принципа Ле Шателье, ответьте на вопрос: экзо- или эндотермической является реакция образования йодокрахмала и реакция его диссоциации?
Работа 3. Обратимость смещения химического равновесия.
В растворах, содержащих соединение Cr (VI), существует равновесие:
2 CrO42- + 2H+ ↔ Cr2O72- + H2O
желтый р-р оранжевый р-р
Выполнение эксперимента.
В пробирку налейте 5–6 капель 0,5 N раствора дихромата калия и по каплям прибавьте концентрированный раствор щелочи (NaOH или KOH). Наблюдайте изменение окраски. Когда раствор приобретает желтую окраску, добавьте туда же по каплям концентрированный раствор серной кислоты и наблюдайте появление оранжевой окраски. В какой среде устойчивы дихромат-ионы Cr2O72-? В какой среде устойчивы хромат-ионы CrO42-?
Сделайте вывод о направлении смещения равновесия, исходя из принципа Ле Шателье.
Экзаменационные вопросы.
1. Основные понятия термодинамики. Внутренняя энергия. Работа и теплота - две формы передачи энергии.
2. Классификация термодинамических систем и процессов. Изобарный и изохорный процессы. Экзотермические и эндотермические реакции.
3. Первый закон термодинамики. Энтальпия. Стандартная теплота образования и стандартная теплота сгорания веществ. Закон Гесса и его следствия.
4. Второй закон термодинамики. Энтропия. Энергия Гиббса.
5. Какую тенденцию выражает: а) энтальпийный фактор б) энтропийный фактор? Какая функция состояния системы даёт количественную характеристику одновременного влияния того и другого факторов? Каким уравнением это выражается?
6. Прогнозирование направления самопроизвольно протекающих процессов.
Роль энтальпийного и энтропийного факторов.
7. Скорость химической реакции. Средняя скорость химической реакции в интервале, истинная скорость.
8. Кинетическая классификация реакций. Молекулярность и порядок реакции. Период полупревращения.
9. Зависимость скорости реакции от концентрации веществ. Закон действующих масс. Кинетические уравнения реакций.
10. Зависимость скорости реакции и времени протекания её от температуры. Температурный коэффициент.
11. Энергия активации. Уравнение Аррениуса. Энергетический профиль реакции. Роль стерического фактора. Понятие о теории переходного состояния.
12. Механизм химический реакции. Понятие о кинетике простых и сложных реакций. Цепные реакции. Фотохимические реакции, фотосинтез.
13. Катализ. Гомогенный и гетерогенный катализ. Энергетический профиль каталитической реакции.
14. Химическое равновесие. Обратимые и необратимые по направлению реакции. Кинетические условия равновесия. Вывод константы химического равновесия. Равновесные концентрации (понятие).
15. Прогнозирование направления смещения химического равновесия. Принцип Ле Шателье. Стационарное состояние организма и его подсистем.
16. Учение о растворах. Роль воды и растворов в жизнедеятельности организма. Вода как универсальный растворитель. Автопротолиз воды. Константа автопротолиза. Ионное произведение воды и его физический смысл. Водородный и гидроксильный показатели.
17. Термодинамика растворения. Растворимость твёрдых и жидких веществ в жидкостях. Понятие об идеальном растворе.
18. Растворимость газов в жидкостях. Законы Генри и Дальтона. Влияние электролитов на растворимость газов. Закон Сеченова.
19. Коллигативные свойства растворов неэлектролитов. Давление насыщенного
пара растворителя над разбавленным раствором неэлектролита. Закон Рауля.
20. Следствия из закона Рауля. Понижение температуры замерзания (кристаллизации) и повышение температуры кипения разбавленных растворов неэлектролитов по сравнению с чистым растворителем.
21. Осмос, осмотическое давление и их биологическая роль. Закон Вант-Гоффа. Определение осмотического давления по криоскопическим данным.
22. Растворы слабых электролитов. Степень и константа электролитической диссоциации. Закон разбавления Оствальда. Электролиты в организме человека.
23. Кислотно-основные равновесия. Равновесия в растворах слабых кислот. Уравнения для расчёта концентрации ионов водорода и рН в растворе слабой кислоты.
24. Кислотно-основные равновесия. Равновесия в растворах слабых оснований. Уравнения для расчёта концентрации ионов водорода и рН в растворе слабого основания.
25. Растворы сильных электролитов. Активность, коэффициент активности. Ионная сила раствора.
26. Коллигативные свойства растворов электролитов. Изотонический коэффициент и его связь со степенью диссоциации слабого электролита в растворе.
27. Осмотические свойства растворов электролитов. Гипо-, гипер- и изотонические растворы. Плазмолиз и гемолиз.
28. Протолитическая теория кислот и оснований. Влияние природы растворителя на силу кислот и оснований. Протолитические равновесия и процессы.
29. Буферные растворы, их классификация. Расчёт концентрации ионов Н+ и рН в буферных растворах разных типов.
30. Механизм буферного действия на примерах ацетатного и аммонийного буферов. Буферная ёмкость раствора.
31. Кислотно-основное равновесие и буферные системы в организме человека.
32. Реакции гидролиза, их типы. Характер водной среды в растворах солей разного типа.
33. Реакции гидролиза. Степень и константа гидролиза. Вывод выражений константы гидролиза для разных типов его.
34. Константа диссоциации слабых кислот и оснований и константа гидролиза солей разного типа, их взаимосвязь и физический смысл.
35. Гетерогенные равновесия. Произведение растворимости. Условия осаждения и растворения осадков. Полнота и последовательность осаждения.
36. Основы объёмного анализа. Классификация методов по характеру химической реакции, по способу титрования. Расчёты в объёмном анализе.
37. Требования к реакциям, применяемым в объёмном анализе. Рабочие растворы. Способы приготовления рабочих растворов (растворы с приготовленным титром, с установленным титром).
38. Методы нейтрализации - ацидометрия и алкалиметрия. Рабочие растворы этих методов. Исходные вещества и требования к ним. Использование методов нейтрализации в клинических и санитарно-гигиенических исследованиях.
39. Кислотно-основные индикаторы, механизм их действия. Интервал перехода окраски и показатель титрования. Выбор индикатора.
40. Окислительно-восстановительные реакции (ОВР). Направление окислительно-восстановительных реакций. Эквиваленты окислителя и восстановителя. Подбор коэффициентов в уравнениях ОВР (методы электронного баланса и ионно-электронного баланса или полу-реакций).
41. Оксидиметрия. Метод перманганатометрии, его особенности. Эквивалент KMnO4 в различных средах. Применение метода в клинических и санитарно-гигиенических исследованиях.
42. Оксидиметрия. Метод иодометрии, его особенности. Определение концентрации рабочих растворов по исходным веществам. Индикатор метода.
43. Координационная теория Вернера, её основные положения - о главной и побочной валентностях, о координации, о пространственной конфигурации комплексных соединений. Современные представления о характере связей в молекулах и структуре этих соединений.
44. Классификация, изомерия и номенклатура комплексных соединений. Значение их в биологических процессах.
45. Равновесие в растворах комплексных соединений. Первичная и вторичная диссоциация этих веществ. Константы нестойкости и устойчивости.
46. Комплексонометрия и её применение в медицинских исследованиях.
47. Квантово-механическая модель строения атома. Характеристика энергетического состояния электрона системой квантовых чисел.
48. Закономерности распределения электронов в атомах (принципы Паули и наименьшей энергии, правило Хунда).
49. Основное и возбуждённое состояния атома и иона. Электронная конфигурация валентных электронов s-, p-, d- и f-элементов.
50. Атомные и ионные радиусы. Энергия ионизации и сродство к электрону. Относительная электроотрицательность.
51. Развитие представлений о природе химической связи. Основные характеристики связи - длина, энергия и валентный угол. Геометрия связи и молекулы.
52. Типы химической связи. Ковалентная химическая связь. Механизмы её образования: обменный и донорно-акцепторный. Свойства ковалентной связи.
53. Ионная связь как предельно поляризованная ковалентная связь. Свойства ионной связи.
54. Металлическая связь как особый вид химической связи.
55. Водородная связь (межмолекулярная и внутримолекулярная).
56. Межмолекулярное взаимодействие (дисперсионное, индукционное, ориентационное).
57. Распространённость химических элементов в земной коре. Макро- имикроэлементы. Биогенные элементы. Биосфера, круговорот биогенных элементов.
58. Химия элементов s-блока. Электронные структуры атомов и катионов. Биологическая роль Na, K, Ca, Mg. Химическое сродство и биологический
антагонизм этих элементов (Na - K, Mg - Ca).
59. Химия элементов d-блока. Электронные структуры атомов и катионов. Наиболее биологически важные элементы блока - Cr, Cu, Mn, Fe, Zn, Co, Mo.
60. Химия элементов р-блока. Электронные структуры атомов и катионов. Значение биогенных р-элементов (C, N, P, O, S, H, галогены).
Приложение
Способы выражения концентрации растворов. Таблица 1.
| Название | Размер-ность | Формула для расчёта |
| Массовая доля, w(Х) | — | 
|
| Объёмная доля, j(Х) | — | 
|
| Молярная доля, c(Х) | — | 
|
| Молярная концентрация, С(Х) | моль/л | 
|
Молярная концентрация эквивалента, С( 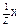 ) )
| моль/л | 
|
| Моляльная концентрация, в(Х) или Сm(X) | моль/кг | 
|
| Титр, t(X) | г/мл | 
|
Приложение
Таблица 2
Примеры определения эквивалента вещества в реакциях кислотно-основного типа.
| Уравнение реакции | Эквивалент вещества Х, 
| Фактор эквива-лент-ности | Молярная масса эквивалента |
| H3PO4 + 2KOH = K2HPO4 + 2H2O «Х» два эквивалента |
 (половина молекулы)
(половина молекулы)
|

| 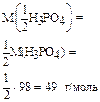
|
| H3PO4 + 3KOH = K3PO4 + 3H2O «Х» три эквивалента |  (одна треть молекулы)
(одна треть молекулы)
|

| 
|
| Al2(SO4)3 + 4KOH = [Al(OH)2]2SO4 + K2SO4 «Х» четыре эквивалента |  (четверть молекулы)
(четверть молекулы)
|

| 
|
| Mg(OH)2+H2SO4= (MgOH)2SO4 +2H2O два эквивалента | 1 Mg(OH)2 (одна молекула) | M(Mg(OH)2 = 58 г/моль |
Приложение
Таблица 3.
Связь между различными способами выражения концентрации растворов.
| Способ выражения кон-центрации, обозначение, размерность | Формула пересчёта |
| Молярная концентрация, С(Х), моль/л | 
|

| |

| |
Молярная концентрация эквивалента (нормальная концентрация),
С( 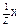 ) или N(X), моль/л ) или N(X), моль/л
| 
|
| Z. C(X) | |

| |
| Титр, t(X), г/мл | 
|
| Моляльная концентрация, в(Х) или Сm(X), моль/кг растворителя |

|
Приложение
Таблица 4.
Примеры определения фактора эквивалентности и молярной массы эквивалента в окислительно-восстановительных реакциях
| Уравнение реакции | Эквивалент вещества Х, 
| Фактор эквива-лент-ности | Молярная масса эквивалента |
 I2 + 5Cl2 + 12KOH= 2KIO3 +10KCl + 6H2O
I2 + 5Cl2 + 12OH- = 2IO3- +10Cl-+6H2O
I2 + 12OH--10e- = 2IO3- + 6H2O 1
«Х» десять эквивалентов
Cl2 + 2e- = 2Cl- 5
«Х» два эквивалента I2 + 5Cl2 + 12KOH= 2KIO3 +10KCl + 6H2O
I2 + 5Cl2 + 12OH- = 2IO3- +10Cl-+6H2O
I2 + 12OH--10e- = 2IO3- + 6H2O 1
«Х» десять эквивалентов
Cl2 + 2e- = 2Cl- 5
«Х» два эквивалента
|
 (одна десятая часть молекулы)
(одна десятая часть молекулы)
|
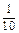

| 
|
 Cr2(SO4)3 + 3H2O2 + 10KOH = 2K2CrO4 + K2SO4 + 8H2O
2Cr3+ + 3H2O2 +10OH- = Cr2(SO4)3 + 3H2O2 + 10KOH = 2K2CrO4 + K2SO4 + 8H2O
2Cr3+ + 3H2O2 +10OH- =  +4H2O
2Cr3+ +8OH--6e- = +4H2O
2Cr3+ +8OH--6e- =  + 4H2O 1
«Х» шесть эквивалентов
H2O2 + 2е- = 2ОH- 3
«Х» два эквивалента + 4H2O 1
«Х» шесть эквивалентов
H2O2 + 2е- = 2ОH- 3
«Х» два эквивалента
| 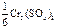 (одна шестая часть молекулы)
(одна шестая часть молекулы)
 Н2О2
(половина молекулы) Н2О2
(половина молекулы)
|
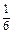

| 
|
Приложение: Таблица 5.
Произведение растворимости (ПР) некоторых малорастворимых веществ (250С, * - 18¸200С)
| Вещество | ПР | Вещество | ПР | Вещество | ПР |
| AgBr AgCN Ag2CO3 AgCl AgI AgSCN AgOH Ag3PO4* Ag2S Ag2SO4 Ag2CrO4 Al(OH)3 BaCO3 BaC2O4* BaCrO4 BaF2 BaSO4 Ba3(PO4)2 BaSO3 BaS2O3 Be(OH)2 Bi(OH)3 Bi2S3 CaCO3 CaC2O4 CaF2 Ca(OH)2 CaSO4 Ca3(PO4)2 CdCO3 Cd(OH)2 CdS CoCO3 Co(OH)2 CoS* | 7,7.10-13 2,0.10-12 6,2.10-12 1,6.10-10 1.10-16 1.10-13 2.10-8 1,8.10-18 1.10-51 7,7.10-5 4.10-12 1,9.10-33 8.10-9 1,7.10-7 2,3.10-10 1,7.10-6 1,1.10-10 6,03.10-39 8.10-7 1,6.10-5 6,3.10-22 4,3.10-31 1,6.10-72 4,8.10-9 2,6.10-9 4.10-11 3,1.10-5 6,1.10-5 1.10-29 2,5.10-14 1,2.10-14 1.10-29 1.10-12 2.10-16 2.10-27 | Cr(OH)3 CuBr CuCO3 CuCl CuI Cu(OH)2 Cu2S CuS (CuOH)2CO3 FeCO3* Fe(OH)2 Fe(OH)3 FeS GeS Hg2Br2 Hg2CO3 Hg2Cl2 Hg2I2 Hg2S HgS* K2PtCl6 La(OH)3 Li2CO3 MgCO3 MgF2 MgC2O4* MgNH4PO4 Mg3(PO4)2 Mg(OH)2 MnCO3 Mn(OH)2* MnS* Na3AlF6 NiCO3 Ni(OH)2 | 1.10-30 5,3.10-9 1,4.10-10 1,8.10-7 1,1.10-12 5,6.10-20 2,5.10-50 4.10-38 1,7.10-34 2,5.10-11 4,8.10-16 4.10-38 4.10-19 3.10-35 5.10-23 9.10-17 2.10-18 4.10-29 1.10-45 4.10-58 5.10-5 1.10-20 1,7.10-3 1.10-5 6.10-9 8,6.10-5 2,5.10-13 1.10-13 5.10-12 1.10-10 4.10-14 1,4.10-15 4,1.10-10 1,4.10-7 7.10-14 | NiS* PbBr2 PbCO3 PbCl2 PbCrO4 PbF2 PbI2 Pb(OH)2 PbS PbSO4 Pd(OH)2 PtBr4 PtCl4 PtS Sb(OH)2 Sb2S3 Sn(OH)2 Sn(OH)4 SnS SrCO3 SrC2O4* SrF2 SrSO4 Th(OH)4 Ti(OH)3 TlBr TlCl Tl(OH)3 Tl2SO4 Tl2S ZnCO3 Zn(OH)2 ZnS* (сфалерит) Zn(CN)2 | 1,4.10-24 7,4.10-6 1,5.10-13 1,7.10-5 1,8.10-14 3,7.10-8 8,7.10-9 2.10-16 1.10-29 2.10-8 1.10-24 3.10-41 8.10-29 8.10-43 4.10-42 1,6.10-93 5.10-26 1.10-56 1.10-28 1.10-9 5,6.10-8 3,4.10-9 2,8.10-7 1.10-50 1.10-40 4.10-6 2.10-4 1.10-44 4.10-3 5.10-21 6.10-11 5.10-17 8.10-26 2,6.10-13 |
Таблица 6. Константы нестойкости комплексных ионов в водных растворах.
| Схема диссоциации | Кн | Схема диссоциации | Кн |
 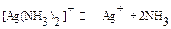 


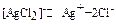


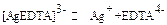 



  


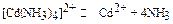 

 
| 1.10-33 9,3.10-8 1,8.10-3 2,5.10-14 8.10-22 1,76.10-5 7,8.10-8 2.10-5 4,8.10-8 5.10-39 8,5.10-16 1.10-21 1,5.10-30 4.10-42 5,3.10-20 8.10-7 2.10-4 2,5.10-9 7,6.10-8 1,4.10-19 6.10-11 3,3.10-17 2,1.10-13 |   
    
   
  
 


 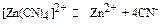  
| 9,6.10-29 3,2.10-19 7,4.10-21 1,6.10-19 3.10-7 2,6.10-11 2,8.10-6 2,2.10-11 7,9.10-14 8,1.10-20 6,3.10-3 1.10-24 1.10-31 2,8.10-9 5,9.10-4 1,1.10-8 1,8.10-14 1.10-16 3.10-21 3,5.10-10 1,3.10-17 3,6.10-16 2.10-4 |
Приложение
Таблица 7
Таблица логарифмов для вычисления рН
| Числа | ||||||||||
Примеры расчета рН по величинам [H+]:
[H+] = 5,3.10-1 моль/л; рН = -lg[H+] = -lg 5,3.10-1 = - (0,724 - 1) = -(-0,276) » 0,28;
[H+] = 5,3.10-4 моль/л; рН = -lg[H+] = -lg5,3.10-4 = -(0,724 - 4) = -(-3,276) » 3,28;
Примеры расчета [H+] по величинам рH:
рН = 0,42; [H+] = antilg(-рН) = antilg (-0,42) = antilg (0,580 - 1) = 3,8.10-1 моль/л;
рН = 3,42; [H+] = antilg(-рН) = antilg (-3,42) = antilg (0,580 - 4) = 3,8.10-4 моль/л.
Приложение
Таблица 8
Множители и приставки для образования десятичных кратных и дольных и их наименований
| Мно-жи-тель | Прис-тавка | Обозначение | Мно-жи-тель | Прис-тавка | Обозначение | ||
| Русс-кое | Между-народное | Русс-кое | Между-народное | ||||
| 1012 109 106 103 102 | тера- гига- мега- кило- гекто- дека- | Т Г М к г да | T G M k h da | 10-1 10-2 10-3 10-6 10-9 10-12 | деци- санти- милли- микро- нано- пико- | g с м мк н п | D c m m n p |
Таблица 9
Константы ионизации оснований (250С)
| Формула | Kа1 | Kа2 | Kа3 | pKа |
| NaOH LiOH Ba(OH)2 Sr(OH)2 Ca(OH)2 Mg(OH)2 La(OH)3 Fe(OH)2 Zn(OH)2 NH4OH Cu(OH)2 Fe(OH)3 Al(OH)3 Cr(OH)3 V(OH)3 | 5,9 6,75.10−1 2,3.10−1 − − − − 1,2.10−2 − 1,79.10−5 3,4.10−7 − − − − | − − − 1,5.10−1 4,3.10−2 2,5.10−3 − 1,3.10−4 4.10−1 − − 1,82.10−11 − − − | − − − − − − 5,2.10−4 − − − − 1,35.10−12 1,38.10−9 1,02.10−10 8,3.10−12 | −0,77 0,17 0,64 0,82 1,37 2,6 3,3 3,89 4,4 4,75 6,47 10,74 8,86 9,99 11,08 |
Приложение
Таблица 11: Растворимость кислот, оснований и солей в воде при 250С
| Анионы | Катионы | ||||||||||

| K+, Na+ | 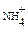
| Ba2+ | Ca2+ | Mg2+ | Sr2+ | Al3+ | Cr3+ | Fe2+ | Fe3+ | |
| OH─ | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н |
| F─ | М | Р | Р | М | Н | Н | Н | М | Н | Н | Н |
| Cl─ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |
| Br─ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |
| I─ | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? |

| Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |

| Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? |
| S2─ | Р | Р | Р | Р | Р | — | Н | — | — | Н | — |
| HS─ | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? |

| Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? |

| Р | Р | Р | Н | Н | Р | Н | Р | Р | Р | Р |

| Р | Р | Р | ? | Р | ? | — | ? | ? | ? | ? |

| Р | Р | Р | Н | Н | Н | Н | — | — | Н | ? |

| Р | Р | Р | Р | Р | Р | Р | ? | ? | Р | ? |

| Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? |

| ? | Р | — | Н | Р | Р | М | — | — | ? | Н |

| Н | Р | — | Н | Н | Н | Н | Н | Н | Н | Н |

| ? | Р | Р | Н | Н | М | Н | ? | ? | Н | ? |

| Р | Р | Р | Р | Р | Р | Р | ? | ? | Р | ? |
| HCOO─ | Р | Р | Р | Р | Р | Р | ? | Р | Р | Р | Р |
| CH3COO─ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — |
«Р»− растворяется (> 1 г на 100 г Н2О)
«М» − мало растворяется (от 0,1 г до 1 г на 100 г Н2О)
Приложение
Продолжение таблицы 11
| Анионы | Катионы | ||||||||||||

| 
| 
| 
| Ag+ | 
| 
| 
| 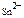
| Cu2+ | ||||
| OH─ | Н | Н | Н | Н | — | — | — | Н | Н | Н | |||
| F─ | Р | Р | Р | Р | Р | ? | — | Н | Р | Р | |||
| Cl─ | Р | Р | Р | Р | Н | Н | Р | М | Р | Р | |||
| Br─ | Р | Р | Р | Р | Н | Н | М | М | Р | Р | |||
| I─ | Р | Р | Р | Р | Н | Н | Н | Н | М | Р | |||

| Р | Р | Р | Р | Р | Р | Р | Р | — | Р | |||

| Р | М | ? | ? | М | ? | ? | ? | ? | ? | |||
| S2─ | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | |||
| HS─ | ? | Н | ? | ? | ? | ? | ? | ? | ? | ? | |||

| Н | Н | ? | М
Популярное: Почему человек чувствует себя несчастным?: Для начала определим, что такое несчастье. Несчастьем мы будем считать психологическое состояние... Организация как механизм и форма жизни коллектива: Организация не сможет достичь поставленных целей без соответствующей внутренней... Как вы ведете себя при стрессе?: Вы можете самостоятельно управлять стрессом! Каждый из нас имеет право и возможность уменьшить его воздействие на нас...  ©2015-2024 megaobuchalka.ru Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. (616)
|
Почему 1285321 студент выбрали МегаОбучалку... Система поиска информации Мобильная версия сайта Удобная навигация Нет шокирующей рекламы |
(0.012 сек.)

