 |
Главная |
Окислители и восстановители
|
из
5.00
|
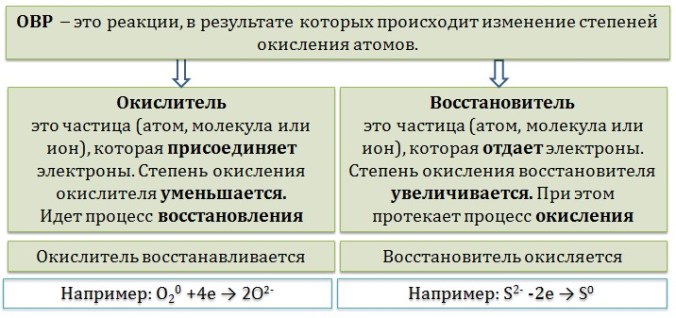
Окислители — это частицы (атомы, молекулы или ионы), которые принимают электроны в ходе химической реакции. При этом степень окисления окислителя понижается. Окислители при этом восстанавливаются.
Восстановители — это частицы (атомы, молекулы или ионы), которые отдают электроны в ходе химической реакции. При этом степень окисления восстановителя повышается. Восстановители при этом окисляются.
Химические вещества можно разделить на типичные окислители, типичные восстановители, и вещества, которые могут проявлять и окислительные, и восстановительные свойства. Некоторые вещества практически не проявляют окислительно-восстановительную активность.
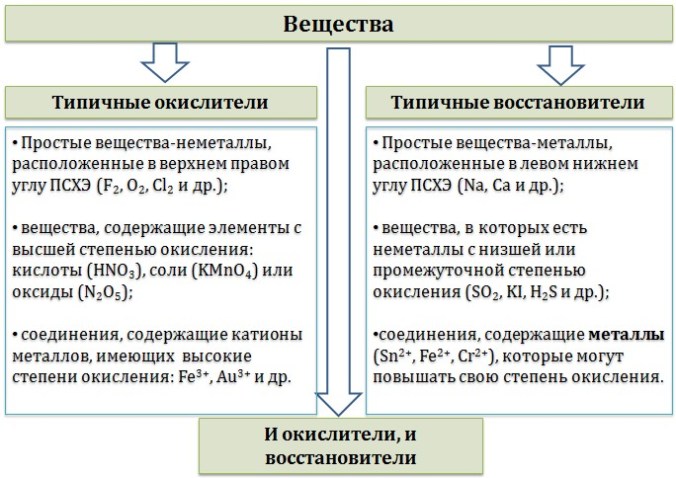
К типичным окислителям относят:
· простые вещества-неметаллы с наиболее сильными окислительными свойствами (фтор F2, кислород O2, хлор Cl2);
· сложные вещества, в составе которых есть ионы металлов или неметалловс высокими положительными (как правило, высшими) степенями окисления: кислоты (HN+5O3, HCl+7O4), соли (KN+5O3, KMn+7O4), оксиды (S+6O3, Cr+6O3)
· соединения, содержащие некоторые катионы металлов, имеющих высокие степени окисления: Pb4+, Fe3+, Au3+ и др.
Типичные восстановители – это, как правило:
· простые вещества-металлы (восстановительные способности металлов определяются рядом электрохимической активности);
· сложные вещества, в составе которых есть атомы или ионы неметаллов с отрицательной (как правило, низшей) степенью окисления: бинарные водородные соединения (H2S, HBr), соли бескислородных кислот (K2S, NaI);
· некоторые соединения, содержащие катионы с минимальной положительной степенью окисления (Sn2+, Fe2+, Cr2+), которые, отдавая электроны, могут повышать свою степень окисления;
· соединения, содержащие сложные ионы, состоящие из неметаллов с промежуточной положительной степенью окисления (S+4O3)2–, (НР+3O3)2–, в которых элементы могут, отдавая электроны, повышать свою положительную степень окисления.
Большинство остальных веществ может проявлять как окислительные, так и восстановительные свойства.
Типичные окислители и восстановители приведены в таблице.
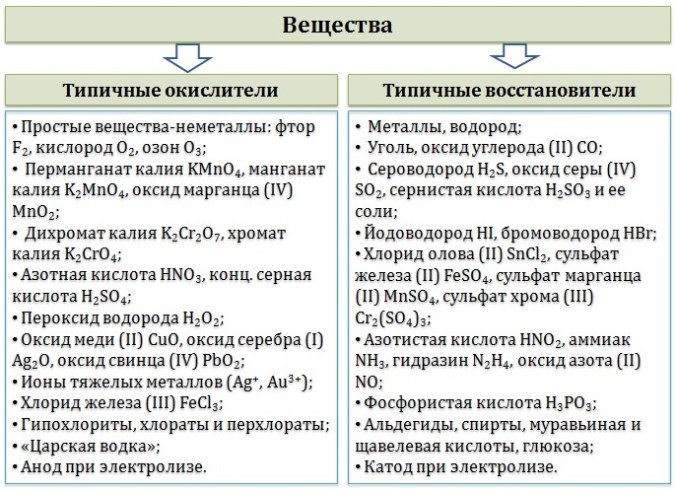
В лабораторной практике наиболее часто используются следующие окислители:
· перманганат калия (KMnO4);
· дихромат калия (K2Cr2O7);
· азотная кислота (HNO3);
· концентрированная серная кислота (H2SO4);
· пероксид водорода (H2O2);
· оксиды марганца (IV) и свинца (IV) (MnO2, PbO2);
· расплавленный нитрат калия (KNO3) и расплавы некоторых других нитратов .
К восстановителям, которые применяются в лабораторной практике относятся:
· магний (Mg), алюминий (Al), цинк (Zn) и другие активные металлы;
· водород (Н2) и углерод (С);
· иодид калия (KI);
· сульфид натрия (Na2S) и сероводород (H2S);
· сульфит натрия (Na2SO3);
· хлорид олова (SnCl2).
|
из
5.00
|
Обсуждение в статье: Окислители и восстановители |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

