 |
Главная |
КИНЕТИКА ЦЕПНЫХ РЕАКЦИЙ.
|
из
5.00
|
Неразветвленные реакции.
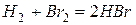
Распишем эту реакцию по стадиям:

Выведем кинетическое уравнение, используя метод стационарных концентраций относительно промежуточных продуктов – атомов  и
и  .
.

Складываем эти две скорости и получаем:

Из второго уравнения выразим концентрацию радикальных частиц водорода:

Составим уравнение скорости суммарной реакции:

и подставим в него значения концентраций атомов водорода и брома:

Разветвленные реакции.
Реакция синтеза бромистого водорода – пример простой цепи. В этом случае количество первоначально возникших частиц не изменяется. Примером разветвленных реакций является реакция горения водорода:
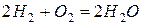
Эту реакцию можно разбить на стадии:
 зарождение цепи
зарождение цепи
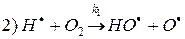 разветвление цепи
разветвление цепи
 продолжение цепи
продолжение цепи
 обрыв цепей на стенке
обрыв цепей на стенке
 обрыв цепей в объеме
обрыв цепей в объеме
Образование свободного радикала  при тройном соударении рассматривается как реакция обрыва цепи, так как этот свободный радикал малоактивен и при не очень больших давлениях не может продолжать цепь.
при тройном соударении рассматривается как реакция обрыва цепи, так как этот свободный радикал малоактивен и при не очень больших давлениях не может продолжать цепь.
Обозначим:
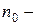 число активных частиц, появившихся в результате акта зарождения цепи.
число активных частиц, появившихся в результате акта зарождения цепи.
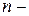 количество всех активных частиц.
количество всех активных частиц.
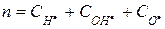 ;
;  и
и 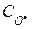

Система дифференциальных уравнений для концентраций свободных радикалов запишется в виде:




f – фактор g – фактор
разветвления цепи обрыва цепи

Модельное уравнение Семенова
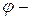 фактор автоускорения.
фактор автоускорения.
АНАЛИЗ УРАВНЕНИЯ СЕМЕНОВА.

неразветвленный разветвленный

Для стационарных процессов по теории Боденштейна  .
.
 ,
,  ,
, 

Рассмотрим разветвленные процессы:
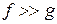 ,
,  ,
, 

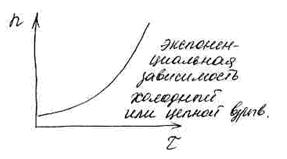
В этом случае имеет место прогрессивное нарастание концентрации радикалов, а следовательно, и скорости цепной реакции. В определенный момент времени скорость становится такой большой, что приводит к цепной воспламеняемости или взрыву.
Пределы взрываемости цепной реакции:

 нижний предел взрываемости. Он зависит от формы и материала сосуда.
нижний предел взрываемости. Он зависит от формы и материала сосуда.
 верхний предел взрываемости. Зависит от состава и количества примесей, от природы веществ, в незначительной степени от температуры.
верхний предел взрываемости. Зависит от состава и количества примесей, от природы веществ, в незначительной степени от температуры.
Ниже нижнего предела взрываемости обрыв цепи происходит за счет соударения о стенки сосуда.
Выше верхнего предела взрываемости обрыв цепи происходит за счет тройных соударений.
ОСОБЕННОСТИ ЦЕПНЫХ РЕАКЦИЙ.
1. Реальная скорость процесса намного больше теоретической.
2. На скорость процесса влияют форма и материал сосуда.
3. На скорость влияет наличие примесей в реакционной среде.
4. Цепные реакции имеют верхний и нижний предел взрываемости.
|
из
5.00
|
Обсуждение в статье: КИНЕТИКА ЦЕПНЫХ РЕАКЦИЙ. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

