 |
Главная |
Общая характеристика элементов I А группы. Особенности лития и его соединений.
|
из
5.00
|
ЛЕКЦИЯ 1
Тема: s - Э лементы I группы
Общая характеристика элементов I А группы. Особенности лития и его соединений.
В периодической системе всего 14 s -элементов (включая водород и гелий). Это элементы I А и II А групп. Элементы I А группы – щелочные металлы Li, Na, K, Rb, Cs, Fr. Все они имеют на внешнем электронном уровне атома по одному электрону ns 1, сильно удаленному от ядра, с низким потенциалом ионизации. Всегда проявляют степень окисления +1.

Сверху вниз в подгруппе возрастает радиус атома элементов за счет возникновения новых электронных уровней.
В группах по мере увеличения числа энергетических уровнейатомные радиусы растут. Переход нейтрального атома в катион 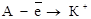 , сопровождается уменьшением радиуса поскольку в катионе заряд ядра удерживает меньшее число электронов. Очевидно, с возрастанием заряда ионный радиус катиона будет падать.
, сопровождается уменьшением радиуса поскольку в катионе заряд ядра удерживает меньшее число электронов. Очевидно, с возрастанием заряда ионный радиус катиона будет падать.
Энергия ионизации– это та энергия, которую необходимо затратить на отрыв внешнего электрона у невозбужденного атома. Строение внешних оболочек ns 1, поэтому они имеют низкие энергии ионизации, уменьшающиеся при переходе по подгруппе сверху вниз. Связь электрона с ядром ослабевает при этом за счет увеличения радиуса атома и экранирования заряда ядра предшествующими внешнему электрону оболочками, увеличивается расстояние электрона от ядра и энергия ионизации уменьшается.
С ростом заряда ядра от Na к Fr усиливаются восстановительные свойства, это самые активные металлы. Их стандартные электродные потенциалы j° отрицательные и имеют большое абсолютное значение. Наиболее отрицателен j° лития равный -3,02 В по сравнению с ионами других щелочных металлов (ион Li+ имеет среди них наименьший радиус), хороший комплексообразователь. Энтальпия гидратации катионов лития велика (∆Н° гидрат.= - 486,6 кДж/моль). Чем меньше алгебраическая величина потенциала, тем выше восстановительная способность этого металла и тем ниже окислительная способность его ионов. Металлический литий – самый сильный восстановитель, а ион Li+ самый слабый окислитель.
С увеличением порядкового номера, уменьшается относительная электроотрицательность (ОЭО).
Все щелочные металлы образуют одинаковую кристаллическую структуру. У щелочных металлов тип металлической структуры – объемно - центрированная кубическая упаковка (ОЦКУ).
|

От Li к Cs увеличиваются размеры атомов и межъядерные расстояния в кристаллических решетках. Так как химическая связь большей длины является менее прочной, то по мере роста межъядерного расстояния уменьшается прочность кристаллических решеток, поэтому снижаются температуры плавления и кипения. Щелочные металлы активно окисляются кислородом воздуха при обычной температуре, поэтому их хранят под слоем керосина или бензина.
4Э + О2 = 2Э2О
Взаимодействуют с другими окислителями (галогенами, серой, фосфором), образуя соединения LiCl, Li2S, Li3P, NaBr, Na2S.
С азотом взаимодействует только литий при обычной температуре.
6 Li + N 2 = 2 Li 3 N
Нагревая щелочной литий в струе газообразного водорода получают гидрид.
2 Li + Н2 = 2 LiH - .
С кислородом образуют оксиды, пероксиды, надпероксиды, озониды.
4 Li + O 2 → 2 Li 2 O – оксид лития
2 Na + O 2 → Na 2 O 2 – пероксид натрия
K + O 2 → KO 2 – надпероксид (супероксид калия)
Пероксиды содержат диамагнитный ион О22-, надпероксиды– парамагнитный ион О2-.

Оксиды Na и K могут получиться при недостатке кислорода. Элементы могут образовывать озониды по реакции с озоном:
K + O 3 → KO 3
KOH + O 3 → KO 3 + O 2 + H 2 O
Все озониды, пероксиды, надпероксиды сильные окислители и разлагаются водой.
 KO2 + H2O → KOH + O2 + H2O2
KO2 + H2O → KOH + O2 + H2O2
KO2 + H2O( теплая ) → KOH + O2
КО 3 + H2O → KOH + O2
Причем разложение может идти как обменное взаимодействие.
Na2O2 + 2H2O → 2NaOH + H2O2
Оксиды щелочных металлов Ме2О – кристаллические термически устойчивые вещества, при взаимодействии с водой образуют щелочи.
Ме2О + Н2О = 2МеО H
 Ме2 O + H 2 O → 2 MeOH лабораторные способы
Ме2 O + H 2 O → 2 MeOH лабораторные способы
2 Na + 2 H 2 O → 2 NaOH + H 2↑ получения щелочей
карбонатный способ получения щелочей:
Na2CO3 + Ca(OH)2 → CaCO3↓ + 2NaOH
В промышленности NaOH получают электролизом раствора поваренной соли:
NaCl + H 2 O электролиз → NaOH + Cl 2 + H 2
K ( - ) 2H2O + 2e = H2 + 2OH-
A ( + ) 2Cl- - 2e = Cl2
Этим способом получают достаточно чистый NaOH.
Оксиды и гидроксиды
| Li2O Na2O K2O Rb2O Cs2O Fr2O | растворимость | LiOH
NaOH
KOH
RbOH
CsOH
FrOH | сила оснований |
Гидроксиды щелочных металлов МеОН – твердые кристаллические вещества, легкоплавки, хорошо растворяются в воде с выделением тепла (кроме LiOH), полностью диссоциируют на ионы, сила оснований растет от Li к Fr.
ЭОH ® Э+ + OH-

Более активно реагируют с водой непосредственно щелочные металлы.

Интенсивность взаимодействия с водой увеличивается в ряду Li - Cs, Rb и Cs реагируют с Н2О со взрывом.
Свойства гидроксидов
Все растворимы в воде – щелочи.
LiOH, NaOH, KOH, RbOH, CsOH, FrOH
 |
реакционная способность увеличивается
1) реакция нейтрализации:
NaOH + HCl → NaCl + H2O
2) c кислотными оксидами:
NaOH + CO2 → NaHCO3
2NaOH + CO2 → Na2CO3 + H2O
3) с амфотерными оксидами:
2NaOH + BeO + H2O → Na2[Be(OH)4]
4) с неметаллами:
С l 2 + KOH → KCl + KClO + H 2 O
холодная
С l 2 + KOH → KCl + KClO 3 + H 2 O
горячая
3S + 6NaOH → 2Na2S + Na2SO3 + 3H2O
5) с амфотерными металлами:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
6) с солями:
2 AlCl 3 + 6 NaOH (недост.) → 2 Al ( OH )3 + 6 NaCl
AlCl3 + 4 NaOH( избыт .) → Na[Al(OH)4] + 3NaCl
7) с амфотерными гидроксидами:
Zn(OH)2 + 2NaOH → Na2[Zn(OH)4]
Щелочи жадно поглощают из воздуха влагу и СО2, т.е. содержат примесь Н2О (в виде кристаллогидратов NaOH×H2O) и карбонатов.
Щелочи при плавлении разрушают стекло и фарфор

ΔG0298= -100кДж
За счет этого щелочи нельзя долго хранить в посуде с пришлифованными пробками, они прилипают вследствие взаимодействия щелочи со стеклом.
Твердые щелочи и их концентрированные растворы разрушают живые ткани, особенно опасно попадание частиц твердой щелочи в глаза (приводит к слепоте).
Не только с кислотами, но даже с водой большинство щелочных металлов реагируют со взрывов – отсюда шутливые плакаты с серьезным подтекстом в студенческих практикумах: «Не хотите быть уродом, не бросайте натрий в воду!»
Особенности лития и его соединений
Литий существенно отличается от остальных элементов IA группы. Особые свойства характерны для всех элементов II периода. В отличие от остальных ионов щелочных металлов, у которых по 8 электронов на предвнешнем уровне ион Li+ имеет только 2 электрона. У лития на кайносимметричной 2р-орбитали нет еще ни одного электрона.
Связь лития с другими элементами имеет менее ионный характер, что приближает его к магнию (диагональное сходство элементов в периодической системе). В периодической системе только у 2-го или даже 3-го элемента А групп полностью проявляются характерные свойства. Аномальное поведение Li заключается в том, что у Li самое отрицательное значение электродного потенциала и можно ожидать, что Li поэтому должен быть самым активным из всех металлов. Но это не так. По активности он близок к Mg, Ca.
Поэтому низкое значение электродного потенциала объясняется тем, что у Li самая высокая энергия гидратации из-за малого размера атома. Такая закономерность справедлива лишь для всех водных растворов. По химическим свойствам Li отличается от щелочных металлов, как и его соединения.
Подобно соединениям магния малорастворимы в воде LiF, Li2CO3, Li3PO4. LiOH менее других растворим в воде.
Li взаимодействует с азотом Li3N,
6 Li + N 2 → 2 Li 3 N -3 (нитрид лития),
с кремнием − Li4Si,
4 Li + Si → Li 4 Si (силицид лития)
с углеродом – Li2С2,
2 Li + 2C =  (ацетиленид лития)
(ацетиленид лития)
с водородом − LiH,
2 Li + H 2 → 2 LiH (гидрид лития)
с кислородом − Li2O
4 Li + O 2 → 2 Li 2 O (оксид лития)
Гидроксиды МеОН, за исключением LiOH выдерживают нагревание до более 1000°С, LiOH разлагается при температуре красного каления (550 – 6000С).
Кислородосодержащие соединения (LiOH, LiNO3, Li2CO3) при нагревании разлагаются.


Li2CO3  Li2O + CO2↑
Li2O + CO2↑
Малый радиус иона Li+ обусловливает возможность координации лигандов вокруг этого иона, образование большого числа двойных солей, различных сольватов, высокую растворимость ряда солей лития в органических растворителях (подобно магнию).

Аналогию в свойствах соединений лития и магния можно объяснить близостью величин их ионных радиусов
r (Li+) = 0,068 нм, r (Mg+2) = 0,074 нм.
Получение элементов I А группы
Получение Li :
1) В промышленности – электролизом расплавов солей:
2 LiCl  2 Li + Cl 2
2 Li + Cl 2
Расплав
K ( -) Li+ + 1e →Li0
A (+) 2Cl- - 2e →Cl2
Электролизом водных растворов щелочных металлов их получить нельзя.
2) Остальные металлы получают в основном:
а) металлотермией из расплавов солей или оксидов;
LiCl + Na  Li + NaCl
Li + NaCl
CsCl + Na  Cs + NaCl
Cs + NaCl
Na – получить трудно, т.к. tпл Na и NaCl близки, и для понижения tпл необходимы добавки.
Наиболее чистый Na, K получают
б) электролизом расплавов их хлоридов или гидроксидов.
 расплав
расплав

Реже используется восстановление соединений щелочных металлов Al, Si или коксом; полученные при этом металлы не отличаются высокой чистотой из-за частичного образования алюминатов, карбидов, силицидов.




Возможность протекания этих реакций объясняется более высокой летучестью щелочных металлов по сравнению с Si, С, Al (tкипения(Al) = 2467°C, а tкипения (Na) = 983°C).
Получение соды по методу Сольве
Исходные вещества NH3, CO2, NaCl,
вначале получают CO2
CaCO 3  CaO + CO 2
CaO + CO 2
В теплый насыщенный раствор NaCl пропускают аммиак, а затем углекислый газ, вначале образуется NH4HCO3
1)  ,
,
далее он вступает в обменную реакцию с NaCl
2)  .
.
Из 4-х солей наименее растворим в воде NaHCO3, который выпадает в осадок, затем при нагревании
3)  .
.
2. Водород ( Hydrogenium – воду рождающий)
Имеет 3 изотопа: протий  , дейтерий
, дейтерий  или Д и тритий
или Д и тритий  или Т, тритий образуется в атмосфере в результате ядерных реакций, вызванных действием космического излучения.
или Т, тритий образуется в атмосфере в результате ядерных реакций, вызванных действием космического излучения.
Свободного водорода на Земле почти нет, в атмосфере его содержание не превышает 5×10-5%. Практически весь водород находится в связанном состоянии в составе многих минералов, углей, нефти, живых и растительных организмов, но самым распространенным его соединением является вода.
Водород – s-элемент, в различных вариантах периодической системы помещают его то в I A, вместе со щелочными металлами, то в VII A вместе с галогенами, а иногда рассматривают отдельно.
Со щелочными металлами он сходен в том, что образует положительный ион Н+ и играет роль восстановителя.
Но с галогенами у него больше сходства: в гидридах активных металлов (CaH2, NaH), содержится ион Н-, подобный ионам Г- (NaCl, CaCl2). Молекулы водорода и галогенов двухатомны (Н2, Cl2, Br2). Для водорода, как и для фтора, хлора, характерны газообразное состояние и неметаллические свойства. Потенциалы ионизации водорода и галогенов близки. Атомы водорода легко замещаются атомами галогенов в органических соединениях. Поэтому вариант ПС, где Н возглавляет VII А группу более правилен.
Особенности водорода – единственный валентный электрон водорода находится непосредственно в зоне действия атомного ядра. Особенностями строения атома водорода обусловлено существование водородной связи.
Получение Н2
В промышленности водород получают из воды и углеводородов. При этом восстановителем водорода при температуре (600-900°С) являются атомы углерода
 .
.
Конверсия метана с водяным паром:
 .
.
При более высокой температуре (950-1100°) можно получить разложением метана особо чистый водород и углерод.

В лаборатории:
1) при действии разбавленного раствора кислоты на активный металл (в аппарате Киппа):

или
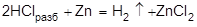
2) щелочные металлы и щелочноземельные вытесняют водород из воды.

3) действием едких щелочей на металлы
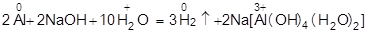

или 
4) разложением гидридов типичных металлов водой

5) электролизом воды (электролиз водных растворов щелочей).
2H2O  2H2 + O2
2H2 + O2
Физические свойства. В обычных условиях водород – это самый легкий газ без цвета, запаха и вкуса, плохо растворим в воде.
Атомарный водород гораздо активнее молекулярного, для которого нужны дополнительные затраты энергии на расcпаривание электронов.
По электроотрицательности занимает промежуточное положение между неметаллами и металлами. И в реакциях с неметаллами и кислородсодержащими веществами играет роль восстановителя.
Химические свойства Н2
Водород легко соединяется с кислородом, горит на воздухе или в атмосфере чистого кислорода бледно-синим пламенем.
1) 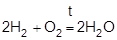
Если состав смеси приближается к стехиометрическому
(2 объема Н2 и 1 объем кислорода), то смесь называется “гремучим газом”, т.к. реакция имеет в этом случае взрывной характер.
Водородно-кислородное пламя, имеющее температуру 2500°-2800°С используют для плавления тугоплавких металлов и автогенной сварки.
2)  (при температуре 450 – 5000С и повышенном давлении, в присутствии катализатора).
(при температуре 450 – 5000С и повышенном давлении, в присутствии катализатора).
3)  (при нагревании).
(при нагревании).
4)  (при повышении температуры и давления, в присутствии катализатора).
(при повышении температуры и давления, в присутствии катализатора).
5)  (с очень активными металлами водород взаимодействует непосредственно как окислитель, превращаясь в ион Н- (гидрид-ион).
(с очень активными металлами водород взаимодействует непосредственно как окислитель, превращаясь в ион Н- (гидрид-ион).
3. Вода и ее свойства. Экологическое и биологическое значение Н2О
Три изотопа водорода  и три стабильных изотопа кислорода 16О, 17О, 18О в различных сочетаниях могут образовывать 18 изотопических разновидностей воды с молекулярными массами от 18 до 24 (Т218О). В тяжелой воде вещества растворяются хуже, растворы меньше проводят электрический ток. Она гигроскопична, жадно поглощает влагу из воздуха. Помещенные в нее без предварительной подготовки живые существа (рыбы, черви и т.п.) погибают, семена в ней не прорастают, микробы не живут. Вода имеет очень большое значение в жизни растений, животных и человека. Согласно с современными представлениями происхождение жизни связано с водной средой. Во всяком живом организме в воде протекают химические процессы, обеспечивающие жизнедеятельность организма.
и три стабильных изотопа кислорода 16О, 17О, 18О в различных сочетаниях могут образовывать 18 изотопических разновидностей воды с молекулярными массами от 18 до 24 (Т218О). В тяжелой воде вещества растворяются хуже, растворы меньше проводят электрический ток. Она гигроскопична, жадно поглощает влагу из воздуха. Помещенные в нее без предварительной подготовки живые существа (рыбы, черви и т.п.) погибают, семена в ней не прорастают, микробы не живут. Вода имеет очень большое значение в жизни растений, животных и человека. Согласно с современными представлениями происхождение жизни связано с водной средой. Во всяком живом организме в воде протекают химические процессы, обеспечивающие жизнедеятельность организма.
|
Вода обладает аномально большой теплоемкостью равной 4,18 , песок = 0,79, NaCl = 0,88 (Дж/(г×К).
Поэтому это имеет большое значение для жизни. При переходе от лета к зиме, ото дня к ночи она остывает медленно и является регулятором температуры на земном шаре.
Она имеет самую высокую температуру кипения в ряду
Н2О – Н2S – H2Se – H2Te,
Tкипения, °С 100 -60 -41 -2
Если от H2Te к Н2S температура кипения закономерно уменьшается, то при переходе от Н2S к Н2О резко увеличивается. Это объясняется наличием водородной связи между молекулами воды, вследствие кулоновского взаимодействия положительно заряженного атома водорода одной молекулы и электроотрицательным атомом кислорода другой
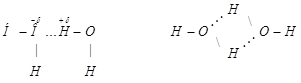
Такое взаимодействие затрудняет отрыв молекул друг от друга, т.е. уменьшает их летучесть, а, следовательно, повышает температуру кипения.
Молекула воды из-за sp3-гибридизации орбиталей атома кислорода имеет угловую конфигурацию, а атомы водорода, соединенные с сильно-электроотрицательным атомом кислорода, определяют ее способность к установлению четырех водородных связей с соседними молекулами.

|
Химические свойства Н2О
Вода – очень активный реагент по следующим причинам:
а) за счет ориентационного взаимодействия с полярными молекулами других веществ;
б) установления водородных связей;
в) проявления донорных свойств со стороны атома кислорода по отношению к частицам – акцепторам электронных пар;
г) электролитической диссоциации при обычных условиях (ионы Н+ гидратируются, образуя ионы Н3О+ ).
1. При температуре выше 1000°С диссоциация водяного пара, но равновесие сдвинуто в сторону воды.
 .
.
2. Оксиды металлов и неметаллов соединяются с водой, образуя основания и кислоты (гидрооксиды).


3. Некоторые соли образуют с водой кристаллогидраты. При растворении веществ с ионной структурой молекулы растворителя удерживаются около иона силами электростатического притяжения, т.е. за счет ион -дипольного взаимодействия.
Например: кристаллогидрат сульфата натрия Na2SO4×10H2O (глауберова соль), Na2CO3×10H2O - кристаллическая сода.
Гидраты, образующиеся в результате донорно-акцепторного взаимодействия (где ионы растворенного вещества выступают обычно в качестве акцепторов, а молекулы растворителя в качестве доноров электронных пар) представляют собой частный случай комплексных соединений.
Аквакомплексы– лигaндами является вода, [Co(H2O)6]Cl2, [Al(H2O)6]Cl3, [Cr(H2O)6]Cl3 и др. Некоторые аквакомлексы в кристаллическом состоянии удерживают кристаллизационную воду [Cu(H2O)4]SO4×H2O – медный купорос.
4. Пероксид водорода. Окислительно - восстановительная двойственность Н2О2
1. Строение молекулы. Структурная формула Н - О – О - Н. Энергия связи О-О (210 кДж/моль) почти в 2 раза меньше энергии связи О-Н (468 кДж/моль). Из-за несимметричного распределения связей Н - О молекула Н2О2 сильно полярна. Между молекулами Н2О2 возникает довольно прочная водородная связь, поэтому в обычных условиях Н2О2 – сиропообразная светло-голубая жидкость с высокой температурой кипения равной 150°С. Температура плавления 0,41°С. Почти в 1.5 раза тяжелее воды, поверхностное натяжение (σ) больше, чем у Н2О.
В молекуле Н2О2 связи между атомами кислорода и водорода полярны (вследствие смещения общих электронных пар к кислороду). В водных растворах – это слабая кислота, хоть и в незначительной степени распадается на ионы:
 I ст. К1 = 2,6×10-12.
I ст. К1 = 2,6×10-12.
 II ст. практически не протекает,
II ст. практически не протекает,
т.к. подавляется диссоциацией Н2О, которая протекает в большей степени, чем Н2О2. Сместить диссоциацию по 2-й ступени можно введением щелочи.
2. С некоторыми основаниями Н2О2 взаимодействует непосредственно образуя соли, что подтверждает его кислотные свойства.
Ba(OH)2 + H2O2 = BaO2 + 2H2O
соль
пероксида водорода
3. В отличие от воды пероксид водорода – непрочное соединение, разлагается даже при комнатной температуре (диспропорционирует на свету)
Н2О2-1 + Н2О2-1 = О20 + 2Н2О-2
Н2О2 = Н2О+ О
Неустойчивость Н2О2 обусловлена непрочностью связи О - О.
Атомы кислорода в молекуле Н2О2 связаны непосредственно друг с другом неполярной ковалентной связью. Связи О - Н полярны. Поэтому молекула Н2О2 также полярна.
Пероксиды относят к классу солей. Как соли они могут вступать в реакцию обмена с кислотами:
ВаО 2 + Н 2 SO4 = BaSO4 ¯ + H2O2
в отличие от оксидов
SnO2 + 2H2SO4 = Sn(SO4)2 + 2H2O
Этой реакцией пользуются для различия оксидов и пероксидов.
 Н 0.95 А0 = 0,095нм
Н 0.95 А0 = 0,095нм
1,48 А0 = 0,148нм
120°
О О
95°
Н
ЕО-О = 210 кДж/моль ЕО-Н = 468 Дж/моль
Молекула нелинейна, две связи О - Н расположены не симметрично, а в 2-х плоскостях под углом 120°. Поэтому полярность mН2О2 > mН2О.
4. Окислительно-восстановительная двойственность Н2О2
Н2О2 + 2К I = I 2 + 2 KOH
окислитель восстановитель
Н 2 О 2 + Ag+2O = 2Ag0 + O2 + H2O
восстановитель окислитель
H2O2 + KMnO4 + H2SO4 → O2 + MnSO4 + K2SO4 + H2O
H2O2 + KI + H2SO4 → H2O + I2 + K2SO4
Na2O2 и K2O2 – используют для регенерации кислорода в подводных лодках и в изолирующих противогазах.
2Na2O2 + 2CO2 → 2Na2CO3 + O2↑
Наличие атомарного кислорода сообщает Н2О2 и Na2O2 сильные окислительные свойства. Na2O2 способен гидролизоваться с образованием H2O2 по реакции
Na2O2 + 2H2O = 2NaOH + H2O2
В связи с этим они находят применение для отбеливания шерсти, шелка, мехов.
Аптечная перекись водорода – 3% водный раствор Н2О2, применяется как дезинфицирующее средство, (30% раствор называется пергидроль).
|
из
5.00
|
Обсуждение в статье: Общая характеристика элементов I А группы. Особенности лития и его соединений. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы



