 |
Главная |
Расчет объема продуктов горения
|
из
5.00
|
V0co2= 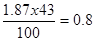
V0н2o= 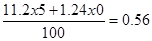
V0N2= 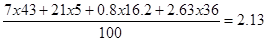
Так как коэфф. избытка воздуха (α>1), то рассчитаем объем избытка воздуха:
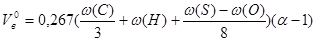 , м3 ,
, м3 ,
где 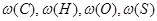 - массовые доли углерода, водорода, кислорода и серы в горючем веществе, %;
- массовые доли углерода, водорода, кислорода и серы в горючем веществе, %;
α - коэффициент избытка воздуха;
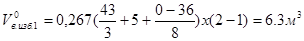 ;
;

Найдем общий объем продуктов горения:
Общий объём продуктов горения, выделяющихся при сгорании 1 кг вещества в нормальных условиях, определяем, суммируя объёмы компонентов продуктов горения:
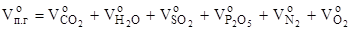 , м3,
, м3,
где: 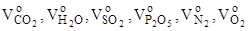 - объёмы образующихся при нормальных условиях газов: оксида углерода (IV), водяного пара, оксида серы (IV), оксида фосфора (V), азота и кислорода, м3.
- объёмы образующихся при нормальных условиях газов: оксида углерода (IV), водяного пара, оксида серы (IV), оксида фосфора (V), азота и кислорода, м3.
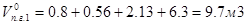
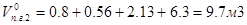
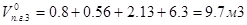
Пересчитываем общий объём продуктов горения на заданное количество вещества:
 , м3
, м3
а именно:


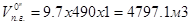
Находим объём продуктов горения при заданных условиях:
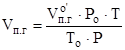 , м3
, м3
где: Vпг 0/ - объем продуктов горения, выделившейся при сгорании заданного количества вещества, м3;
Ро - давление при нормальных условиях, Па;
То - температура при нормальных условиях, К;
Р - заданное давление, Па;
Т - заданная температура, К.
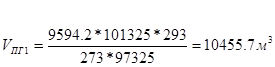
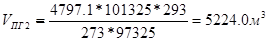
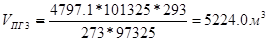
Рассчитаем объем компонентов п.г.:
Объём компонентов продуктов горения определяется по формулам:
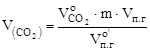 , м3;
, м3; 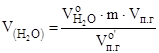 , м3 и т.д.
, м3 и т.д.
При нахождении процентного состава компонентов продуктов горения их общий объём 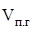 принимается за 100% и определяется из соотношения:
принимается за 100% и определяется из соотношения:
j 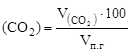 , %; j
, %; j 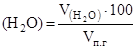 , % и т.д.
, % и т.д.
V(со2)1=0.8*490*10455.7/ 9594.2 = 427.1 м3;
V(со2)2=0.8*490*5224/ 4797.1 = 426.8 м3;
V(со2)3=0.8*490*5224/ 4797.1 = 426.8 м3;
V(Н2О)1 =0.56*490*10455.7/ 9594.2 =299 м3;
V(Н2О)2 =0.56*490*5224/ 4797.1 =298.8 м3;
V(Н2О)3 =0.56*490*5224/ 4797.1 =298.8 м3;
V( N2) 1=2.13*490*10455.7/ 9594.2 =1137.4 м3;
V( N2) 2=2.13*490*5224/ 4797.1 =1336.5 м3;
V( N2) 3=2.13*490*5224/ 4797.1 =1336.5 м3;
Рассчитаем процентный состав компонентов:
Ф(со2)1=427.1*100/10455.7= 4.0%
Ф(со2)2=426.8*100/5224= 8.1%
Ф(со2)3=426.8*100/5224= 8.1%
Ф(Н2О) 1=299*100/10455.7=2.8%
Ф(Н2О) 2=298.8*100/5224=5.7%
Ф(Н2О) 3=298.8*100/5224=5.7%
Ф(N2)1 =1137.4 *100/10455.7= 10.8%
Ф(N2)2 =1336.5 *100/5224= 25.5%
Ф(N2)3 =1336.5 *100/5224= 25.5%
4. Расчет теплового баланса процесса горения
Расчет низшей теплоты сгорания
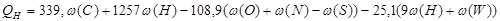 , кДж/кг
, кДж/кг
где 339,4; 1257; 108,9; 25,1; 9 - коэффициенты при углероде, водороде,
кислороде и т.д. - величины безразмерные;
 - массовые доли кислорода, водорода, азота,
- массовые доли кислорода, водорода, азота,
углерода и серы, %;
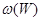 - массовая доля влаги в горючем веществе, %.
- массовая доля влаги в горючем веществе, %.
огнетушащий технический защита пожар
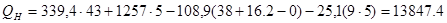 кДж/кг.
кДж/кг.
Расчет температуры горения
Qн = 13847.4 , кДж/кг
Qп.г.=Qн-Qнедож-Qп.из.=0.79хQн=0.79х 13847.4 =10939.4 , кДж/кг
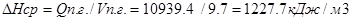
ТГ=1173 К
т.к. в смеси воздуха присутствует азот, то понижаем температуру на 100 градусов
ТГ=1073 К
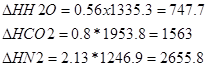 }
} 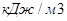
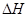 возд.=6.3*1108.2=6981.6
возд.=6.3*1108.2=6981.6
∑ Нср.=11948.1 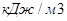 > Qп.г =10939.4 кДж/кг;
> Qп.г =10939.4 кДж/кг;
Понижаем на 100 градусов, получим:
ТГ=973 К
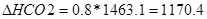
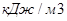
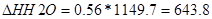
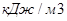
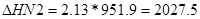
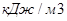
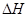 возд. =6.3*960.3=6049.8
возд. =6.3*960.3=6049.8 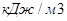
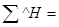 9891.5
9891.5 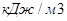 <Qп.г =10939.4 кДж/кг;
<Qп.г =10939.4 кДж/кг;
Методом интерполяции определяем ТГ:
11948.1 Дж/моль - 1073К
кДж/моль - ТГ
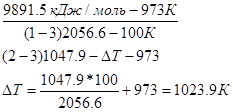
ТГ = 1023.9 К.
Расчет параметров развития пожара
Определение приведенной массовой скорости выгорания
По справочнику РТП стр.100
VМ1=0.35/60=0.0058 ,кг/(м2/с);
VМ2=0.35/60=0.0058 , кг/(м2/с);
VМ3=0.35/60=0.0058 , кг/(м2/с);
Расчет плотности теплового потока
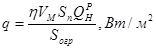
где η - коэффициент химического недожога, принимается по справочнику РТП стр.97
VM пр - массовая скорость выгорания, кг/(м2/с);
Sп - площадь пожара на определенный момент времени, м2;
QPH - низшая теплота сгорания, кДж/моль;
Sогр- площадь поверхности ограждающих конструкций, м2;
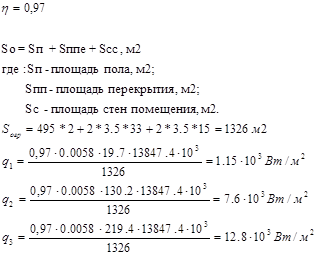
Определение температуры среды в помещении
По монограмме Рис.3 на стр. 16 М/У по полученным значениям q, α определяется температура среды в помещении на определенные, заданные моменты времени.
Т1 = 80 С=353К
Т2= 340 С=613К
Т3 = 410 С=683К
|
из
5.00
|
Обсуждение в статье: Расчет объема продуктов горения |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

