 |
Главная |
Буферные системы крови
|
из
5.00
|
Особенно большое значение буферные системы имеют в поддержании кислотно-основного равновесия организмов. Значение рН большей части внутриклеточных жидкостей находится в интервале от 6,8 до 7,8.
Кислотно – основное равновесие в крови человека обеспечивается гидрокарбонатной, фосфатной, белковой и гемоглобиновой буферными системами. Нормальное значение рН плазмы крови 7,40 ± 0,05.
Гемоглобиновая буфернаясистемана 35% обеспечивает буферную емкость крови:  . Оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин. Оксигемоглобин обычно бывает в виде калиевой соли.
. Оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин. Оксигемоглобин обычно бывает в виде калиевой соли.
Карбонатная буферная система:  по своей мощности занимает первое место. Она представлена угольной кислотой (Н2СО3) и бикарбонатом натрия или калия (NaНСО3, КНСО3) в пропорции 1/20. Бикарбонатный буфер широко используется для коррекции нарушений кислотно-основного состояния организма.
по своей мощности занимает первое место. Она представлена угольной кислотой (Н2СО3) и бикарбонатом натрия или калия (NaНСО3, КНСО3) в пропорции 1/20. Бикарбонатный буфер широко используется для коррекции нарушений кислотно-основного состояния организма.
Фосфатная буферная система  . Дигидрофосфатобладает свойствами слабой кислоты и взаимодействует с поступившими в кровь щелочными продуктами. Гидрофосфат имеет свойства слабой щелочи и вступает в реакцию с более сильными кислотами.
. Дигидрофосфатобладает свойствами слабой кислоты и взаимодействует с поступившими в кровь щелочными продуктами. Гидрофосфат имеет свойства слабой щелочи и вступает в реакцию с более сильными кислотами.
Белковая буферная системаосуществляет роль нейтрализации кислот и щелочей благодаря амфотерным свойствам: в кислой среде белки плазмы ведут себя как основания, в основной – как кислоты: 
Буферные системы имеются и в тканях, что способствует поддержанию рН тканей на относительно постоянном уровне. Главными буферами тканей являются белки и фосфаты. Поддержание рН осуществляется также с помощью легких и почек. Через легкие удаляется избыток углекислоты. Почки при ацидозе выделяют больше кислого одноосновного фосфата натрия, а при алкалозе – больше щелочных солей: двухосновного фосфата натрия и бикарбоната натрия.
Примеры решения задач
Пример 1.
Рассчитать рН буферного раствора, приготовленного смешением 10 мл 0,1М раствора уксусной кислоты и 100 мл 0,1М раствора ацетата натрия (рК(сн3 соон) =4,76).
Решение:
Рассчитываем рН кислотного буферного раствора по формуле 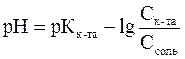 , тогда
, тогда 
Ответ: 5,76
Пример 2.
Рассчитать буферную емкость по кислоте, если на титрование 10 мл сыворотки крови пошло 5 мл 0,1 моль/л соляной кислоты, если при титровании рН изменился от 7,36 до 5,0.
Решение:
Рассчитываем буферную емкость по формуле: 

Ответ: 0,021 моль/л
Пример 3.
Буферный раствор состоит из 100 мл 0,1моль/л уксусной кислоты и 200 мл 0,2моль/л ацетата натрия. Как изменится рН этого раствора, если к ней добавить 30 мл 0,2моль/л раствора гидроксида натрия.
Решение:
Рассчитываем рН буферного раствора по формуле: 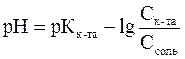

При добавлении к буферному раствору NaOH увеличивается количество соли и уменьшается количество кислоты в буферном растворе:
0,006 0,006 0,006
СH3COOH + NaOH = CH3COONa + H2O
Рассчитываем n(NaOH) = 0,03 л · 0,2 моль/л = 0,006 моль, следовательно в буферном растворе количество кислоты уменьшается на 0,006 моль, а количество соли увеличится на 0,006 моль. 
Рассчитываем рН раствора по формуле:

Отсюда: рН2 – рН1 = 5,82 – 5,3 = 0,52
Ответ: изменение рН буферного раствора = 0,52.
|
из
5.00
|
Обсуждение в статье: Буферные системы крови |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

