 |
Главная |
УЧАСТИЕ ОПИОИДНОЙ И ДОФАМИНОВОЙ СИСТЕМ МОЗГА В РЕАЛИЗАЦИИ СВОЙСТВ ЭТАНОЛА
|
из
5.00
|
Этиология и патогенез алкоголизма
Выполнила: Лушникова Е. И
Проверила: Пешкова Т. Я.
Астана, 2015г.
Содержание:
Этиология
- социальные факторы
- психологические факторы
- личностный подход к алкоголизму
- индивидуально-биологические факторы
Патогенез
- участие опиоидной и дофаминовой систем мозга в реализации аддиктивных свойств этанола
- окисление этанола в мозге
- влияние этанола на уровень нейропептидов в организме
Литература
Алкоголизм – это заболевание, вызванное частым употреблением спиртных напитков и характеризующееся появлением сильного пристрастия к алкоголю.
ЭТИОЛОГИЯ
Существует много различных взглядов на этиологию и патогенез алкоголизма. Многочисленные исследования показали сложность и многофакторность развития алкоголизма. Большинство авторов едино в одном: наряду с социальными, большое значение в развитии этой болезни имеют психологические и индивидуально-биологические факторы.
Выделяют следующие социальные факторы, предрасполагающие к развитию заболевания:
•отношение общества к употреблению спиртных напитков
•отношение к употреблению алкоголя господствующей в обществе религии (терпимое или запрещающее)
•алкогольная политика государства (доступность и уровень потребления)
•питейные традиции и обычаи
•этническая принадлежность
•семейное положение
•уровень образования и т.д.
Алкогольный стереотип поведения индивида определяет констелляция социальных факторов, включающих доступность алкоголя, алкогольные обычаи и влияние микросреды, формирующие установку на потребление спиртного, и границы дозволенного в приеме алкоголя.
Очень большое значение в развитии алкоголизма придается микросоциальной среде, наличию в ней определенного «алкогольного климата». Сложившиеся в семье и ближайшем окружении традиции и обычаи формируют не только отношение к употреблению алкоголя, но и в значительной мере формируют личность, делая ее в большей или меньшей степени подверженной риску развития алкоголизма.
Среди психологических факторов формирования алкоголизма отмечаются такие особенности личности, как:
•повышенная тревожность и внушаемость
•отсутствие стойких и серьезных интересов
•недостаточная способность к адаптации в обществе
•плохая переносимость физического и эмоционального напряжения
•заниженная самооценка
•гедонистические установки со стремлением к немедленному получению удовольствия
•отсутствие социально-позитивных установок
•сниженная способность противостоять стрессорным воздействиям
•сниженная способность умело разрешать конфликтные ситуации
•неумение организовать свой досуг и др.
Конкретные психологические механизмы алкоголизации различны при разных вариантах акцентуации и психопатии. У неустойчивых, гипертимных и истерических личностей прием спиртного – выражение общей тяги к удовольствиям, у психастеников – стремление к снижению тревоги и напряжения, у возбудимых – способ эмоциональной реакции на неприятности.
При этом имеют значение и преморбидные характерологические черты, которые не только определяют мотивацию отношения к алкоголю, но и влияют на скорость развития заболевания. В большинстве случаев личность страдающего алкоголизмом – незрелая, с недостаточной социальной адаптацией и затруднениями в установлении межличностных отношений. Наличие таких черт личности объясняют как наследственностью, так и дефектами воспитания. С целью компенсации своего состояния подобные личности часто прибегают к употреблению алкоголя или других психоактивных веществ.
Тот факт, что алкоголь способствует расслаблению, часто вызывает повышенное настроение, эйфорию, снимает эмоциональное напряжение, определяет мотивы приема спиртных напитков лицами с эмоциональной неустойчивостью, пониженными адаптационными возможностями.
Высказано предположение, что в основе формирования психической зависимости лежат нейрофизиологические сдвиги – патологическая активация определенных гипоталамических систем, получивших название «центр наслаждения». По мнению академика И.П.Анохиной, алкоголь влияет на катехоламиновую систему, прежде всего на дофаминовую медиацию в области локализации «центра наслаждения» (лимбическая система, стволовые образования мозга). Алкогольная интоксикация приводит к освобождению дофамина из депо, его избыточное количество скапливается в синаптической щели и обусловливает эйфоризирующий эффект.
Личностный подход к алкоголизмувключает в себя два аспекта - личностных черт алкоголика и личностного смысла алкоголизации.
Подход личностных черт предполагает, что одни типы личности более склонны к алкоголизации и/или заболеванию алкоголизмом, чем другие. Однако на основе личностных факторов оказалось крайне трудно предсказать чувствительность к патологическим эффектам действия алкоголя. Существует много перечней личностных черт, якобы образующих личностную предиспозицию к алкоголизму. То, как описывается личность алкоголика, во многом обусловлено социальной позицией врача по отношению к нему. Поэтому столь отличаются клинические описания алкоголиков - уличных бродяг или заключенных от описаний алкоголиков, самостоятельно обращающихся за помощью к частнопрактикующим врачам. Обнаруживающиеся же черты сходства, скорее всего, обусловлены постаддиктивными личностными изменениями. Следует отметить, что в нашей стране еще А.М. Рапопорт (1959) полагал неудачными попытки определить “конституцию” алкоголика и основные черты его “психологии”.
Личностный смысл алкоголизации впервые был изучен в десятилетнем цикле эмпирических исследований D.N. McCielland wiht nowork. (1972). Этот цикл включал следующие исследования:
•Эффекты мужского социального пьянства на фантазирование изучались в естественном окружении у студентов.
•Эффекты различных видов окружения на воздействие алкоголя, главным образом, на мысли о физическом сексе или агрессии, были изучены в ингибирующем и релаксирующем типах окружения. Тип окружения модифицировал воздействие алкоголя.
•Народные сказки и легенды изучались как представляющие коллективные фантазии. Методом контент-анализа было проанализировано по 10 сказок и легенд из 44-х культур. Здесь было показано, что алкоголизация - важная часть кластера действий, манифестирующих как потребность во власти.
•Влияние значения власти на пьянство мужчин из рабочего класса изучалось во время сессий алкоголизации в баре. Было выявлено, что чувства, связанные с властью, преципитируют желание алкоголизироваться.
•Алкоголизм в мексиканской деревне изучался в рамках психоаналитической традиции культуральной психиатрии.
•Исследовалось восприятие себя студентами-проблемными пьяницами.
•Была предпринята попытка помочь алкоголикам социализировать их потребность во власти.
Таким образом, первичный личностный смысл алкоголизации заключается в потребности во власти. Авторы указывают на ограниченные возможности генерализации названного вывода. Потребность во власти объясняет не более 25% вариации употребления алкоголя в популяции. Эта интерпретация не приложима к женщинам и к определенным социальным паттернам алкоголизации, например, к церемониальному пьянству. Сегодня наибольшее влияние эта концепция имеет на исследования кросс-культуральной ориентации.
Индивидуально-биологические факторыформирования зависимости от алкоголя прежде всего определяются наследственностью. Установлено, что риск развития алкоголизма у родственников первой степени родства в 7-15 раз выше, чем в популяции. Риск заболеть у однойцевых близнецов в 2,5 раза выше, чем у двуяйцевых; у взрослых детей мужского пола, родившихся от отцов-алкоголиков, риск заболевания алкоголизмом достигает 67%. Существуют целые народности с крайне низкой толерантностью к алкоголю. Считается, что наследуется не сам алкоголизм, а предрасположение к нему, высокий риск его развития, если начинается злоупотребление.
Несмотря на бесспорные доказательства роли генетического фактора, установить его вклад в развитие алкоголизма у всей популяции больных с зависимостью от алкоголя крайне сложно. Это связано с тем, что обычно обследуются больные в стационарах, у которых заболевание протекает неблагоприятно. Основная масса страдающих алкоголизмом за врачебной помощью не обращается в связи с хорошей адаптацией и относительно благоприятным течением заболевания. По-видимому, эти группы больных существенно различаются по влиянию средовых и генетических факторов на формирование алкоголизма.
Однако длительное употребление алкоголя хотя не всегда приводит к формированию алкоголизма. Иногда, напротив, короткий период злоупотребления спиртными напитками быстро приводит к формированию алкогольной зависимости. Эти общеизвестные факты свидетельствуют о значении биологических особенностей индивидуума, определенных физиологических и биохимических параметров в развитии патологических сдвигов в организме, определяющих болезненное влечение к алкоголю.
В настоящее время можно отметить несколько направлений в исследовании роли биологических факторов в развитии алкоголизма:
•Одним из важных показателей является скорость разрушения алкоголя в организме, которая контролируется главным образом ферментом алкогольдегидрогеназой (АДГ). Типы активности АДГ очень варьируют. Это обусловливает разную скорость разрушения и выведения алкоголя из организма, а также образование разного количества ацетальдегида - продукта метаболизма алкоголя, которому многие исследователи отводят важную роль в формировании заболевания.
•В ряде исследований предполагается, что изначальная склонность к алкоголю может определяться наследственной недостаточностью тиаминового обмена и обмена аминокислот. Большинство этих особенностей определяются наследственными факторами.
•В последние годы исследуется аминокислоты, являющиеся нейротрансмиттерами (ГАМК, глицин), и нейрогормоны (вазопрессин), играющие роль в поддержании толерантности к алкоголю.
Среди биологических факторов алкоголизма немаловажную роль играют:
•остаточные явления органического поражения центральной нервной системы
•задержки и отклонения в соматополовом созревании
•хронические и острые астенизирующие заболевания
•невротизация в детстве, а также раннее приобщение к некачественным крепким спиртным напиткам
Среди биологических факторов отмечалась роль эндокринной системы, соотношение секреции пролактина и тестостерона.
Рядом авторов изучалась проблема роли невротических состояний в патогенезе алкоголизма и взаимного влияния неврозов и хронической алкогольной интоксикации. При изучении психологических мотиваций злоупотребления алкоголем было установлено, что изменения личности, характерные для неврозов, могут служить стимулом для развития влечения к алкоголю. Существуют данные о том, что повышение содержания в головном мозге кинуренина связано с появлением тревоги и влечения к алкоголю. В развитии неврозов выделяют три группы факторов: определяющие, предрасполагающие и пусковые. Роль пускового фактора, как правило, играет эмоциональный стресс, который в свою очередь способствует развитию алкогольной мотивации. Также среди возможных пусковых факторов приводится интоксикационный. Смягчение острых невротических проявлений за счёт употребления алкоголя приводит к включению в невротические механизмы нового фактора с токсическим влиянием на мозг, что утяжеляет течение самого невроза. Таким образом, возникает порочный круг, возникновение невротических состояний способствует алкоголизации; в свою очередь алкоголизация ухудшает течение неврозов, а возможно и провоцирует их развитие.
Алкоголизм и депрессия. Сам механизм взаимосвязи депрессии и влечения к психоактивным веществам, в том числе и к алкоголю, исследователями описывается по-разному:
•в виде двух расстройств со своими патогенетическими механизмами
•в форме единого сложного симптомокомплекса
В пользу последнего варианта говорят результаты нейрохимических исследований, свидетельствующих о сходстве патогенетических механизмов депрессивных расстройств и синдрома патологического влечения. Собственно, стремление к изменению «актуального психического состояния», т. е. к эйфории, уже говорит об изначальном снижении у аддикта его эмоционального фона. Известно также, что подростки с нарушением поведения и в то же время обнаруживающие депрессивные расстройства, раньше начинают употреблять алкоголь, чем подростки с «изолированным» нарушением поведения, без депрессии.
Высокая степень корреляции аффективных и аддиктивных симптомов позволяет выделять факторы риска возникновения болезней зависимости. К ним можно отнести склонность к депрессиям, избыточную длительность аффективных реакций, циклотимию, состояния эмоционального напряжения, тревожные расстройства, «беспокойство, депрессию». Особую проблему представляют дистимии – незначительно выраженные, «субклинические» депрессии с невротическими и тревожными компонентами; эти состояния чаще других видов депрессивной патологии наблюдаются при алкоголизме.
ПАТОГЕНЕЗ
Известно, что возникновение алкоголизма и развитие обусловленной этим патологии связано со способностью организма адаптироваться к присутствию алкоголя и продуктам его метаболизма (ацетальдегиду и др.) и, при этом, "нормально" функционировать. Общебиологически алкоголизм является еще и следствием "инерционности" регуляторных процессов, участвующих в адаптационной перестройке структур организма: его рецепторов, ферментов, компонентов мембран и т.п., - объединенных в «элементарную токсикоманическую единицу», и со своей проекцией на уровне психики.
В условиях злоупотребления алкоголем на регуляторно-адаптационные механизмы контроля над активностью ферментов в крови накладываются эффекты алкогольной интоксикации. Среди патогенных процессов, способных существенно повлиять на регуляторные отношения, следует отметить: изменение проницаемости гисто-гематических барьеров вследствие усиления переокисления липидов мембран клеток; явления цитолиза и клеточного некроза, приводящие к непосредственному выходу тканевых ферментов в кровь.
1. Адаптационно-регуляторные механизмы гиперферментемии ГГТ и АСТ при алкоголизме 1 и 2 стадий.
Ранее нашими исследованиями было показано, что увеличение в сыворотке крови активности ГГТ в 1,5-3 раза при злоупотреблении алкоголем происходит уже в самом начале заболевания алкоголизмом, в его 1 стадии.
Активность других трансфераз, таких как АСТ и АЛТ, в начале заболевания остается в пределах нормы. А известно, что явления цитолиза, клеточного некроза всегда сопровождаются увеличением в крови активности не одного, а сразу целого ряда ферментов, в том числе и таких как АСТ и АЛТ.
Следовательно, правомерно предположить, что причиной увеличения ГГТ в начале алкоголизма являются метаболические процессы, а именно, адаптационно-регуляторный ответ организма на употребление алкоголя.
(Здесь и далее стадии алкоголизма нами рассматриваются в классификации, предложенной А.А. Портновым. В ее основу положен такой ведущий признак алкоголизма, как толерантность к алкоголю. И, как оказалось, это немаловажно, если в качестве цели иметь именно биохимические параллели в патогенезе алкоголизма).
Нашими же исследованиями было показано, что во 2 стадии алкоголизма, наряду с дальнейшим увеличением ГГТ в сыворотке крови (в 5-10 и более раз), начинает увеличиваться в крови и активность АСТ (в 1,5-2 раза), тогда как уровень АЛТ еще (или часто) остается в пределах границ нормы.
Следовательно, и гиперферментемию ГГТ и АСТ (во 2 стадии алкоголизма) также можно расценивать как результат дальнейшего усиления общеметаболического, адаптационно-регуляторного ответа организма на продолжающееся злоупотребление алкоголем (для 2 стадии характерно употребление алкоголя уже в максимально возможных количествах 19,20).
Конечно, на определенном этапе алкоголизма и цитолизный механизм сывороточной гиперферментемии может вносить свой вклад в общее увеличение уровня активности ферментов в крови. Скорее всего, это может происходить в 3 стадии алкоголизма, а также на этапе перехода 2 –3 стадия, для которых характерны и наиболее выраженная соматическая патология. Возможно именно поэтому в 3 стадии алкоголизма изменения активности трансфераз: ГГТ, АСТ и АЛТ, - в сыворотке крови, как было показано, утрачивают свою прежнюю закономерность. Хотя, имеющиеся в литературе данные свидетельствуют, что вклад этот вряд ли будет существенным. Так, специально проведенные исследования с параллельным сопоставлением активности различных ферментов в сыворотке крови и в биопсийных препаратах печени показали, что гиперферментемия АСТ и АЛТ часто наблюдается и в отсутствие некрозов в паренхиме печени.
Представление о преимущественно адаптационно-регуляторном характере гиперферментемий при алкоголизме (в его 1 и 2 стадиях) в принципе не противоречит и общей концепции механизмов гиперферментемий, сформулированной еще А.Ф. Блюгером 4, согласно которой гиперферментемия может быть обусловлена выходом ("просачиванием") ферментов из клеток различных органов и тканей при нарушении проницаемости клеточных мембран, но может быть обусловлена и усилением синтеза ферментов по принципу "обратной связи".
Сравнительно недавно, наконец, непосредственно в эксперименте было показано, что употребление этанола крысами в течение 12 недель вызывает именно индукцию активности ГГТ в плазматических мембранах гепатоцитов, опосредованную через увеличение синтеза в них м-РНК. Обнаружено и увеличение м-РНК для АСТ митохондриальных гепатоцитов людей, употребляющих алкоголь, при условии отсутствия у них цирроза печени.
С этих позиций рассмотренные нами в более ранней публикации механизмы увеличения ГГТ в сыворотке крови при алкоголизме (как адаптационно-регуляторное вовлечение межуточного обмена цистеин - глутатиона в "чрезмерный" алкоголь-липидный метаболизм), становятся более обоснованными.
2. Повышение уровня активности ГГТ в крови при алкоголизме – необходимое условие для обмена алкоголя.
Известно, что судьба алкоголя в организме в наибольшей степени связана с синтезом жирных кислот и липидов, опосредованным через ацетил-КоА - синтетазные реакции. Естественно, что алкоголь, употребляемый чрезмерно, чрезмерно же активизирует, нагружает и липидный обмен, и, в первую очередь, те его звенья, которые непосредственно участвуют в превращении и «депонировании» образующихся из алкоголя жирных кислот.
На фоне усиливающейся при этом скорости обмена ацетил-КоА происходит и жировая инфильтрация гепатоцитов. Факты усиленного обмена липидов при алкоголизме, жировая инфильтрация печени и другое, привели сегодня ряд исследователей к представлению, что механизм возникновения алкогольной патологии печени обусловлен, с одной стороны, “депонированием” жировых соединений в печени, а с другой, - химической агрессивностью ацетальдегида, проявляющейся, в усилении свободно-радикальных путей окисления липидов.
Ключевым соединением липидного обмена, как известно, является ацетил-КоА. Поэтому закономерно, что с увеличением употребления алкоголя одновременно растет активность и в зависящих от ацетил-КоА звеньях обмена. Увеличится и потребность в других их участниках, таких как: КоА, пантотеновая кислота, биотин, тиамин, ацилпереносящие белки, и др.
Как известно, в качестве реакционной группы кофермент КоА содержит сульфгидрильную группу. А активное состояние сульфгидрильных групп в организме поддерживается за счет их восстановительного обмена (оборота) с цистеином и глутатионом (GSH).
Непосредственная роль ГГТ в метаболизме GSH и цистеина, как и в поддержании их уровня в тканях, стала очевидной после того, как были обнаружены пациенты с недостаточной активностью ГГТ. Причем, в крови таких пациентов одновременно с низкой активностью ГГТ оказалась низкой и концентрация GSH (в сочетании с накоплением его и цистеина в моче). Цистеин, как известно, является одним из исходных субстратов в синтезе GSH. Но GSH необходим организму не только для восстановления реакционноспособности SH- групп кофермента КоА, но и для функционирования антиоксидантной глутатион-зависимой системы защиты от свободно-радикального окисления липидов. Причем, как недавно было показано на культуре изолированных гепатоцитов крыс, ГГТ может принимать и непосредственное участие в этих процессах. Да и в литературе уже неоднократно было показано, что этанол не только может вызывать истощение запасов восстановленного GSH в печени, но и снижать общую концентрацию тиоловых групп мембранных и цитоплазматических белков, например, клеток миокарда (эксперименты на крысах), а также уменьшать активность глутатионредуктазы.
Следовательно, ни само превращение этанола в организме, ни его "депонирование" в форме жирных кислот, ни работа систем защиты организма от переокисления липидов,- все это невозможно без поддержания в организме высокой уровня КоА. Не исключено, что важную роль в этом может играть и функционирование «системы» цистеин – глутатион - ГГТ.
Таким образом, все это дает нам основания предполагать, что повышение активности ГГТ при алкоголизме (1, 2 стадия) является, прежде всего, результатом необходимости обеспечения в организме условий «нормального» протекания обмена алкоголя (в условиях злоупотребления им). Конечно, совсем исключать на этапе 2-3, 3 стадии алкоголизма вклад в эти процессы и цитолиза, вряд ли было бы правильно.
3. Почему цистеин может предотвращать жировую инфильтрацию печени при алкоголизме.
Известно, что пищевой рацион злоупотребляющих алкоголем бывает достаточно ограничен. В случающиеся же периоды продолжительных выпивок может наблюдаться как временное исчезновение аппетита, так и полное отвращения к еде.
Отсюда, не без основания, можно предположить, что злоупотребление алкоголем обязательно будет сопровождаться и дефицитом аминокислот и, в первую очередь, - незаменимых аминокислот, например, таких как цистеин и метионин, которые непосредственно участвуют в процессах обмена липидов и алкоголя. Но так как резервным источником цистеина, как считается, может являться GSH 36, то в условиях злоупотребления алкоголем активизация оборота цистеина (за счет ресинтеза GSH, а также индуцируемого для этих целей фермента ГГТ), - будет одним из способов поддержания в организме на необходимом уровне скорости "взаимопревращений” и цистеина, и GSH, и кофермента КоА. Косвенно об этом свидетельствует, например, и такой факт. Измерение концентрации GSH и цистеина в эритроцитах хронических алкоголиков показывает, что при уменьшении GSH концентрация цистеина возрастает, тогда как парентеральное назначение S-аденозил-L-метионина (SAM) - вызывает в эритроцитах восстановление тиоловых групп.
Возможная схема путей активизации “цистеин-глутатионового” оборота в условиях злоупотребления алкоголем представлена нами на рис. 1.
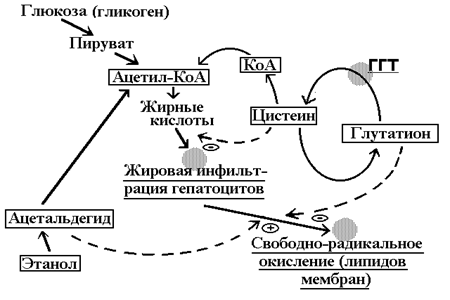
Pис. 1. Возможная схема путей активизации “цистеин-глутатионового” оборота при посредничестве гамма-глутамилтрансферазы (ГГТ) в условиях злоупотребления алкоголем
Сплошными стрелками указаны основные направления метаболических превращений; пунктирными - направление регуляторных воздействий и его характер: “+” - активирующий, “-” - тормозящий". Темными кружками отмечены ключевые, лимитирующие места в патогенезе алкоголизма.
На рисунке показано, как ГГТ, принимая участие непосредственно в обороте GSH и цистеина, может «противостоять» и жировой инфильтрации гепатоцитов, и свободно-радикальному окислению липидов мембран (показано пунктирными стрелками).
Небезынтересно в этой связи отметить, что характерное для алкоголизма накопление жира в печени, а не в жировых депо, происходит, например, и при белковом голодании, но также и при дефиците в рационе метионина (предшественника цистеина). В то же время показано, что цистеин, в условиях эксперимента по алкоголизации крыс, способен предотвращать ожирение печени. Эффективно противостоит токсическому эффекту алкоголя на печень и SAM, а также глицин, т.е. соединения, являющиеся участниками в синтезе глутатиона в организме.
Более того, на основе SAM разработан лекарственный препарат – адеметионин (гептрал, ФРГ), нашедший сегодня применение в лечении соматизированных депрессий, в гепатологии – как эффективное гепатопротективное средство, включая алкогольный гепатит, а в наркологии – как антидепрессант в остром периоде алкогольной абстиненции.
На основе другого естественно метаболита разработан лекарственный препарат – глицин (Россия), показавший, например, себя как эффективное нейропротективное средство в остром периоде ишемического инсульта, а в наркологии – как одно из средств профилактики алкогольной интоксикации.
Таким образом, становится понятно, почему именно адекватные алиментарные воздействия, включающие полноценный, животный белок, направленные на устранение белкового дефицита, а также витаминные назначения: тиамин (В1), фолиевая кислота, пиридоксин (В6), пантотеновая кислота (В3), цианкобаламин (В12) и др., - направленные на оптимизацию углеводного и жирового обменов злоупотребляющего алкоголем, - должны способствовать предотвращению процессов жирового и, следующего за этим - фиброзного перерождения печени. Витаминные препараты уместны, особенно, если учесть, что алкоголизм постоянно сопровождается различными гипо - и авитаминозами.
УЧАСТИЕ ОПИОИДНОЙ И ДОФАМИНОВОЙ СИСТЕМ МОЗГА В РЕАЛИЗАЦИИ СВОЙСТВ ЭТАНОЛА
Функции опиоидной системы в значительной степени определяются взаимодействием с други-
ми нейромедиаторными системами мозга. Опиоидные пептиды влияют на синтез, высвобождение и утилизацию ацетилхолина в ЦНС. Показано взаимодействие опиоидной системы с адренергической, с ГАМК-эргической и серотониновой системами. Но особенно тесно морфофункционально и анатомически опиоидная система мозга связана с дофаминовой.
Установлено, что опиоидные рецепторы локализованы на дофаминергичеких нейронах, а опиоидные пептиды обладают активирующим влиянием на обмен дофамина (ДА) и его высвобождение, причем влияние агонистов отдельных типов опиоидных рецепторов на высвобождение ДА в различных отделах мозга неодинаково. Предполагается, что активирующее действие m-опиоидных рецепторов на дофаминовую систему осуществляется через ингибирование ГАМК-ергических нейронов, которые тонически контролируют скорость высвобождения ДА. С другой стороны, показано увеличение уровня предшественников энкефалинов и мРНК, кодирующей их синтез, при длительной блокаде дофаминергической передачи, а также при разрушении нигростриального дофаминергического пути.
Дофаминовая система мозга представлена дофамином, продуктами его метаболизма, ферментами синтеза и деградации, а также дофаминовыми рецепторами различных типов. ДА синтезируется из аминокислоты тирозина, которая проникает ет из крови с помощью специального переносчика в дофаминергические клетки. Скорость синтеза ДА зависит от активности тирозингидроксилазы (КФ 1.14.16.2), которая контролируется множеством
сложных механизмов. ДА окисляется с помощью моноаминоксидазы (МАО, КФ 1.4.3.4) и катехол-О-метилтрансферазы (КОМТ, КФ 2.1.1.6).
Дофаминовые рецепторы представлены двумя основными типами - D1 и D2, которые подразделяются на подтипы. D1-рецепторы локализуются постсинаптически , имеют низкое сродство к ДА и агонистам и стимулируют аденилатциклазную активность, а D2-рецепторы локализуются как пресинаптически, так и постсинаптически, обладают высоким сродством к ДА и ингибируют аденилатциклазу. D1-рецепторы имеют D1 и D5 подтипы, а D2-рецепторы представлены D2, D3 и D4 подтипами, причем D3-рецепторам отводится роль ауторецепторов, регулирующих высвобождение и синтез ДА
Данные литературы о действии этанола на опиоидную систему противоречивы. Результаты ва-
рьируют в зависимости от применяемых схем вве дения этанола, изменения в содержании опиоидных пептидов в различных структурах мозга также неодинаковы. Некоторые авторы не выявили откло нений от контроля в уровне мет-энкефалина и лейэнкефалина в структурах мозга после однократного и длительного введения крысам этанола.
При хроническом введении этанола результаты также варьируют в зависимости от путей введе-
ния и концентрации этанола в крови животных, но практически во всех экспериментах наблюдали изменения в уровне опиоидных пептидов, что указывает на вмешательство этанола в процессы ихсинтеза и распада.
В отделах мозга действие этанола на пул биологически активных опиоидных пептидов осуще-
ствляется за счет разных механизмов. Главная дезинтегрирующая роль этанола на центральные энкефалинэргические системы мозга заключается,возможно, не в изменении содержания тех или иныхпептидов, а в сдвиге равновесия между ними идругими нейромедиаторами.
Неодинаковое содержание мет-энкефалина иикоэффициента отношения -эндорфин/мет-энкефалину у линейных мышей, отличающихся уровнем потребления этанола, дало основание авторам утверждать, что потребление этанола животными связано с дефицитом энкефалинэргических структур. Возможно, что при реализации наркотических эффектов этанола важное значение приобретает изменение соотношения уровней опиоидных пептидов между собой, что вызывает изменения функциональной активности опиоидных рецепторов
мозга.
Литература:
|
из
5.00
|
Обсуждение в статье: УЧАСТИЕ ОПИОИДНОЙ И ДОФАМИНОВОЙ СИСТЕМ МОЗГА В РЕАЛИЗАЦИИ СВОЙСТВ ЭТАНОЛА |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

