 |
Главная |
Стандартные электродные потенциалы
|
из
5.00
|
До сих пор рассматривались окислительно-восстановительные потенциалы отдельных реакций между двумя атомами редокс-пары, т.е. между двумя электродами. Эти величины не являются абсолютной мерой потенциала, и не позволяют сравнивать потенциалы отдельных атомов-электродов между собой. Для такого сравнения необходим один общий электрод сравнения, который бы играл роль стандартного. В качестве такого электрода был выбран стандартный электрод реакции восстановления водорода, которая имеет вид:
H+ + e-« 0,5H2.
Стандартный потенциал этой реакции E0H при парциальном давлении H2 1 атм и активности H+ 1 принят равным 0,00 В.
Любая окислительно-восстановительная реакция может быть представлена с участием водорода, как донора или акцептора электронов. Например, для реакции окисления железа,
Fe2+ → Fe3+ + e-,
необходим электрон, который может дать реакция восстановления водорода:
H+ + e- → 0,5H2.
Суммируя уравнения этих полуреакций, получим:
Fe2+ + H+ = Fe3+ + 0,5 H2.
Электрический потенциал такой реакции можно представить как сумму потенциалов двух полуреакций:
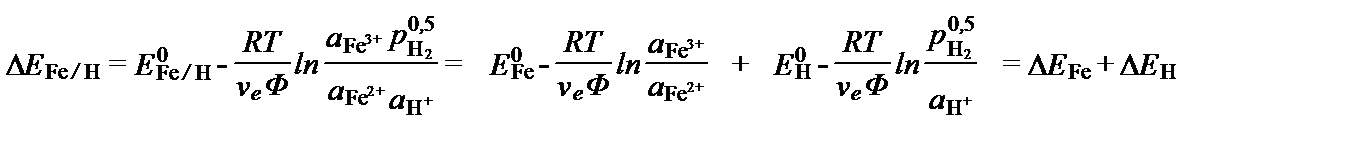 .
.
В этом уравнении ΔEFe/H – потенциал суммарной реакции, ΔEFe и 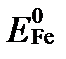 - реальный и стандартный потенциалы первой полуреакции, ΔEH и
- реальный и стандартный потенциалы первой полуреакции, ΔEH и 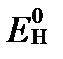 - реальный и стандартный потенциалы второй полуреакции.
- реальный и стандартный потенциалы второй полуреакции.
Из него следует, что электрический потенциал железа можно определять относительно потенциала водорода по уравнениям:
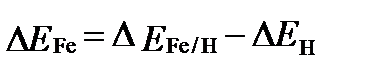 или
или 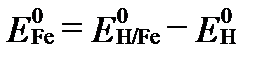 .
.
Аналогичным образом можно измерить электрические потенциалы всех атомов-электродов относительно 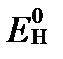 :
:
 .
.
Потенциал реакции, замеренный относительно стандартного водородного потенциала называют стандартным электродным потенциаломи обычно обозначают символом Ehj. Так как величина 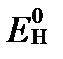 принята равной 0, величина
принята равной 0, величина 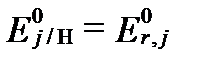 и также измеряется в вольтах или милливольтах.
и также измеряется в вольтах или милливольтах.
Направленность окислительно-восстановительных реакций с участием водорода определяют по характеру полуреакции водорода. Поэтому потенциал  считается окислительным, если водород отдает электроны, и восстановительным, если он их принимает. В большинстве стран, включая Россию, США и Канаду, в расчетах окислительные потенциалы используют чаще, чем восстановительные. Общее уравнение окислительного потенциала любой реакции имеет вид:
считается окислительным, если водород отдает электроны, и восстановительным, если он их принимает. В большинстве стран, включая Россию, США и Канаду, в расчетах окислительные потенциалы используют чаще, чем восстановительные. Общее уравнение окислительного потенциала любой реакции имеет вид:
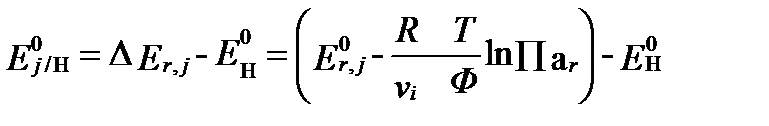 . (II‑166)
. (II‑166)
Поэтому равенство  = 0 не означает отсутствие заряда. Оно означает, что ∆Er,j =
= 0 не означает отсутствие заряда. Оно означает, что ∆Er,j = 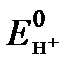 , т.е. что электрод нейтрален только относительно водородного электрода. Положительное значение
, т.е. что электрод нейтрален только относительно водородного электрода. Положительное значение  означает, что электрод имеет дефицит электронов относительно
означает, что электрод имеет дефицит электронов относительно 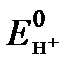 , т.е. является более сильным окислителем, чем водород. Отрицательное значение
, т.е. является более сильным окислителем, чем водород. Отрицательное значение  означает, что электрод содержит избыток электронов, в сравнении с
означает, что электрод содержит избыток электронов, в сравнении с 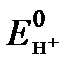 , и является более сильным, чем он, восстановителем.
, и является более сильным, чем он, восстановителем.
Рисунок II-16. Талица электродных потенциалов металлов.
| Метал | Ион | Электродный потенциал, вольты | Реакционная способность металов |
| K | K+ | -2,92 | Реагируют с водой |
| Na | Na+ | -2,71 | |
| Li | Li+ | -3,04 | |
| Sr | Sr2+ | -2,89 | |
| Ca | Ca2+ | -2,87 | |
| Mg | Mg2+ | -2,37 | Реагируют с кислотами |
| U | U3+ | -1,66 | |
| Al | Al3+ | -1,67 | |
| Zn | Zn2+ | -0,76 | |
| Cr | Cr2+ | -0,74 | |
| Fe | Fe2+ | -0,44 | |
| Cd | Cd2+ | -0,40 | |
| Co | Co2+ | -0,28 | |
| Ni | Ni2+ | -0,24 | |
| Sn | Sn2+ | -0,14 | |
| Pb | Pb2+ | -0,13 | |
| Fe | Fe3+ | -0,04 | |
| H2 | H+ | 0,00 | |
| Cu | Cu2+ | +0,34 | Могут реагировать с некоторыми сильно окисляющими кислотами |
| Ag | Ag+ | +0,80 | |
| Hg | Hg2+ | +0,85 | |
| Au | Au3+ | +1,50 | |
| Pt | Pt2+ | +1,19 |
Достоинство величин стандартного электродного потенциала в том, что они дают возможность сравнивать между собой потенциалы разных атомов-электродов, участвующих в окислительно-восстановительных реакциях.Их величины для конкретных реакций могут быть найдены в справочной литературе или рассчитаны.
В справочной литературе эти потенциалы всегда даются по отношению к потенциалу стандартного водородного электрода с указанием температуры (обычно 25oC). Для его расчета используется уравнение II-151. Для этого первоначально определяется величина свободной энтальпии реакции 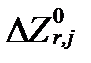 , согласно уравнению II-91. Методика расчета показана в примере II-5.
, согласно уравнению II-91. Методика расчета показана в примере II-5.
Пример II‑5.
Надо определить стандартную величину окислительно-восстановительного потенциала Fe2+.
Fe2+ + 2e-® Fe
Стандартная свободная энтальпия чистых веществ Fe и e- равна 0, а у Fe2+ имеет значения около –20,3 ккал/моль. Поэтому стандартная свободная энтальпия данной реакции равна 20,3 ккал/моль. Тогда
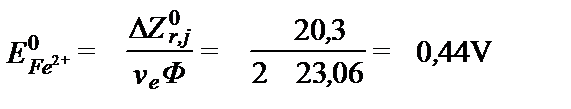
pe0= – 7,44
Величины стандартных электродных потенциалов, как и термодинамическая константа равновесия, зависят от температуры. Для оценки этого влияния воспользуемся уравнением II-97 и умножим его на соотношение 0,059/ve. Тогда это уравнение примет вид:
 (II‑167)
(II‑167)
Согласно уравнению II-151 это выражение можно переписать относительно стандартных электродных потенциалов:
 , (II‑168)
, (II‑168)
где  - стандартный электродный потенциал при температуре T, а
- стандартный электродный потенциал при температуре T, а  - изменение энтальпии при изменении температуры.
- изменение энтальпии при изменении температуры.
Стандартные электродные потенциалы металлов  , как правило, характеризуют реакции их окисления от нулевого заряда (Me0 = Men+ + ne ) при 25°С. Как видно из таблицы II-9, эти потенциалы металлов зависят от их положения в перидической таблице Д.И. Менеделеева и от величины их заряда. Металлы, расположенные в порядке возрастания их стандартных электродных потенциалов, образуют так называемый электрохимический ряд (electrochemical series of metal):Li→ Rb→ К→ Ва→ Sr→ Ca→ Na→ Mg→ Al→ Mn→ Zn→ Cr→ Fe→ Cd→ Co→ Ni→ Sn→ Pb→ H→ Sb→ Bi→ Cu→ Hg→ Ag→ Pd→ Pt→ Au. Этот рядхарактеризует электрохимические свойства металлов:
, как правило, характеризуют реакции их окисления от нулевого заряда (Me0 = Men+ + ne ) при 25°С. Как видно из таблицы II-9, эти потенциалы металлов зависят от их положения в перидической таблице Д.И. Менеделеева и от величины их заряда. Металлы, расположенные в порядке возрастания их стандартных электродных потенциалов, образуют так называемый электрохимический ряд (electrochemical series of metal):Li→ Rb→ К→ Ва→ Sr→ Ca→ Na→ Mg→ Al→ Mn→ Zn→ Cr→ Fe→ Cd→ Co→ Ni→ Sn→ Pb→ H→ Sb→ Bi→ Cu→ Hg→ Ag→ Pd→ Pt→ Au. Этот рядхарактеризует электрохимические свойства металлов:
1. Чем больше отрицательный электродный потенциал металла, тем больше его восстановительная способность.
2. Каждый металл способен вытеснять (восстанавливать) из растворов соли тех металлов, которые стоят в электрохимическом ряду напряжений металлов правее (в таблице II-9 ниже) его.
3. Все металлы, имеющие отрицательный стандартный электродный потенциал, т. е. находящиеся в электрохимическом ряду напряжений металлов левее (в таблице II-9 выше) водорода, способны вытеснять H+ из растворов кислот.
|
из
5.00
|
Обсуждение в статье: Стандартные электродные потенциалы |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

