 |
Главная |
Оборудование для термического окисления
|
из
5.00
|
Термическое окисление кремния
· Оборудование для роста окисных пленок
· Модель Дила-Гроува
· Зависимость толщины окисла от времени окисления
· Особенности роста тонких и толстых слоев окисла
· Свойства термических пленок двуокиси кремния
Оборудование для термического окисления.
Слой двуокиси кремния формируется обычно на кремниевой пластине за счет химического взаимодействия в приповерхностной области полупроводника атомов кремния и кислорода. Кислород содержится в окислительной среде, с которой контактирует поверхность кремниевой подложки, нагретой в печи до температуры T = 900 - 1200 ºС. Окислительной средой может быть сухой или влажный кислород. Схематично вид установки показан на рис. 1 (в современных установках пластины в подложкодержателе располагаются вертикально).
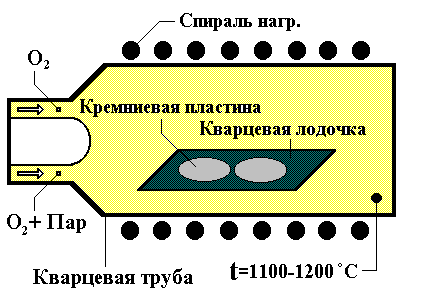
Требования к оборудованию:
· контролируемая с точностью до 1 градуса температура подложкодержателя,
· обеспечение плавного повышения и понижения температуры в реакторе (двухстадийный нагрев),
· отсутствие посторонних частиц в реакторе (подложкодержатель сначала вводится в трубу реактора, а затем опускается на дно),
· отсутствие посторонних примесей, в частности, ионов натрия на внутренней поверхности реактора (с целью их удаления проводится предварительная продувка трубы реактора хлором),
· обеспечение введения кремниевых пластин в реактор сразу после их химической очистки.
Химическая реакция,
идущая на поверхности кремниевой пластины, соответствует одному из следующих уравнений:
· окисление в атмосфере сухого кислорода (сухое окисление): Siтверд.+ O2 = SiO2;
· окисление в парах воды (влажное окисление): Siтверд.+2H2O = SiO2 + 2H2;
· термическое окисление в присутствии хлора (хлорное окисление);
· термическое окисление при взаимодействии молекул воды, синтезированных из атомарно чистых кислорода и водорода непосредственно у поверхности кремния, с атомами кремния (пирогенное окисление).
Время окисления в стандартных технологических процессах составляет 4 - 5 часов.
Значительным достижением в совершенствовании технологии окисления кремния явилось добавление в окислительную среду в процессе окисления хлорсодержащих компонентов. Это привело к улучшению стабильности порогового напряжения полевых МДП транзисторов, увеличению напряжения пробоя диэлектриков и повышению скорости окисления кремния. Главная роль хлора в пленках двуокиси кремния (обычно с концентрацией хлора 1016- 1020 см-3) заключается в превращении случайно проникших в SiO2 примесных ионов натрия или калия в электрически неактивные.
МодельДила-Гроува.
Методом радиоактивного маркера показано, что рост SiO2 происходит за счет диффузии кислорода к поверхности кремния. Выход SiO2 за границы 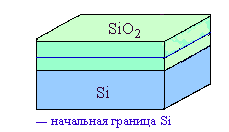 начального объема, занимаемого кремнием, обусловлен их разными плотностями.
начального объема, занимаемого кремнием, обусловлен их разными плотностями.
Для теоретического обоснования было предложено множество моделей, основанных на объемной диффузии заряженных частиц или нейтральных пар, а также эффектах туннелирования электронов, кинетике адсорбции, образования пространственного заряда, изменении граничных концентраций диффундирующих частиц в зависимости от толщины пленки и многих других.
К сожалению, ни один из указанных механизмов не способен полностью объяснить обширный класс имеющихся к настоящему времени экспериментальных данных. Что касается получения пленок двуокиси кремния, то кинетику ее роста в широком диапазоне толщин SiO2 можно объяснить, исходя из достаточно простой модели Дила-Гроува(см. рис. 2).
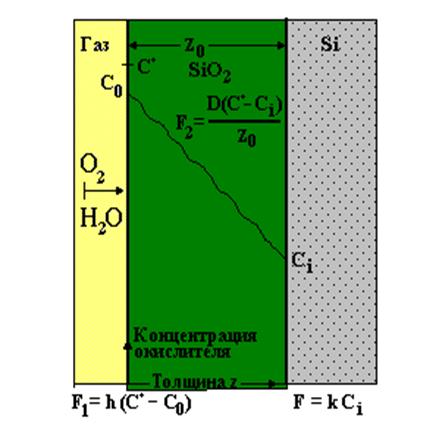
Процесс окисления происходит на границе Si - SiO2, поэтому молекулы окислителя диффундируют через все предварительно сформированные слои окисла и лишь затем вступают в реакцию с кремнием на его границе. Согласно закону Генри, равновесная концентрация твердой фазы прямо пропорциональна парциальному давлению газа P:
C* = HP, где
C*- максимальная концентрация окислителя в газе для данного значения давления P,
H - постоянный коэффициент Генри.
В неравновесном случае концентрация окислителя на поверхности твердого тела меньше, чем C*.
Поток F1 определяется разностью между максимальной и реальной поверхностной концентраций окислителя:
F1 = h(C* - C0), где
C0 - поверхностная концентрация окислителя, h - коэффициент переноса.
Значение концентрации окислителя C0 зависит от температуры, скорости газового потока и растворимости окислителя в SiO2.
Для того чтобы определить скорость роста окисла, рассмотрим потоки окислителя в объеме окисла F2 и на его границе с кремнием F3. Согласно закону Фика, поток через объем окисла определяется градиентом концентрации окислителя:
F2 = - D(dC/dz) = D(C0 - Ci)/z0, (1)
где Ci - концентрация окислителя в молекулах на кубический сантиметр при z = z0,
D - коэффициент диффузии при данной температуре, z0 - толщина окисла.
Величина потока F3 на границе окисла с полупроводником зависит от постоянной K скорости поверхностной реакции и определяется как:
F3= kCi (2)
При стационарных условиях эти потоки равны, так что F3 = F2 = F1 = F.Следовательно, приравняв соотношения (1) и (2), можно выразить величины Ci и C0 через C*:
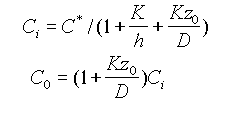 (3)
(3)
Для того чтобы определить скорость роста окисла, представим поток F3 как изменение числа молекул в слое dz0 за время dt. Тогда уравнение потока на границе SiO2 - Si будет иметь следующий вид:
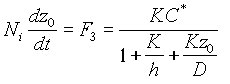 (4)
(4)
Скорость роста окисла определяется потоком F3 и количеством молекул окислителя Ni , входящих в единичный объем окисла. Поскольку концентрация молекул SiO2 в окисле равна 2.2*1022 см-3, то для получения двуокиси кремния требуется такая же концентрация молекул кислорода или в два раза большая концентрация молекул воды.
Соотношение между величинами z0 и t определяется интегралом вида

Зависимость толщины окисла от времени окисления.
Следовательно, для малых времен окисления толщина окисла определяется постоянной скорости поверхностной реакции K и прямо пропорциональна времени окисления (8). Для больших времен  окисления скорость роста зависит от постоянной диффузии D (9), а толщина окисла пропорциональна корню квадратному из времени процесса.
окисления скорость роста зависит от постоянной диффузии D (9), а толщина окисла пропорциональна корню квадратному из времени процесса.
На скорость окисления влияют также ориентация подложки, присутствие паров воды, наличие натрия, хлора и концентрация легирующей примеси в кремнии. На рис. 3 приведена зависимость толщины пленки SiO2 от времени окисления во влажном кислороде при парциальном давлении паров воды 85*103 Па.
Для широкого класса полупроводников и металлов кинетика процесса активного окисления характеризуется в равновесии линейным законом, то в случае пассивного окисления физическая картина процесса усложняется процессом переноса реагента к реакционной поверхности раздела сквозь растущую пленку. При этом кинетика окисления может быть аппроксимирована следующими законами:
· линейным Х(т) = К1*т; (1)
· параболическим Х2(т) = К2*т; (2)
· кубическим Х3(т) = К3*т; (3)
· логарифмическим Х(т) = К4*lg(В*т+ 1); (5)
· обратно логарифмическим K5/X(т) = А - lg(т) (6)
Существование каждого из этих законов определяется условиями проведения процесса окисления и свойствами исходного материала. Константы К1- К5 зависят от температуры, давления реагента и природы окисляемого материала.
Зависимость экспериментально наблюдаемых кинетических закономерностей от температуры процесса приведена в Таблице 1.
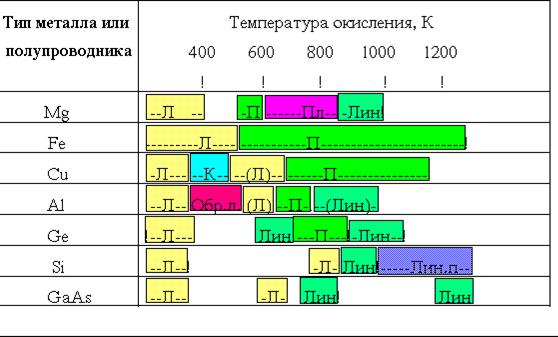
Особенности роста тонких и толстых пленок двуокиси кремния.
Отметим, что в микроэлектронике наиболее часто используются окислы кремния толщиной в несколько десятых долей микрона а верхний предел по толщине для обычного термического окисления составляет 1 - 2 мкм. В технологии СБИС используются также как более тонкие, так и более толстые пленки SiO2.
Одним из приборов, в которых используются сверхтонкие слои двуокиси кремния толщиной 2 - 5 нм являются энергонезависимые элементы памяти. Обычно для этих целей в применяется многослойная структура металл - нитрид кремния - двуокись кремния - кремний (МНОП транзистор). SiO2 в данной системе позволяет произвести контролируемую инжекцию заряда в нитрид кремния при подаче высокого потенциала на затвор транзистора (цикл записи или стирания информации) и препятствует растеканию этого заряда в отсутствии потенциала на затворе (хранение информации).
По мере повышения степени интеграции ИС становится необходимым получение пленок подзатворного диэлектрика с хорошо контролируемыми параметрами толщиной 20-50 нм. В ряде случаев необходимо иметь качественные пленки SiO2 толщиной 5 - 100 нм под маскирующими слоями нитрида кремния для предотвращения появления дефектов в кремниевой подложке, обусловленных наличием механических напряжений.
Обычно для получения воспроизводимых по свойствам пленок в реакторах атмосферного давления подбирают соответствующие температурно-временные условия (см. рис. 4). Однако необходимо учитывать, что для пассивирования ионов натрия хлором, вводимым в пленку в процессе окисления, требуются достаточно высокие температуры окисления. Плотность окисла и концентрация дефектов в кремнии также определяются температурой. Часто применяется двухстадийный процесс сухого окисления кремния, состоящий из окисления с добавлением HCl при средних температурах (около 1000 ºС), с последующей термообработкой в атмосфере O2, N2 и HCl при температуре 1150 ºС.
Для получения высокооднородных пленок SiO2 с воспроизводимыми свойствами используют также реакторы пониженного давления (РПД реакторы). Окисление, проводимое в РПД, позволяет синтезировать тонкие слои SiO2 с точностью до нескольких ангстрем. Температура окисления T = 900 - 1000 ºС, давление P = 30 - 300 Па. Окислы гомогенны, аналогичны окислам, полученным в реакторах атмосферного давления, напряженность электрического пробоя пленок E = 10 - 13 МВ/см. Толщина синтезируемых в РПД пленок составляет 2 - 14 нм.
Еще одним способом, используемым для производства тонких пленок SiO2, является их получение во влажной атмосфере, но при пониженной температуре (T = 750 ºС) и атмосферном давлении (P = 1 МПа).
Толстые окисные пленки получают, как правило, во влажной атмосфере при повышенном давлении. По своим свойствам они более пористые, имеют меньшие значения напряженности пробоя. Такие пленки используются в биполярной технологии для создания окисной изоляции и в МОП технологии - для выращивания толстых изолирующих слоев. Верхний предел по толщине для термического окисления составляет 1-2 мкм. Пленку такой толщины получают при давлении 2*106 Па при окислении в парах воды и температуре 900 ºС в течение 1 - 2 часов.
Свойства пленок SiO2
Основными контролируемыми параметрами пленок являются: коэффициент преломления, химический состав пленки, пористость, плотность, скорость травления, напряженность поля пробоя. Значения некоторых типичных характеристик термических пленок SiO2 приведены в
Таблице 2.
| Параметр | Значение параметра |
| Плотность, г/см3 | 2.2 |
| Показатель преломления | 1.46 |
| Диэлектрическая постоянная | 3.82 |
| Ширина запрещенной зоны, эВ | 8.9 |
| Удельное сопротивление постоянному току при T = 25 ºС, Ом*см | 1014-1016 |
| Скорость травления в буферном растворе HF, нм/мин | |
| Линия ИК поглощения, мкм | 9.3 |
| Коэффициент теплового расширения, С-1 | 5*10-7 |
| Механические напряжения в окисле, дин/см2 | 3*109 |
|
из
5.00
|
Обсуждение в статье: Оборудование для термического окисления |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

