 |
Главная |
Расчет рабочей массы топлива
|
из
5.00
|
ЗАДАНИЕ НА РАСЧЕТНО-ГРАФИЧЕСКУЮ РАБОТУ
| Тема: | Тепловой и аэродинамический расчёт методической толкательной печи с вращающимся подом |
| Студенту | Березанской К.А. |
Исходные данные:
| № варианта | СОСТАВ СУХОГО ГАЗА, объемные % | Коэф-ент расхода воздуха,n | Температура подогрева воздуха,0С | ||||||||||
| СО2 | СО | Н2 | СН4 | С2Н6 | С3Н8 | С4Н10 | Н2S | О2 | N2 | ||||
| 5,5 | 20,2 | 0,2 | 0,2 | 15,9 | 1,1 |
| Марка стали | Размер заготовки, δxbxl,мм | 
| Р, т/ч | dв, г/м3 | dг, г/м3 | tме, 0С | Тип печи |
| Ст.40 | D300х800 | МВР |
| Руководитель: | Сеничкин Б.К. | |
| Задание получил: | Березанская К.А. |
Магнитогорск, 2014
Расчет горения топлива
Расчет рабочей массы топлива
Рассчитать расход воздуха, количество и состав продуктов горения природного газа следующего состава:
Влагосодержание сухого газа dГ = 15 г/м3, температура tВ = 30°С.
Пересчет состава сухого газа на влажный проводится по формулам:
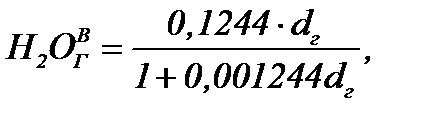 =1,832%
=1,832%
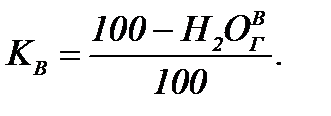 =0,982%
=0,982%
Аналогично рассчитываем:
CO2 =5,5*0,982=5,401%;
CO=28*0,982=27,496%;
H2=30*0,982=29,46%;
CH4=20,2*0,982=19,8364%;
N2=15,9*0,982=15,6138%;
H2S=0,2*0,982=0,1964%;
O2=0,2*0,982=0,1964%.
1.2. Теплота сгорания топлива
В практических расчетах обычно пользуются величиной  , поскольку в тепловых устройствах пары воды, содержащиеся в продуктах горения, удаляются из рабочего пространства в газообразном состоянии.
, поскольку в тепловых устройствах пары воды, содержащиеся в продуктах горения, удаляются из рабочего пространства в газообразном состоянии.
Низшая теплота сгорания газового топлива определяется как сумма тепловых эффектов реакции горения каждого компонента, содержащегося в одном кубическом метре топлива:
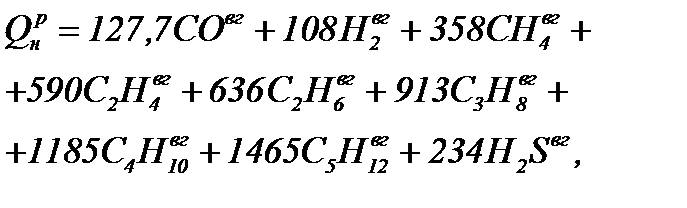
Q = 127,7*27,496+108*29,46+358*19,8364+234*0,1964=3511,2392+3181,68+7101,4312+45,9576=13840,308 кДж/кг
1.3. Определение расхода воздуха
Количество окислителя (кислорода), необходимого для полного горения единицы топлива, определяется на основе стехиометрических соотношений горючих компонентов и окислителя. Рассчитанное количество окислителя по стехиометрическим уравнениям представляет собой теоретически необходимое количество кислорода (Vо2) для полного сжигания единицы топлива до СО2 и Н2О.
Для сжигания 1 м3 газового топлива требуется кислорода
Vo2= 0.01· [0.5(H2+CO) + Σ (m + n/4) ·2Cm Hn ]=[0,01(0,5(27,496+29,46)+(3*0,1964)]= =0,01(28,7726+39,4764)=0,68249 %
В атмосферном воздухе содержится 79% N2 и 21% O2. Таким образом, азота по объему в 79/21 = 3,762 раза больше, чем кислорода. Учитывая это, теоретически необходимый расход атмосферного воздуха (Lo) можно определить из выражения
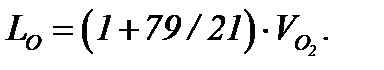 =(1+3,762)0,68249=3,24995 м3/ м3
=(1+3,762)0,68249=3,24995 м3/ м3
Принимаем, что газ сжигается горелками внешнего смешивания . Тогда коэффициент расхода воздуха принимаем равным n = 1,1. Фактический расход воздуха Ln составит
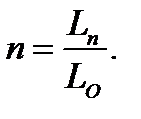
Ln=n*Lo=1,1*3,24995=3,57495м/м3
1.4. Определение выхода и состава продуктов горения
Количество составляющих продуктов горения топлива рассчитывается в соответствии с формулами
VRO2= 0,01( CO+ H2+Σm CmHn)= 0,01[5,401+0,1964+27,496+(1*19,8364)]=0,5293%
VH2O= 0,01(H2O+ H2+Σn/2 CmHn)+0,001244dBLn=0,01[1,832+29,46+0,1964+(2*19,8364) +0,001244*32*3,57495= 0,85392161%
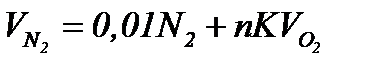 =0,01*15,6138+1.1*3,76*0,68249=2,97892%
=0,01*15,6138+1.1*3,76*0,68249=2,97892%
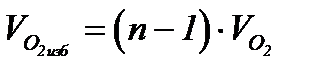 =(1,1-1)0,68249=0,06825%
=(1,1-1)0,68249=0,06825%
Объем продуктов полного горения единицы топлива представляет собой сумму всех четырех составляющих
Vn = VRO2 + VN2 + VH2O +VO2изб =0,5293+0,85392161+2,97892+0,06825=4,43039161%
Состав продуктов горения определяется как отношение содержания каждого компонента к объему продуктов полного горения единицы топлива, выраженное в процентах:
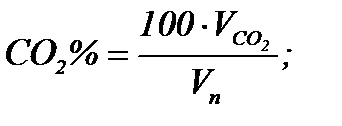
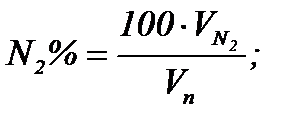
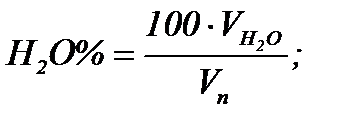

Состав влажных продуктов горения определяется по формуле :
CO2=11,94%
N2= 67,23%
H2O= 19,27%
O2изб= 1,54%
Плотность рассчитывается по правилу аддитивности в соответствии с составом продуктов горения
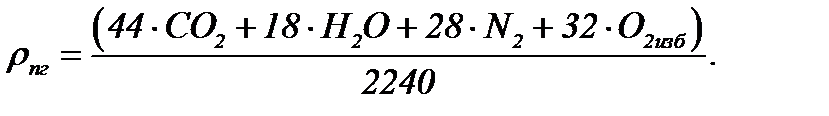 =1,25кг/м3
=1,25кг/м3
Исходя из величины общей теплоты продуктов горения, отнесенного к 1м3 их объема iобщ, тогда:
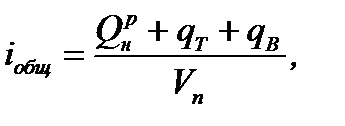
где qB, qT - физическая теплота подогретых, соответственно,
воздуха и топлива.
Расчет физической теплоты, вносимой влажным воздухом, расходуемым на окисление единицы топлива, проводится по формуле (20). Данная величина определяется по фактическому расходу Ln, энтальпии при соответствующей температуре его подогрева iB и влажности dB
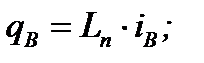
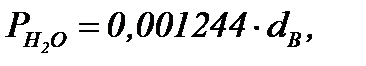 =0,039808%
=0,039808%
tB =400°
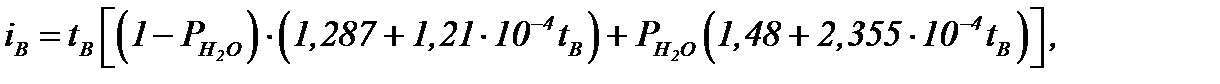 = 537,9624602кДж/м3
= 537,9624602кДж/м3
При нагреве газа свыше 500°С расчет физической теплоты газа qТ может быть выполнен по выражению
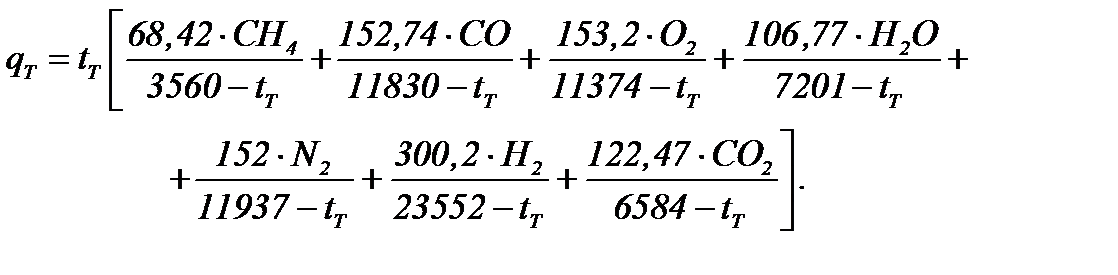
qT =1788,054кДж/кг
Теплота, вносимая в зону горения твердым и жидким топливом, весьма мала и ею можно пренебречь.
Содержание свободного воздуха в продуктах горения при n = 1,1 составит
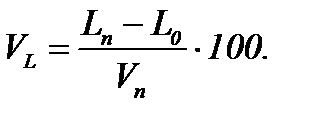 =7,335694643%
=7,335694643%
Рассчитать теоретическую температуру горения Тт, в зависимости от сорта топлива, можно по формулам:
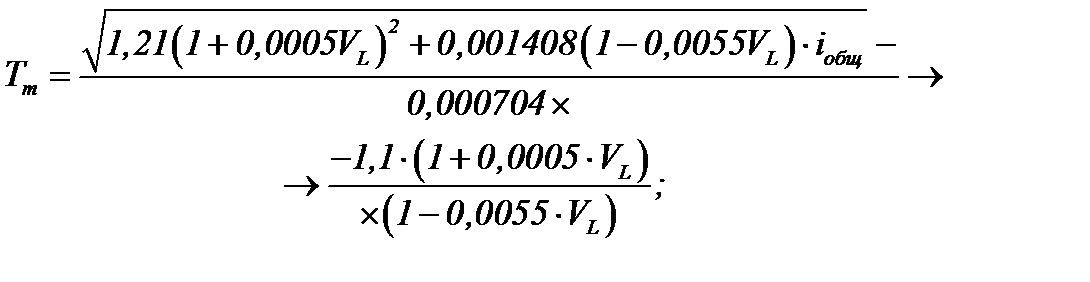
Tm=1999,501295K
По it–диаграмме, при i = 3767,68 кДж/м3 и tTa = 1474,75°C.
Время нагрева металла
Температуру уходящих из печи дымовых газов принимаем равной tух=1050°С; температуру печи в томильной зоне на 50° выше температуры нагрева металла, т.е. 1300°С. Распределение температур по длине печи представлено на рис. 1
Поскольку основным назначением методической зоны является медленный нагрев металла до состояния пластичности, то температура в центре металла при переходе из методической в сварочную зону должна быть порядка 400-500°С.
Разность температур между поверхностью и серединой заготовки для методической зоны печей прокатного производства можно принять (формула 88) равной (700-800) S, где S- прогреваемая (расчетная) толщина. В рассматриваемом случае двухстороннего нагрева S=0,55S=0.6·0.1=0,066 м. и, следовательно, ∆t=700·0,055=38,5°С, т.е. следует принять температуру поверхности сляба в конце методической зоны равной 500°С.
Определим ориентировочные размеры печи. При однорядном расположении заготовок ширина печи будет равна
Bпечи=L+2α=3+4·0,2=3,8 м.
Здесь α=0,2 м – зазоры между слябами и стенками печи.
В соответствии с рекомендациями высоту печи принимаем равной: в томильной зоне 1,4 м, в сварочной 1,4 м, в методической 1,4 м.
Находим степени развития кладки (на 1 м длины печи) для:
Методической зоны ωм = (2·1,4+3,8)/0,8=8,25;
Сварочной зоны ωм = (2·1,4+3,8)/0,8=8,25;
Томильной зоны ωм = (2·1,4+3,8)/0,8=8,25.
Определим эффективную длину луча, м:
Sэф=(4*h*B)/(2*h+2*B)=1,2
|
из
5.00
|
Обсуждение в статье: Расчет рабочей массы топлива |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

