 |
Главная |
Обратимые и необратимые по направлению реакции. Понятия о химическом равновесии. Принцип Ле-Шателье
|
из
5.00
|
Состояние реагирующих веществ, при котором скорость прямой реакции равна скорости обратной реакции называется состоянием химического равновесия. Состояние химичесчкого равновесия характеризуется константой равновесия K. Так, для реакции H2+I2=2HI
K= 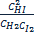
Для обратимой реакции
V1=K1[A]a[B]b
V2=K2[C]c[D]d
В 1884г. Французский ученый Ле-Шателье сформулировал принцип подвижного равновесия: при изменении каких-либо параметров системы, находящейся в химическом равновесии, происходит смещение его в направлении, при котором уменьшается влияние этого изменения.
Химическая кинетика, как основа для изучения скоростей и механизма биохимических процессов. Средняя скорость реакции.
Кинетика-наука, изучающая механизм и закономерности протекания химических реакций. В хим.кинетике используется графический метод изображения функциональных зависимостей.
A→B
(график)
Vср.= 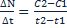 потому что скорость реакции не может быть отрицательной Vср.=-
потому что скорость реакции не может быть отрицательной Vср.=-  поэтому пишем Vср.=
поэтому пишем Vср.=  =
= 
Скоростью химической реакции называется изменение концентрации реагирующих веществ в единицу времени.
Vср.=lim(  )
)  →0=
→0= 
 =tgα
=tgα
Закон действующих масс. Константа скорости реакции. Зависимость скорости реакции от концентрации.
Кинетика базируется на законе действующих масс: скорость химической реакции пропорциональна произведению концентраций реагентов в степенях, равных стехиометрическим коэффициентам в уравнении реакции.
V=kCA1V1CA2V2CA3V3
Например:
N2+3H2=2NH3
Vпр.=k1[N2][H2]3
Vобр.=k2[NH3]2
По закону действующих масс можно рассчитать скорость реакции в данный момент времени.
C+O2 V=K[O2]
При увеличении концентрации реагирующих веществ и давления, скорость увеличивается.
Молекулярность и порядок реакции. Лимитирующая стадия процесса.
Молекулярностью реакции считается число молекул, участвующих в элементарном акте химического взаимодействия. Они делятся на:
Мономолекулярные I2=2I
Бимолекулярные H2+Cl2=2HCl
Тримолекулярные 2NO+O2=2NO2
Порядок реакции определяется суммой степеней входящих в закон действующих масс для определения скорости этой реакции.
H2+Cl2=2HCl
V=K[H2][Cl] V1=1+1=2
Если реакция осуществляется путем последовательно протекающих стадий (не обязательно все из них являются химическими) и одна из этих стадий требует значительно большего времени, чем остальные, то есть идет намного медленнее, то такая стадия называется лимитирующей. Именно эта самая медленная стадия определяет скорость всего процесса.
|
из
5.00
|
Обсуждение в статье: Обратимые и необратимые по направлению реакции. Понятия о химическом равновесии. Принцип Ле-Шателье |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

