 |
Главная |
Фазовые диаграммы систем Mn - O и Si - O
|
из
5.00
|
Фазовая диаграмма состояния системы Si-O
Диаграмма состояния O-Si построена в интервале концентраций 0-66,7 % (ат.) О на основе обобщения литературных данных. В системе существует обширная область расслаивания в жидком состоянии. Температура монотектической реакции отвечает 1703°С. При 1417°С происходит кристаллизация эвтектики Si + SiO2 (тридимит). Как следует из диаграммы, в системе образуется одна устойчивая оксидная фаза - SiO2 (кремнезем). Никаких других промежуточных фаз, кроме SiO2, в системе не обнаружено.
Растворимость кислорода в твердом Si была определена с помощью метода ИК-спектроскопии и представлена ниже:
| Температура, °С | 1412 | 1250 | 1100 | 1000 |
| Растворимость О, % (ат.) | 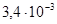
| 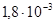
| 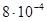
| 
|
При нормальном давлении устойчивы 4 полиморфные модификации SiO2: β-SiO2, α-SiO2, тридимит и кристобалит. Превращение α-SiO2 в SiO2 (коэзит) происходит при давлении 1,8-2,0 ГПа и температуре 500°С. Стишовит образуется при давлении 16-18 ГПа и температурах 1200-1400°С [2].

Рис.1.4. Диаграмма состояния системы Si-O.
Фазовая диаграмма состояния системы Mn-O.
Взаимодействие марганца с кремнием изучалось на основе оксидов: MnO, Mn3O4, Mn2O3, MnO2, Mn2O7. Методом оптической пирометрии определена температура плавления МnО, равная 1842±10°С, область гомогенности МnО находится в интервале 47,4-52,4 % (ат.) O. Температура плавления Мn3О4 равна 156714°С и область гомогенности находится в интервале 57-58,4 % (ат.) О. Соединение Мn3О4 существует в двух модификациях: β-Мn3О4 и α-Мn3О4. Соединение Мn2О3 существует при температуре не выше 900°С, в интервале температур 600-940°С Мn3О4 в присутствии О2 взаимодействует с МnО2 с образованием Мn2О3, при температуре выше 940°С Мn2О3 распадается на Мn3О4 и О2.
На рис. 1.5. приведена диаграмма состояния Mn-О при давлении 0,021 МПа.
Соединение МnО плавится конгруэнтно, а соединение β-Мn3О4 - инконгруэнтно при температуре 1567±4°С. Соединение α-Мn3О4 образуется по перитектоидной реакции при температуре -1190°С. При температуре 1160±5°С β-Мn3О4 распадается по эвтектоидной реакции [2].
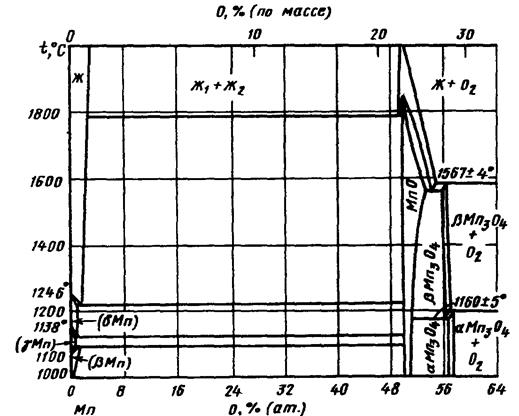
Рис.1.5. Диаграмма состояния Mn-O.
Экспериментальная часть
Расчёт термодинамических функций силицидов марганца по формулам Миедемы и Истмена
Табл. 2.1 Данные, необходимые для расчётов по формулам Миедемы и Истмена [8,9]
| R | P | Q | Φ | n ws 1/3 | ρ, г/см3 | V2/3 | |
| Si | 2,1 | 12,3 | 9,4 | 4,7 | 1,5 | 2,33 | 4,2 |
| Mn | 0 | 14,2 | 9,4 | 4,45 | 1,61 | 7,562 | 3,8 |
Табл. 2.2 Рассчитанные характеристики силицидов марганца.
| Аср. | Vср. | Тразл.,К [7] | ρ | |
| Mn11Si19 | 37,93 | 8,93 | 1423 | 4,25 |
| Mn5Si3 | 44,87 | 8,01 | 1556 | 5,60 |
| Mn5Si2 | 47,27 | 7,79 | 1123 | 6,07 |
| Mn9Si2 | 50,09 | 7,57 | 1333 | 6,61 |
| Mn3Si | 48,23 | 7,71 | 1353 | 6,25 |
Расчеты провели по формулам (1.1) – (1.19).
Результаты расчетов представлены в табл. 2.3.
Табл. 2.3 Стандартные энергии Гиббса образования силицидов марганца.
| хMn | хSi | xsMn | xsSi | f(x) | g | φ | ΔΗf°, Дж/моль | S2980,Дж/моль*К | ΔS2980, Дж/моль*К | ΔG2980, Дж/моль | |
| Mn11Si19 | 0,367 | 0,633 | 0,344 | 0,656 | 0,226 | 6,294 | 1,420 | -485547 | 25,30 | -683,23 | -281944 |
| MnSi* | - | - | - | - | - | - | - | -49680 | 45,42 | -5,28 | -48107 |
| Mn5Si3* | - | - | - | - | - | - | - | -151842 | 238,83 | 23,05 | -158711 |
| Mn5Si2 | 0,714 | 0,286 | 0,693 | 0,307 | 0,213 | 6,078 | 1,292 | -124289 | 29,86 | -167,07 | -74502 |
| Mn0,85Si0,15 | 0,85 | 0,15 | 0,837 | 0,163 | 0,137 | 5,989 | 0,819 | -46627 | 33,16 | -176,75 | 6045 |
| Mn3Si* | - | - | - | - | - | - | - | -26693 | 103,83 | -10,56 | -23546 |
| Mn9Si2 | 0,818 | 0,182 | 0,803 | 0,197 | 0,158 | 6,014 | 0,952 | 83007 | 28,20 | -14,13 | 87218 |
|
из
5.00
|
Обсуждение в статье: Фазовые диаграммы систем Mn - O и Si - O |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

