 |
Главная |
Газ в поле тяжести (распределение Больцмана)
|
из
5.00
|
ОСНОВНЫЕ ПОНЯТИЯ.
1. Плотность  вещества,
вещества,
 ,
,  . (1)
. (1)
2. Концентрация  молекул,
молекул,
 ,
,  . (2)
. (2)
 ,
,  . (3)
. (3)
Давление
 ,
,  = Па (Паскаль). (4)
= Па (Паскаль). (4)
 - нормальная (перпендикулярная к площадке) составляющая силы
- нормальная (перпендикулярная к площадке) составляющая силы  , действующей на площадку
, действующей на площадку  .
.
1мм.рт.ст.=133 Па.
4. Моль - кол-во вещества, содержащее столько же молекул, сколько их содержит 12 грамм изотопа углерода  .
.
Один моль вещества содержит  молекул (число Авогадро
молекул (число Авогадро  ).
).
Молярная масса  - масса моля вещества.
- масса моля вещества.
Для воды ( 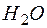 )
)  .
.
Масса одной молекулы  . (5)
. (5)
Количество молей (количество вещества)
 ,
,  . (6)
. (6)
5. Температура Т по шкале Кельвина связана с температурой t по Цельсию:
T=t+273 K.
6. Нормальные условия (н.у.): t=0°С и p=760 мм.рт.ст.
=101,3 кПа.
ИДЕАЛЬНЫЙ ГАЗ.
Условия идеальности газа:
1. можно пренебречь взаимодействием молекул;
2. можно пренебречь собственным объемом молекул;
3. соударения молекул можно рассматривать как абсолютно упругие.
Азот N2, кислород O2 , водород H2, пары воды H2O и другие газы при условиях, близких к нормальным, удовлетворяют условиям идеальности.
Законы идеального газа:
1. Закон Дальтона: давление  смеси газов равно сумме их парциальных давлений
смеси газов равно сумме их парциальных давлений
 . (7)
. (7)
Парциальное – это давление газа, входящего в смесь.
2. Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона)
 , (10)
, (10)
 =8,31 Дж/(моль·К) – газовая постоянная.
=8,31 Дж/(моль·К) – газовая постоянная.
 =1,38·10-23 Дж/K – постоянная Больцмана.
=1,38·10-23 Дж/K – постоянная Больцмана.
Также :

={  }
}  ,
,
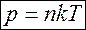 , (11)
, (11)
 - концентрация молекул.
- концентрация молекул.
Основное уравнение МКТ
 , (12)
, (12)
 - средняя кинетическая энергия поступательного движения молекулы.
- средняя кинетическая энергия поступательного движения молекулы.
 - средняя квадратичная скорость молекул,
- средняя квадратичная скорость молекул,  .
.
 .
.
Следствия из основного уравнения МКТ.
1) средняя кинетическая энергия поступательногодвижения молекулы.
 ,
,
 .
.
Приравнивая правые части:  .
.
2) средняя квадратичная скорость молекул
 ,
,
 .
.
 , или
, или 
 .
.
 - масса одной молекулы.
- масса одной молекулы.
Распределение Максвелла молекул по скоростям (распределение Максвелла).
 - число молекул в каком–либо объеме газа,
- число молекул в каком–либо объеме газа,
 - число молекул со скоростями от
- число молекул со скоростями от 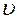 до (
до ( 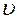 +
+  ).
).
 - относительное число (доля) молекул, движущихся со скоростью
- относительное число (доля) молекул, движущихся со скоростью 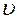 .
.
 - «функция Максвелла», ее вид установлен Д.Максвеллом,
- «функция Максвелла», ее вид установлен Д.Максвеллом,
 (13)
(13)
 Т2 > T 1!!
Т2 > T 1!!
Свойства функции Максвелла:
· Площадь, ограниченная функцией  и осью
и осью 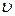 , равна единице:
, равна единице:

 =
=  =
=  = 1 .
= 1 .
· Наиболее вероятная скорость молекул газа 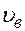 .
.
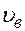 – скорость, с которой движется наибольшее число молекул при данной температуре (на нее приходится максимум функции Максвелла).
– скорость, с которой движется наибольшее число молекул при данной температуре (на нее приходится максимум функции Максвелла).
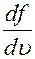 = 0 при
= 0 при 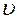 =
= 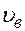 (условие max-ма функции).
(условие max-ма функции).
 ,
,
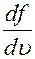 =
= 
 =
=
=  .
.
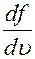 =0, если
=0, если  = 0.
= 0.
 ,
,
или ,  .
.
· Средняя арифметическая скорость 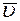 молекул.
молекул.
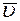 =
=  =
=  , (14)
, (14)
 - число молекул, движущихся со скоростью
- число молекул, движущихся со скоростью  ,
,
 - полное число молекул.
- полное число молекул.
Т.к. величина скорости распределена непрерывно, то сумма в (14) переходит в интеграл:
 , или
, или

 =
=
= 
После интегрирования:
 , или
, или
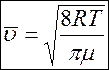 . (15)
. (15)
· Число молекул со скоростями от  до
до 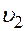 .
.
 =
=  =
=  =
=  .
.
 .
.
Т.е. доля молекул со скоростями от  до
до 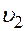 равна площади заштрихованного участка на рисунке 1.
равна площади заштрихованного участка на рисунке 1.
Газ в поле тяжести (распределение Больцмана)

Если плотность среды постоянна, то
 ,
,  .
.
 ,
,
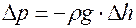 .
.
 Если плотность
Если плотность  меняется, то
меняется, то
 . (16)
. (16)
Из уравнения Менделеева-Клапейрона:
 , или
, или  .
.
Подставим в (16):
 .
.
Разделим переменные и проинтегрируем:
 ,
,
 .
.
 ,
,  ,
,
 . (17)
. (17)

Ур-е (17) - «барометрическая формула». Является приближенным, т.к. считалось, что  = const.
= const.
Т.к.  , то для концентраций также:
, то для концентраций также:
 .
.
 . Тогда
. Тогда
 .
.
 - потенц энергия молекулы в поле тяжести Земли.
- потенц энергия молекулы в поле тяжести Земли.
 - изменение концентрации частиц, в зависимости от величины их потенциальной энергии (распределение Больцмана).
- изменение концентрации частиц, в зависимости от величины их потенциальной энергии (распределение Больцмана).
|
из
5.00
|
Обсуждение в статье: Газ в поле тяжести (распределение Больцмана) |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

