 |
Главная |
Катаболизм аминокислот в толстом кишечнике
|
из
5.00
|
В некоторых ситуациях, а именно:
· при ухудшении всасывания аминокислот,
· при избытке белковой пищи,
· при нарушении деятельности пищеварительных желез,
· при снижении перистальтики кишечника (запоры)
аминокислотыи недопереваренные фрагменты белков достигают толстого кишечника, где подвергаются воздействию кишечной микрофлоры. Такой процесс получил название гниение белков в кишечнике. При этом образуются продукты разложения аминокислот, представляющие собой как токсины(кадаверин, путресцин, крезол, фенол, скатол, индол, пиперидин, пирролидин, сероводород, метилмеркаптан (СН3SН) и другие), так инейромедиаторы (серотонин, гистамин, октопамин, тирамин). Всасываясь в кровь, эти вещества вызывают общую интоксикацию, колебания артериального давления, головные боли, понижение аппетита, понижение болевой чувствительности, анемии, миокардиодистрофии, нарушение желудочной секреции, в тяжелых случаях возможны угнетение дыхания, сердечной деятельности и кома.
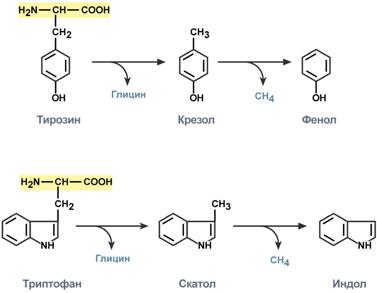
Реакции превращения тирозина и триптофана

Реакции првращения лизина и аргинина
http://www.xumuk.ru/biologhim/180.html
Переваривание белков
Главными источниками белков для человека являются пищевые продукты животного и растительного происхождения. В табл. 12.4 представлены средние данные о содержании белка в основных пищевых продуктах. Главным образом животные (мясо, рыба, сыр) и только некоторые растительные (горох, соя) продукты богаты белками, в то время как наиболее распространенные растительные пищевые продукты содержат небольшие количества его.

Весь сложный процесс переваривания пищевых белков в пищеварительном тракте «настроен» таким образом, чтобы путем последовательного действия протеолитических ферментов лишить белки пищи видовой и тканевойспецифичности и придать продуктам распада способность всасываться в кровь через стенку кишечника. Примерно 95–97% белков пищи всасывается в виде свободных аминокислот. Следовательно, ферментный аппарат пищеварительного тракта осуществляет поэтапное, строго избирательное расщепление пептидных связей белковоймолекулы вплоть до конечных продуктов гидролиза белков – свободных аминокислот. Гидролиз заключается в разрыве пептидных связей —СО—NH— белковой молекулы.

Протеолитические ферменты (протеиназы) обладают широкой специфичностью действия, определяемой как размером полипептида, так и структурой радикалов аминокислот, участвующих в образовании пептидной связи. Основные ферменты, катализирующие гидролитический распад пищевых белков и пептидов, приведены в табл. 12.5.
Следует подчеркнуть, что с пищей человек получает огромное разнообразие белков, однако все они подвергаются воздействию ограниченного числа протеиназ. Эти ферменты относятся к классу гидролаз (см. главу 4) и часто называются также пептидазами. Известны две группы пептидаз: экзопептидазы, катализирующие разрыв концевойпептидной связи с освобождением одной какой-либо концевой аминокислоты, и эндопеп-тидазы, преимущественно гидролизующие пептидные связи внутри полипептидной цепи. Эндопептидазы обладают разной субстратнойспецифичностью действия, всецело определяемой природой радикалов аминокислот по соседству с разрываемойпептидной связью, поэтому белковая молекула распадается под действием разных эндопептидаз на строго определенное число пептидов, сравнительно легко идентифицируемых методами хроматографии и электрофореза(метод отпечатков пальцев). Это свойство эндопептидаз нашло широкое применение в исследовательской работе при выяснении первичной структуры индивидуальных белков.

|
из
5.00
|
Обсуждение в статье: Катаболизм аминокислот в толстом кишечнике |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

