 |
Главная |
Процессинг и посттрансляционная модификация нейропептидов
|
из
5.00
|
Общий принцип синтеза всех достаточно изученных НП состоит в образовании относительно больших пептидов-предшественников, из которых после завершения трансляции выщепляются протеазами соответствующие НП. Как правило, в состав пептида-предшественника входит одна или большее число последовательностей НП (иногда весьма различных по структуре) и так называемая сигнальная последовательность, способствующая миграции предшественника внутри клетки после завершения трансляции в шероховатой эндоплазматической сети и отщепляемая в конце этой части пути.
В 1984 году Gainer сформулировали гипотезу секреторных везикул, согласно которой процессинг биологически активных пептидов осуществляется в процессе передвижения молекул пропептидов по гранулярному ЭПР, комплексу Гольджи и в секреторных везикулах. Последние содержат полный набор ферментов процессинга, специфичный для данной клетки (ткани), а также специальные системы поддержки оптимальной рН среды.
Процессинг нейропептидов внутри секреторных гранул включает в себя эндо- и экзопротеолитические реакции, а также гликолизирование, сульфатирование, амидирование и фосфорилирование N- и С-концевых аминокислотных остатков, что предохраняет образовавшийся продукт от дальнейшей деградации.
Многие пептиды-предшественники образуют промежуточное соединение с гликозидами, которые оказывают стабилизирующее действие на некоторых стадиях процессинга и влияют на выбор мест атаки протеиназами. Протеиназы, обеспечивающие выщепление НП в течение нескольких десятков минут — часа после трансляции, не являются высокоспецифичными. В значительной мере точное выщепление обусловлено наличием в последовательности аминокислот пептидов-предшественников парных остатков. Они в первую очередь атакуются протеиназами, близкими по характеру действия к катепсину В и трипсину. Выщепляемые в этой фазе процессинга фрагменты во многих случаях уже представляют собой активные НП. Нередко эти фрагменты подвергаются дальнейшему протеолизу опять-таки с образованием новых НП. На этой фазе описано участие не только трипсиноподобных протеиназ, но и ряда других протеиназ, специфичность которых тоже не является очень высокой. Однако в различных нейронах и, возможно, даже в разных терминалях одного нейрона их набор может быть неодинаковым, что обеспечивает в конечном счете ту или иную специализацию на продукции строго определенных НП (единичных или их комплексов).
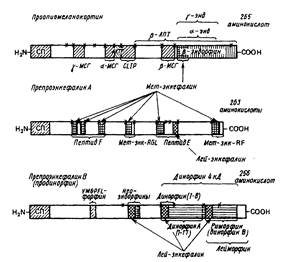
Так например, многие эндопептидазы, участвующие в процессинге энкефалинов обладают очень узкой субстратной специфичностью. Так, эндопептидаза, специфичная к связи Lys-Arg, не расщепляет связи Arg-Arg и Arg-Lys, что объясняют специфичностью фермента не только к гидролизуемой связи, но и, вероятно, к ближайшему аминокислотному окружению. Расщепление может происходить иногда не по парам остатков основных аминокислот, а по моноостаткам аргинина, лизина или каких-либо других аминокислот. Например, тиоловая прогормон-конвертаза расщепляет предшествен-ники энкефалинов с обеих сторон по моно- и диосновным остаткам аминокислот, но более высокую специфичность проявляет к моноосновным сайтам. Все этапы процессинга хорошо иллюстрируются схемой превращений проопиомеланокортина, из которого могут формироваться β-липотропин, АКТГ1-39, АКТГ1-24, АКТГ18-39 (так называемый CLIP), α, β- и γ-МSH, β-, γ- и α-эндорфины, Met-энкефалин, дезтирозильные производные эндорфинов, С-концевой дипептид β-эндорфина и, возможно, еще некоторые другие НП. Еще раз подчеркнем, что имеется в виду не одновременное образование всех этих НП в одном нейроне или терминали, а более или менее избирательное формирование их в зависимости от набора протеаз в данной клетке.
Обращает на себя внимание, что синтез ряда опиоидных пептидов, содержащих в качестве минимальной активной последовательности Met-энкефалин, обеспечивается по крайней мере двумя пептидами-предшественниками — проопиомеланокортином (локализованным главным образом, но не исключительно в гипофизе) и препроэнкефалином А (локализованным преимущественно, но опять-таки не исключительно в надпочечниках). Сходным образом лей-энкефалинсодержащие опиоидные НП выщепляются из мозгового пептида-предшественника продинорфина (препроэнкефалина В) и из уже упоминавшегося препроэнкефалина А, совмещающего в себе последовательности НП с лей-энкефалиновыми и мет-энкефалиновыми активными центрами. Однако общность минимальных последовательностей опиоидных НП, заключенных в разных пептидах-предшественниках, не означает идентичности содержащих их НП большого размера: продинорфин образует лей-морфин и перекрывающийся с ним каскад динорфинов разного размера (динорфин В (риморфин) и 4кД-ди-норфин), а также α- и β-неоэндорфины. Из препроэнкефалина А формируются самостоятельные НП, содержащие и лей-энкефалин, и мет-энкефалин (например так называемый пептид Е).
Сходные закономерности структуры можно отметить и для некоторых других пептидов-предшественников, хотя они, как правило, исследованы в гораздо меньшей степени, чем предшественники опиоидов, АКТГ и МСГ. Можно полагать, что дальнейший анализ биологической активности их фрагментов позволит выявить источники новых НП.
Обращают на себя внимание большие области пептидов-предшественников, где пока не идентифицированы НП. Хотя часть из них выполняет (судя по β -эндорфину, АКТГ) функции дополнительных "адресных" последовательностей, уточняющих взаимодействие НП преимущественно с определенной тканью иди органом, есть основания предполагать и в них наличие последовательностей еще не идентифицированных НП. В ряде случаев образование НП и процессы их распада переплетаются друг с другом. Например, один из путей распада β-эндорфина - НП, имеющего самостоятельное функциональное значение, ведет, как уже упоминалось, к образованию γ-эндорфина и опять-таки НП, имеющего уникальную функциональную характеристику; отщепление концевого аминокислотного остатка от γ -эндорфина приводит к образованию α-эндорфина, весьма своеобразного по функциям, и т.д.
Регуляция метаболизма активных регуляторных пептидов определяется большим спектром воздействий, изменяющих гомеостаз на любом уровне - уровне клетки (транскрипция, трансляция и посттрансляционный процессинг), ткани (секреция и инактивация нейропептидов), а также на уровне организма в целом. Именно эти морфогенетические и биохимические особенности биогенеза и определяют уровень активных регуляторных пептидов в организме. При этом, несомненно, важная регулирующая роль в метаболизме нейропептидов принадлежит протеолитическим ферментам.
|
из
5.00
|
Обсуждение в статье: Процессинг и посттрансляционная модификация нейропептидов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

