 |
Главная |
ТЕОРИЯ АКТИВИРОВАННОГО КОМПЛЕКСА (ТАК) ИЛИ ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ (ТПС).
|
из
5.00
|
Теории химической кинетики.
Теория активных столкновений (ТАС).
Основные предпосылки:
1. Молекулы представляют в виде шариков.
2. Для того, чтобы произошло взаимодействие, необходимо столкновение.
3. Процесс протекает только в том случае, если энергия столкновения больше или равна определенному значению энергии, которая называется энергией активации.
В основу этой теории положено два учения: молекулярно-кинетическая теория и теория Больцмана.
Вывод уравнения ТАС.
z – общее число столкновений в единицу времени.
z= 
Д – эффективный диаметр молекул;
n – число молекул в единице объема;
M – молекулярная масса.
С помощью закона Больцмана определяем количество активных столкновений z  , т.е. таких, в которых энергия превышает энергию активации:
, т.е. таких, в которых энергия превышает энергию активации:
z 
Тогда доля активных столкновений составит:

Рассмотрим бимолекулярную газовую реакцию типа: 2А  , где Р – продукты реакции. Например, это может быть разложение йодистого водорода:
, где Р – продукты реакции. Например, это может быть разложение йодистого водорода:
2HJ 
Теперь заметим, что в результате каждого активного столкновения расходуется две молекулы исходного вещества. Поэтому количество прореагировавших молекул в единице объема будет равна удвоенному количеству активных столкновений в то же время и в том же объеме:
 или
или
 (
(  )
)
Отсюда видно, что скорость реакции зависит от квадрата концентрации.
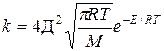
 = k
= k 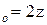
k=k  уравнение Аррениуса
уравнение Аррениуса
Сравнение этих уравнений позволяет установить физический смысл предэкспоненциального множителя k  , который оказывается пропорциональным общему количеству столкновений всех молекул в единице объема за единицу времени.
, который оказывается пропорциональным общему количеству столкновений всех молекул в единице объема за единицу времени.
В общем виде уравнение Аррениуса для всех типов реакций часто пишут в виде:
k=z  уравнение Аррениуса
уравнение Аррениуса
Константа, рассчитанная по этому уравнению, не дает совпадения с экспериментальными данными. Для корректировки в это уравнение вводят стерический фактор р.
Тогда уравнение Аррениуса с точки зрения ТАС запишется следующим образом:
k = pz 
Считается, что стерический фактор отличается от единицы потому, что для осуществления реакции необходима определенная ориентация реагирующих молекул.
В этом уравнении Е – энергия активации, рассчитанная по ТАС, абсолютная (истинная) энергия активации, а экспериментальная – эффективная энергия активации.
Е 

Факты, которые не объясняет ТАС:
1. Не дает метода теоретического расчета энергии активации.
2. Не объясняет протекания в растворах.
3. Не объясняет природы стерического фактора.
МОНОМолекулярные реакции с точки зрения ТАС.
Теория Линдемана.
В элементарном акте мономолекулярной реакции участвует всего одна молекула. В соответствии с теорией активных столкновений реакция начинается со встречи двух активных молекул. Количество столкновений пропорционально квадрату концентраций. Поэтому, казалось бы, что мономолекулярные реакции, как и бимолекулярные, должны иметь порядок, равный двум. Но многие мономолекулярные реакции описываются уравнением первого порядка, причем порядок реакции может изменяться при изменении концентрации (давления) и быть дробным.
Объяснение механизмов газовых мономолекулярных реакций дано Линдеманом. Он предположил, что после столкновения активные молекулы могут не только распадаться на продукты реакции, но и дезактивироваться. Механизм реакции представляется двухстадийным:
1) A+A 
2) 
A  – активная молекула.
– активная молекула.
На первом этапе происходит перераспределение энергии, в результате чего одна молекула становится активной, а другая дезактивируется.
На второй стадии оставшиеся активные молекулы мономолекулярно превращаются в продукты реакции.
Рассмотрим стационарный процесс:
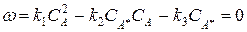
Выразим концентрацию активной частицы А*:  . Подставим это выражение в выражение скорость определяющей стадии (вторая стадия):
. Подставим это выражение в выражение скорость определяющей стадии (вторая стадия):
 уравнение Линдемана
уравнение Линдемана
Анализ уравнения Линдемана:
1. СА – очень маленькая. В этом случае промежутки между столкновениями молекул настолько велики, что дезактивация происходит редко. Распад активных молекул на продукты происходит без затруднений; лимитирующей стадией является стадия активации. В связи с этим в уравнении Линдемана пренебрегаем в знаменателе  относительно k3 (
относительно k3 (  << k3).
<< k3).
 ; n=2 (второй порядок реакции)
; n=2 (второй порядок реакции)
2. СА – очень большая. В этом случае лимитирующей стадией является стадия вторая, мономолекулярная. Затрудненность этой стадии объясняется тем, что активные молекулы часто теряют избыточную энергию при столкновении и не успевают образовывать продукты реакции. Тогда в уравнении Линдемана в знаменателе можно пренебречь k3 относительно  (
(  >>k3).
>>k3).
 ; n=1 (реакция первого порядка)
; n=1 (реакция первого порядка)
3. СА – средняя. В этом случае мономолекулярные реакции могут иметь дробный порядок (1<n<2).
ТЕОРИЯ АКТИВИРОВАННОГО КОМПЛЕКСА (ТАК) ИЛИ ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ (ТПС).
Основным представлением ТАК является положение о том, что всякая химическая реакция протекает через образование некоторого переходного состояния, которое затем распадается на продукты данной реакции.
Основные положения теории:
1. В ходе процесса молекулы постепенно приближаются друг к другу, в результате чего меняются межъядерные расстояния.
2. В ходе реакции образуется активированный комплекс, когда один из атомов становится как бы обобществленным, и межъядерное расстояние становится одинаковым.
3. Активированный комплекс превращается в продукты реакции.
Например, реакцию разложения йодоводорода можно представить следующим образом:

Сначала две молекулы HJ расположены достаточно далеко друг от друга. При этом существует взаимодействие лишь между атомами в молекуле. После сближения на достаточно короткое расстояние начинают возникать связи между атомами, входящими в состав разных молекул, и связи H – J становятся более слабыми. В дальнейшем они ещё более ослабевают и полностью разрываются, а новые связи H – H и J – J, наоборот, упрочняются. В результате происходит перегруппировка атомов и вместо исходных молекул НJ образуются молекулы Н2 и J2. В процессе сближения и перегруппировки атомов молекулы образуют некоторый малоустойчивый активированный комплекс из двух молекул водорода и двух молекул йода; комплекс существует очень недолго и в дальнейшем распадается на молекулы продуктов. На его образование необходима затрата энергии, равная энергии активации.
Представление об активированном комплексе и об энергии активации подтверждается с помощью энергетических диаграмм, построение которых используется в ТАК.
Активированный комплекс всегда имеет избыток энергии по сравнению с энергией реагирующих частиц.
А–В+D 
 → A+B–D
→ A+B–D
переходное состояние

Е1 – энергия связи BD без А.
Е2 – энергия связи АB без D.
Е3 – энергия связи переходного состояния.
Е4 – энергия свободных атомов.
Е3 – Е2 = Е активации прямой реакции.
Е2 – Е1 = ∆Н тепловой эффект реакции.
Е4 – Е2 – энергия разрыва связи АВ.
Е4 – Е1 – энергия разрыва связи ВD.
Так как энергия разрыва связей Е4 >> Е активации, то реакция протекает с образованием активированного комплекса без предварительного разрыва связей.
|
из
5.00
|
Обсуждение в статье: ТЕОРИЯ АКТИВИРОВАННОГО КОМПЛЕКСА (ТАК) ИЛИ ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ (ТПС). |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

