 |
Главная |
Сравнение свойств элементов I А и II А (комплексообразование, образование осадков) на примере Na , K и Mg , Ca
|
из
5.00
|
ХИМИЧЕСКИЕ СВОЙСТВА И БИОЛОГИЧЕСКАЯ РОЛЬ ЭЛЕМЕНТОВ S -БЛОКА
К s-элементам относятся две группы Периодической системы: IА и IIА.
В группу IА входят 8 элементов: литий, калий, натрий, рубидий, цезий, франций, водород, гелий. В группу IIА входят 6 элементов: бериллий, магний, кальций, стронций, барий, радий.
Общим является застраивание в их атомах электронами s-подуровня внешнего энергетического уровня. (Т.Е. говорим о "семействе элементов". ВСПОМИНАЕМ: "семейство элементов" определяется тем, какой подуровень заполняется электронами в последнюю очередь.)
Электронная формула внешней оболочки:
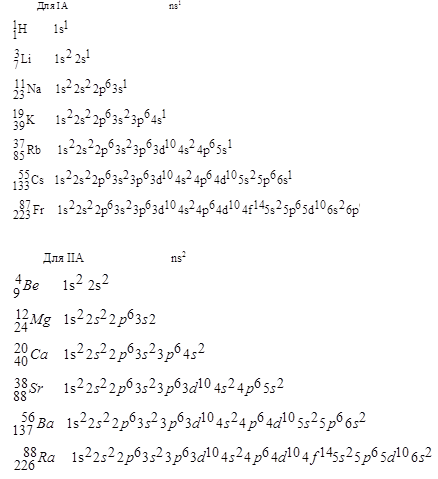
СРАВНЕНИЕ СВОЙСТВ ЭЛЕМЕНТОВ I А И II А (КОМПЛЕКСООБРАЗОВАНИЕ, ОБРАЗОВАНИЕ ОСАДКОВ) НА ПРИМЕРЕ Na , K И Mg , Ca
Общая характеристика элементов I А и II А
Элементные вещества - типичные металлы, обладающие блеском, высокой электрической проводимостью и теплоповодимостью, химически весьма активны.
Как следует из электронных формул, элементы I А группы (Na , K) имеют на внешнем энергетическом уровне по одному s электрону. Элементы II А группы (Mg , Ca) по 2 s электрона.
Химические свойства s элементов I А и II А групп сходны.
s-элементы I А и II А имеют относительно большие радиусы атомов и ионов.
s-элементы I А и II А групп легко отдают валентные электроны. Являются сильными восстановителями. С ростом радиуса атома в группах I А и II А ослабевает связь валентных электронов с ядром, следовательно s-элементы этих групп имеют низкие значения Еи и Еср. к ẽ. Все щелочные и щелочноземельные металлы имеют отрицательные стандартные окислительно-восстановительные потенциалы, большие по абсолютной величине. Что также характеризует их, как сильных восстановителей. Восстановительные свойства возрастают закономерно с увеличением радиуса атома. Восстановительная способность увеличивается по группе сверху вниз.
Для элементов II А группы характерна большая, чем для элементов I А группы способность к комплексообразованию.
s-элементы I А и II А образуют соединения с ионным типом связи.
Исключение составляет водород, для которого в соединениях даже с самыми электроотрицательными элементами характерна преимущественно ковалентная связь (например, фтороводород или вода). Частично ковалентный характер связи в соединениях имеет место у лития, бериллия и магния.
Сравнение свойств элементов I А и II А (комплексообразование, образование осадков) на примере Na , K и Mg , Ca
Атомы элементов I А группы имеют по одному валентному электрону на s подуровне внешнего энергетического уровня. Это обуславливает проявление степени окисления +1.

Все элементы I А группы сходны по свойствам, что объясняется однотипным строением не только внешней, валентной оболочки, но и предвнешней (исключение литий).
С ростом радиуса атома в группе I А ослабевает связь валентного электрона с ядром. Соответственно, уменьшается энергия ионизации атомов. Так как радиус атома калия больше, чем радиус атома натрия, то энергия ионизации калия меньше, чем у натрия.
В результате ионизации образуются катионы Э+, имеющие устойчивую конфигурацию благородных газов.
Химическая активность металлов I А группы возрастает закономерно с увеличением радиуса атома и уменьшением их способности к гидратированию (чем меньше способность к гидратированию, тем активнее металл).
Так как радиус атома калия больше, чем радиус атома натрия, то способность к гидратации для катиона калия будет ниже, чем для катиона натрия, а, следовательно, химическая активность катиона калия выше, чем у катиона натрия.
Вследствие незначительного поляризующего действия (устойчивая электронная структура, большие размеры, малый заряд ядра) комплексообразование для ионов щелочных металлов малохарактерно. Вместе с тем, они способны образовывать комплексные соединения с некоторыми биолигандами (КЧ для натрия и калия может принимать значения 4 и 6). Способность образовывать донорно-акцепторные связи с соответствующими лигандами едва намечается у натрия. У калия имеется значительная тенденция к использованию имеющихся в атоме вакантных d-орбиталей.
Например, образование комплексов калия с антибиотиком валиномицином. Валиномицин образует с калием прочные комплексы, связывание этого антибиотика с натрием очень незначительно.
Большинство солей щелочных металлов хорошо растворимы в воде (исключение составляют некоторые соли лития).
Атомы элементов II А группы имеют по два валентных электрона на s подуровне внешнего энергетического уровня.
В нормальном состоянии у атомов этих элементов нет неспаренных электронов, но при переходе атомов в возбужденное состояние один из s валентных электронов переходит на р-подуровень. Это обуславливает проявление степени окисления +2.

Степени окисления больше +2 элементы II А группы не проявляют.
Несмотря на то, что число валентных s электронов у атомов II А группы одинаково, свойства магния и кальция отличаются друг от друга.
Это связанно с тем, что в атоме кальция, в отличие от атома магния, имеются свободные d-орбитали, близкие по энергии к ns орбиталям.
Магний и кальций существенно различаются размерами атомов и ионов:
· металлический радиус атома Mg = 160 пм;
· металлический радиус атома Ca = 197 пм.
· кристаллический радиус иона Mg2+ = 74 пм;
· кристаллический радиус иона Ca2+ = 104 пм..
Больший размер иона кальция обусловливает и более высокое координационное число этого иона – КЧ (Ca2+) 6, 8, тогда как КЧ (Mg2+) – 6. Прочность комплексных соединений уменьшается по мере увеличения радиуса атома, следовательно, комплексные соединения магния будут более прочными, чем комплексные соединения кальция. Ион Mg2+ образует шестикоординационные соединения регулярной структуры. Ca2+ образует несимметричные комплексы. Кальций предпочтительно координируется с атомами кислорода, магний – с атомами азота.
Многие соли щелочноземельных металлов малорастворимы в воде (малорастворимы CaF2, MgF2; практически не растворимы фосфаты кальция и магния). Причем с ростом порядкового номера растворимость солей снижается.
Такой характер изменения растворимости солей играет важную роль в биологическом действии катионов этой группы. Уменьшение растворимости кальция фосфата и карбоната по сравнению с фосфатами и карбонатами магния является, по видимому, одной из причин формирования скелета всех живых организмов именно из этих соединений кальция.
В живых организмах из ионов кальция и фосфат-ионов образовался кристаллический минерал ГИДРОКСИЛАПАТИТ – Ca10(PO4)6(OH)2 – основное вещество костной и зубной ткани. Магний является макроэлементом, но лучшая растворимость магния фосфата Mg3(PO4)2 и основного карбоната Mg(OH)2)*4MgCO3*H2O объясняет тот факт, что его соединения не сыграли значительной роли в построении скелета.
|
из
5.00
|
Обсуждение в статье: Сравнение свойств элементов I А и II А (комплексообразование, образование осадков) на примере Na , K и Mg , Ca |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

