 |
Главная |
Временные характеристики УВ системы
|
из
5.00
|
Вопросы к дисциплине
«Формирование углеводородных систем» Косенкова Н.Н.
Определения углеводородной системы, оценка эффективности УВ систем
1) УВ система – динамическая система, в которой присутствуют факторы, элементы и процессы, которые приводят к скоплению коммерческих запасов нефти и газа. Система – комплекс взаимосвязанных элементов и процессов.
По Cornford УВ система – это все коммерческие скопление нефти и газа, полученные из одной зрелой НГМТ (PS concept – 1 НГМТ, разные типы резервуаров). Play concept – несколько НГМТ, 1 тип резервуара.
УВ мб представлены:
1) Термогенными и биогенными газами, образующими, как обычные скопления, так и газогидратные, в плотных (tight) и глинистых (shale) коллекторах, в угольных пластах
2) Конденсатом
3) Нефтью
4) Природными битумами
В зависимости от имеющейся информации УВ мб:
1) Известная (!) – имеются залежи УВ, связанные с НГМТ (есть корреляция нефть - ОВ)
2) Предполагаемая (.) – имеются геохимические предпосылки для генерации УВ, но нет открытых залежей
3) Гипотетическая (?) – имеются геологические благоприятные факторы для нефтегазоносности, но нет геохимичексих данных
2) КПД УВ систем = кол-во открытых УВ/ кол-во генерированных УВ
По опубл данным КПД известных УВ систем 0,5-30%
Кол-во открытых УВ= (Sместорождений*Hнефтенасыщ пород*пористость)-потери
Кол-во генерир УВ = потенциал НГМТ*толщина НГМТ)*S*TR
2. Элементы и процессы УВ системы


Временные характеристики УВ системы

Временные характеристики УВ системы
В процессе перемещения УВ в пластах непрерывно изменяются давление, температура, количественное соотношение нефти и газа. Это сопровождается непрерывным изменением состава газовой и жидкой фаз и переходом различных углеводородов из одной фазы в другую. Особенно быстро такие превращения происходят при движении нефти по стволу скважины от забоя к устью.
Дальнейшее движение нефти и газа к потребителю также сопровождается непрерывными фазовыми превращениями. Закономерности фазовых переходов и фазовое состояние газонефтяных смесей при различных условиях необходимо знать для решения многих задач.
Интенсивность выделения газовой фазы из нефти зависит от многих факторов, основными из которых являются:
- темп снижения давления и температуры при движении нефтяного потока;
- наличие в составе нефти лёгких углеводородов (С2–С6);
- молекулярная масса нефти;
- вязкость нефти.
СХЕМА ФАЗОВЫХ ПРЕВРАЩЕНИЙ ОДНОКОМПОНЕНТНЫХ СИСТЕМ
Углеводородные газы, подобно всем индивидуальным веществам, изменяют свой объём при изменении давления и температуры. На рис. 4.1 представлена диаграмма фазового состояния для чистого этана. Каждая из кривых соответствует фазовым изменениям при постоянной температуре и имеет три участка. Слева от пунктирной линии отрезок соответствует газовой фазе, горизонтальный участок – двухфазной газожидкостной области, левый участок – жидкой фазе. Отрезок пунктирной линии вправо от максимума в точке С называется кривой точек конденсации (или точек росы), а влево от максимума – кривой точек парообразования (кипения). В точке С пунктирной линии кривые парообразования и конденсации сливаются. Эта точка называется критической. С приближением температуры и давления к критическим значениям свойства газовой и жидкой фаз становятся одинаковыми, поверхность раздела между ними исчезает, и плотности их уравниваются. Следовательно, с приближением к критической точке по кривой начала кипения плотность жидкой фазы будет непрерывно убывать. Если же к ней приближаться по линии точек конденсации, то плотность пара будет непрерывно возрастать.

Рис. 4.1. Диаграмма фазового состояния чистого этана.
Для индивидуальных углеводородов граничным давлением между жидкой и газовой фазой является давление упругости паров (при данной температуре), при котором происходит конденсация или испарение. Обе фазы (жидкость и пар) при данной температуре присутствуют в системе только в том случае, если давление равно упругости насыщенного пара над жидкостью.
Фазовые превращения углеводородов можно также представить в координатах давление-температура (рис. 4.2). Для однокомпонентной системы кривая давления насыщенного пара на графике давление-температура является одновременно кривой точек начала кипения и линией точек росы. При всех других давлениях и температурах вещество находится в однофазном состоянии.
Фазовая диаграмма индивидуальных углеводородов ограничивается критической точкой С (рис. 4.2). Для однокомпонентных систем эта точка определяется наивысшими значениями давления и температуры, при которых ещё могут существовать две фазы одновременно.

Рис. 4.2. Диаграмма фазового состояния чистого этана в координатах Т-Р.
Из рисунка 4.2 следует, что путём соответствующих изменений давления и температуры углеводороды можно перевести из парообразного состояния в жидкое, минуя двухфазную область. Газ, характеризующийся параметрами точки А (рис. 4.2), можно изобарически нагреть до температуры точки В, а затем, повысив давление в системе при постоянной температуре, перевести вещество в область точки D, расположенную выше критической точки С, и далее в область точки Е. Свойства системы при этом изменяются непрерывно, и разделения углеводорода на фазы не произойдёт. При дальнейшем охлаждении системы (от точки D до точки Е), а затем при снижении давления до точки F вещество приобретёт свойства жидкости, минуя область двухфазного состояния.
Значительно сложнее закономерности фазовых переходов двух- и многокомпонентных систем.
В смеси углеводородов каждый компонент имеет собственные значения упругости насыщенных паров, поэтому процессы конденсации и испарения не будут проходить при конкретных значениях давления и температуры, а в определённом диапазоне значений давления и температуры. Границы диапазона будут тем больше, чем больше разница между критическими значениями давления и температуры индивидуальных компонентов, входящих в систему. Более подробную информацию по фазовым переходам многокомпонентных систем можно найти в литературе [3, 4].
4.2. ФАЗОВЫЕ ПЕРЕХОДЫ В НЕФТИ, ВОДЕ И ГАЗЕ
Фазовые переходы подчиняются определённым закономерностям, в основе которых лежит понятие равновесия фаз. Равновесие фаз характеризуется константой равновесия, которая зависит от температуры и давления.
Константа фазового равновесия i-го компонента характеризуется отношением мольной доли компонента в газовой фазе (уi или Nyi) к мольной доле этого компонента в жидкой фазе (хi или Nxi), находящейся в равновесном состоянии с газовой фазой:
 . (4.1)
. (4.1)
Для определения равновесного состояния газожидкостных смесей используются законы Дальтона и Рауля.
Согласно закону Дальтона каждый компонент, входящий в газовую фазу имеет своё парциальное давление Pi, а общее давление в газовой системе равно сумме парциальных давлений:
 (4.2)
(4.2)
Согласно закону Рауля, парциальное давление компонента над жидкостью (нефтью) равно давлению насыщенного пара (Рнас. пара) или упругости пара (Qi) и этого компонента, умноженному на его мольную долю в нефти:
 или
или  (4.3)
(4.3)
где Qi – упругость паров компонента;
Nxi – мольная доля компонента
piнас. пара – давление насыщенного пара i-го компонента.
В момент равновесия парциальное давление i-го компонента в газовой фазе равно парциальному давлению компонента над жидкостью. Отсюда следует закон Дальтона-Рауля для равновесного состояния газовой и нефтяной фазы:
 ; (4.4)
; (4.4)
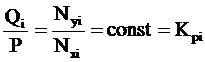 , (4.5)
, (4.5)
где Кi – константа равновесия i-го компонента при данной температуре и давлении смеси.
Уравнение материального баланса для одного моля нефтегазовой смеси:
 , (4.6)
, (4.6)
где L – мольная доля жидкой фазы;
V – мольная доля паровой фазы
Nzi – мольные доли компонентов в нефтегазовой смеси.
По условию сумма мольной доли жидкой и паровой фаз равна единице. Отсюда:
V=1–L. (4.7)
Используя уравнения (4.6) и (4.7) получим выражение для мольной доли компонента жидкой фазы:
 , (4.8)
, (4.8)
или
 , (4.9)
, (4.9)
и для мольной доли компонента газовой фазы:
 . (4.10)
. (4.10)
4. 
Моделирование кинетического преобразования органического вещества
ПРИМЕР ПЕРЕСЧЕТА ТОС НА НАЧАЛЬНЫЕ КОНЦЕНТРАЦИИ


ОБЩАЯ СХЕМА РАЗЛОЖЕНИЯ КЕРОГЕНА



|
из
5.00
|
Обсуждение в статье: Временные характеристики УВ системы |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

