 |
Главная |
Константа химического равновесия
|
из
5.00
|
Лекция 11
Химическое равновесие. Принцип Ле Шателье.
План:
Обратимость химических реакций
Понятие о химическом равновесии
Константа химического равновесия
Факторы, влияющие на равновесие. Принцип Ле-Шателье
Обратимость химических реакций и понятие о химическом равновесии
Необратимыми называются реакции, которые протекают только в одном направлении и идут до конца. Различают практически и совершенно необратимые реакции. В практически необратимых преобладает реакция, идущая в одном направлении. Среди них выделяют несколько типов:
1.Реакции двойного обмена с образованием малорастворимого вещества
NaCl + AgNO3 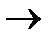 NaNO3 + AgCl
NaNO3 + AgCl 
С1- + Ag+ 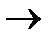 AgCI
AgCI 
2.Реакции с образованием газообразных веществ
Na 2 CO 3 +  2 HCl
2 HCl 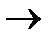 2 NaCl + H 2 O + С O 2
2 NaCl + H 2 O + С O 2 
C О32- + 2Н+ 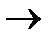 H 2 O + С O 2
H 2 O + С O 2 
3.Реакции с образованием малодиссоциирующих веществ
HNO 3 + KOH 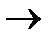 KNO 3 + H 2 O
KNO 3 + H 2 O
Н+ + ОН- = H 2 O
4.Ионные реакции окисления – восстановления
Zn + H2SO4 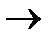 ZnSO4 + H2
ZnSO4 + H2 
Zn + 2H+ 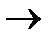 Zn+2 + H2
Zn+2 + H2 
5.Реакции, приводящие к образованию комплексных соединений
CuSO4 + 4NH4OH = [Cu(NH3)4]SO4 + 4H2O
С u 2+ + 4 NH 4 OH = [ Cu ( NH 3 )4] 2+ + 4 H 2 O
6.Реакции, сопровождающиеся выделением большого количества энергии
C 6 H 12 O 6 + 6 O 2 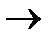 6С O 2 + 6 H 2 O
6С O 2 + 6 H 2 O  H 0 = -2867кДж/моль
H 0 = -2867кДж/моль
Примеры совершенно необратимых процессов:
2К ClO 3 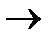 2 KCl + 3 O 2
2 KCl + 3 O 2
Pb ( N 3 )2 
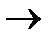 Pb + 3 N 2
Pb + 3 N 2
(азид свинца)
(в обычных условиях нельзя получить бертолетову соль непосредственно из KCl и О2), а также нельзя провести синтез азида свинца из азота и свинца.
Обратимыми называются реакции, которые протекают в противоположных направлениях и не идут до конца. Примеры обратимых реакций:
N 2 + 3 H 2 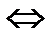 2 NH 3
2 NH 3
C + CO2 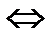 2CO
2CO
N2 + O2 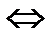 2NO
2NO
H2 + J2 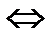 2HJ
2HJ
PCl5 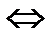 PCl3 + Cl2
PCl3 + Cl2
CO + Cl2 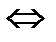 COCl2 (фосген)
COCl2 (фосген)
2NO + O2 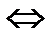 2NO
2NO
Понятие о химическом равновесии
В ходе реакции устанавливается подвижное химическое равновесие, при котором скорости прямой и обратной реакции равны. Такое состояние системы реагирующих веществ , при котором скорости прямой и обратной реакций равны между собой называется химическим равновесием .
Константа химического равновесия
Для реакции в общем виде mA + nB 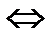 p С + gD скорости прямой и обратной реакций описываются следующими кинетическими уравнениями
p С + gD скорости прямой и обратной реакций описываются следующими кинетическими уравнениями
→
v1  = к 1 · [A] m · [B] n
= к 1 · [A] m · [B] n
←
v2 = k2 · [C] p · [D] g
Концентрации реагирующих веществ, которые устанавливаются при химическом равновесии, называются равновесными, обозначаются при помощи квадратных скобок, в отличии от неравновесных. → ←
В состоянии динамического равновесия v1 = v2 - кинетическая концепция равновесия. С течением времени v1 уменьшается, а v2- увеличивается. В некоторый момент они становятся равными.
k 1 · [ A ] m · [ B ] n = k 2 · [ C ] p · [ D ] g
разделив обе части уравнения на k2, получим
Кс = k1/k2 = [ C]p · [D]g/ [A]m · [B]n
Этим выражением определяется классическая константа равновесия Кс обратимого процесса, она равна отношению констант прямой и обратной реакций Кс = k 1 / k 2
Константа Кс, отражающая соотношение концентраций компонентов обратимой реакции в состоянии динамического равновесия называется константой равновесия.
Кс = [C]p · [D]g/ [A]m · [B]n –
|
из
5.00
|
Обсуждение в статье: Константа химического равновесия |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

