|
Главная |
Приготовление шкалы стандартных растворов железа.
|
из
5.00
|
В мерные колбы емкостью 50 мл отмеривают от 0 до 20 мл рабочего стандартного раствора железа и доводят объемы дистиллированной водой до метки.
Таблица 2.3
Приготовление шкалы стандартных растворов железа
| № раствора | 1 | 2 | 3 | 4 | 5 |
| Объём рабочего р-ра, мл | 0 | 5 | 10 | 15 | 20 |
| С Fe3+, мг/л | 0 | 0,5 | 1,0 | 1,5 | 2,0 |
Реактивы:
аммиак, разбавленный (2:3) раствор;
кислота соляная, разбавленный (3:2) раствор;
рабочий стандартный раствор железа с CFe3+ 0,005 мг/см3;
сульфосалициловая кислота, 10 %-ный раствор;
Ход определения
В колбу емкостью 50 мл наливают 20 мл анализируемого раствора, затем прибавляют пипеткой 2 мл раствора сульфосалициловой кислоты и, в зависимости от рН фильтрата, раствор соляной кислоты или аммиака; затем содержимое колбы тщательно перемешивают. Спустя 10 мин оптическую плотность окрашенного раствора измеряют с помощью КФК-2 на длине волны l=536—540 нм.
Приготовление и окрашивание, а затем и фотометрирование рабочей шкалы растворов сравнения производится по аналогичной схеме: 20см3 стандартного раствора + раствор сульфосалициловой кислоты и другие реактивы. Полученные значения D наносят на график против соответствующих концентраций железа в мг/л, и на основе этих данных строится калибровочная кривая, по которой определяют содержание трёхвалентного железа в фильтратах. Если значение оптической плотности исследуемого раствора выходит за пределы, обозначенные на графике, пробу следует разбавить и провести повторное фотометрирование.
Погрешность измерения оптической плотности на КФК-2 составляет 0,5% (±0,005).
 |
Таблица 2.4
Зависимость оптической плотности растворов сравнения от концентрации ионов Fe3+
| № раствора | 1 | 2 | 3 | 4 | 5 |
| С Fe3+, мг/л | 0 | 0,5 | 1,0 | 1,5 | 2,0 |
| D | 0 | 0,014 | 0,030 | 0,035 | 0,050 |
Определение значения рН исследуемых растворов
Во всех вышеперечисленных опытах вместе с определением концентраций ионов Al3+ и Fe3+ в исследуемых растворах изучалось влияние порошка диатомита на реакцию раствора. Проводилось измерение значений рН растворов извлечения и фильтратов потенциометрическим методом, и затем вычислялось ΔрН по формуле:
ΔрН=рНисх-рНф, где рНисх – значение рН раствора извлечения,
рНф – значение рН фильтрата.
Замеры рН проводились с использованием лабораторного рН-метра ЛПУ-01 с хлорсеребряным и стеклянным электродами соответственно в качестве электрода сравнения и измерительного электрода.
Нужное значение рН раствора извлечения в диапазоне от 1 до 13 устанавливалось путём прибавления к 1 М раствору хлористого калия разбавленных растворов соляной кислоты или аммиака.
Настройка рН-метра проводилась по буферным растворам с рН 1.68 (0,05 М раствор тетраоксалата калия), 6,86 (0,025 М раствор калия фосфорнокислого однозамещённого и 0,025 М раствор натрия фосфорнокислого двузамещённого) и 9,18 (0,01 М раствор натрия тетраборнокислого).
| Погрешность измерения рН: | в диапазоне рН 2-14 – ±0,04 в диапазоне рН -2-14 – ±0,40 |
2.4 Результаты исследований и обсуждение
Валовый химический состав исследуемого диатомита
По данным рентгеноспектрального анализа диатомит Инзенского месторождения, послуживший материалом для наших исследований, имеет химический состав, приведённый в таблице 2.5.
Таблица 2.5
Химический состав диатомита Инзенского месторождения Ульяновской области
| Содержание, в % на сухую породу. | |||||||||
| Na2O | MgO | Al2O3 | SiO2 | P2O5 | SO2 | K2O | CaO | TiO2 | Fe2O3 |
| 0,01 | 0,07 | 5,35 | 90,20 | 0,09 | 0,03 | 0,12 | 0,70 | 0,12 | 3,22 |
По сравнению с цифрами, приведёнными в литературе, эта партия характеризуется повышенным содержанием кремнезёма (90,2% против 88,15% по данным У. Г. Дистанова; см. таблицу 1.1). Содержание полуторных окислов – в пределах среднего.
Опираясь на данные о содержании глинистого материала в породе, приводимые У. Г. Дистановым и другими авторами [25, 27], можно считать эти цифры косвенным подтверждением высокого содержания опалового кремнезёма в породе.
На основе полученных данных было рассчитано, что в 100 г диатомита в среднем содержится 2,83 г Al и 1,127 г Fe.
Выход алюминия из диатомита в зависимости от значения рН раствора извлечения
А) В ходе серии экспериментов было установлено, что нативный диатомит становится источником алюминия только при рН раствора извлечения менее 5,72 (±0,04) (интервал значений рНисх 1 – 10), а с уменьшением значения рН выход алюминия в раствор возрастает.
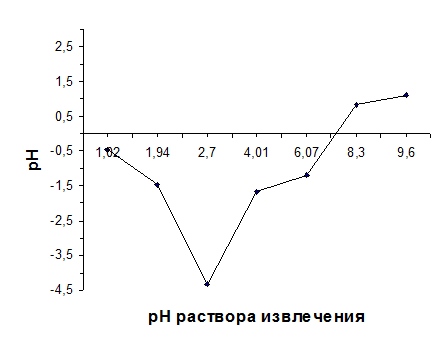
В) Для диатомита, прокалённого при 850°С, появление Al3+ в растворе отмечалось при рН<4,8.
Данные, отражающие зависимость CAl3+ в фильтрате от рН раствора извлечения, приведены в таблицах 2.6 и 2.7 и отражены на графиках, представленных на рисунках 2.1 и 2.2.
Таблица 2.6
Зависимость выхода алюминия от значения рН раствора извлечения для нативного диатомита
| рН исх | 1,02 | 1,94 | 2,70 | 4,01 | 5,72 | 6,07 | 8,30 | 9,60 |
| CAl3+, мг/см3 | 0,0175 | 0,0129 | 0,0033 | 0,0011 | 0,0000 | 0,0000 | 0,0000 | 0,0000 |
 |
Таблица 2.7
Зависимость выхода алюминия от рН раствора извлечения для диатомита, прокалённого при 850°С
| рН исх | 1,08 | 2,15 | 3,12 | 4,80 | 5,72 | 6,48 | 8,30 | 9,60 | |||
CAl3+, мг/см3 | 0,0186 | 0,0109 | 0,0038 | 0,0000 | 0,0000 | 0,0000 | 0,0000 | 0,0000 |
 |
В породе Al2O3 находится в связанном состоянии в составе кристаллической решётки глинистых минералов – гидрослюды и монтмориллонита.
Многочисленные исследования механизма взаимодействия слоистых алюмосиликатов с протонами показывают, что многие из них практически невозможно получить в моноионной Н+-форме, так как они самопроизвольно и немедленно становятся насыщенными Al [36, 98], то есть в них он занимает обменные позиции и способен переходить в раствор.
Д. С. Орлов, Т. А. Соколова и др. объясняют этот факт разрушением кристаллической решётки минералов в ходе реакций протонирования (см. рис. 1.8.). При действии на кристаллиты кислых водных растворов (в природе или лаборатории) катионы оснований Mex+ вытесняются и замещаются на ионы H+. В первую очередь протоны реагируют с гидроксильными группами октаэдрического слоя, находящимися на её боковых сколах. Но, имея достаточно малый радиус, они сравнительно легко мигрируют внутрь кристаллической решётки, а также могут взаимодействовать с ОН-группами, расположенными «на дне» гексагональных пустот тетраэдрической сетки, если глинистый минерал характеризуется подвижной решёткой. В гидрослюде калий с трудом вытесняется из своих обменных позиций, связь между пакетами достаточно прочная, поэтому при слабо- и среднекислом рН раствора взаимодействие с протонами ограничено поверхностными слоями кристаллической решётки.
В результате таких реакций ион Al3+, занимавший центральную позицию в алюмогидроксильном октаэдре, превращается в ион Al(OH)2+ или Al(OH)2+. Структура октаэдра нарушается, и ионы алюминия приобретают способность к обмену. Благодаря избытку ионов H+ и Cl‾ в растворах извлечения весь алюминий переходит в форму простого иона Al3+, и катионы K+ вытесняют его в раствор.
Лабораторные эксперименты и полевые исследования показали, что насыщение почвенного поглотительного комплекса обменным алюминием и развитие процесса подзолообразования связаны с разрушением алюмосиликатов даже при слабокислой реакции почвенного раствора [28, 140]. В результате истощения буферной ёмкости почв и снижения рН до величины менее 4,2 количество подвижного алюминия резко возрастает [4, 23], в том числе и за счёт вышеописанных процессов. Поскольку наши исследования показали значительный рост CAl3+ в фильтратах при 1<рНисх<4,01 (cм. Таблицу 2.6), то эти данные подтверждают предположение о том, что в сильнокислой почве алюмосиликатная составляющая диатомита может стать дополнительным источником обменного алюминия в почвенном растворе. При рН>5,72 не отмечалось его выщелачивания из породы, что также согласуется с литературными данными о поведении алюминия в почве.
При прокаливании диатомита происходит частичное разрушение алюмосиликатов и переход Al2O3 в неактивное состояние: он включается в состав силикатной плёнки на поверхности частиц, устойчивой к воздействию протонов [20, 45]. Поэтому выход алюминия из термоактивированного диатомита отмечался при меньшем, чем для нативного диатомита рН.
Выход железа из диатомита в зависимости от значения рН раствора извлечения
А) Выход железа из нативного диатомита также отмечался только при кислой реакции раствора извлечения (1<рНисх<5,72):
рНисх 3,32 – 5,72 – было зафиксировано появление ионов Fe3+ в фильтрате (при рН 4,50 их концентрация максимальна на данном интервале рН);
рНисх 3,32 – выхода железа из диатомита не отмечалось (CFe3+в фильтрате равна 0);
при рНисх <3,32 вновь начался выход железа из диатомита, с уменьшением значения рН он постоянно возрастал.
В) Порошок диатомита, прокалённого при 850°C, становится источником железа при меньших значениях рН раствора извлечения (<3,12). В более щелочной среде присутствие в фильтратах ионов Fe3+ не отмечалось.
Данные, отражающие зависимость CFe3+ в фильтрате от рН раствора извлечения, приведены в таблицах 2. 8 и 2.9 и отражены на графиках, представленных на рисунках 2.3 и 2.4.
Таблица 2.8
Зависимость выхода железа от значения рН раствора извлечения для нативного диатомита
| рН исх | 1,02 | 1,37 | 1,94 | 2,70 | 3,32 | 4,01 | 4,50 | 6,07 | 8,30 | 9,60 |
| CFel3+, мг/л | 11,07 | 3,56 | 0,79 | 0,40 | 0,00 | 0,59 | 0,79 | 0,00 | 0,00 | 0,00 |
 |
Таблица 2.9
Зависимость выхода железа от значения рН раствора извлечения для диатомита, прокалённого при 850°С
| рН исх | 1,08 | 2,15 | 3,12 | 4,80 | 5,72 | 6,48 | 8,30 | 9,60 | |||
CFel3+, мг/л | 4,74 | 1,18 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
 |
В диатомите железо заключено в кристаллической решётке алюмосиликатов и частично присутствует в виде свободных окислов. Силикатное железо появляется в кислом растворе вследствие разрушения глинистых минералов по вышеописанному механизму. При замещении водородом обменных катионов протоны взаимодействуют с дефектными тетраэдрами, в которых Si4+ замещён на Fe3+, или октаэдрами c Fe3+ вместо Al3+. Связи Fe—O или Fe—OH протонируются, железо занимает обменные позиции и приобретает способность переходить в раствор. Но свободные окислы железа начинают растворяться при более высоком значении рНисх, так как разрушение ионных и ионно-ковалентных связей кристаллической решётки требует большего количества энергии.
Способность ионов Fe3+ гидролизоваться выше, чем у ионов Al3+, поэтому можно предположить, что при 3,32 <рН<5,72 на процесс выхода железа из нативного диатомита накладывался процесс образования Fe3+ гидроксокомплексов Fe(OH)2+, Fe(OH)2+, Fe(OH)°, который не полностью подавлялся присутствием ионов Сl‾ и Н+ в растворе извлечения. В таком виде железо не определяется сульфосалициловым методом. Этим можно объяснить «горб» на графике, представленном на рисунке 2.3.
Ульрихом [48, 709] было показано, что при рН<3,2 в почве начинается растворение минералов гидроокисей и окисей железа, сопровождающееся появлением ионов Fe3+ в почвенном растворе. По данным наших исследований, резкое повышение выщелачивания железа из диатомита отмечалось при рН<3,32 (от нулевого выхода при рН 3,32 до концентрации Fe3+ в фильтрате 11,07 мг/л при рН 1,02), что в общем соответствуют закономерностям перехода железа в подвижное состояние с понижением рН среды, подробно описанными Л. А. Воробьёвой [28, 315].
Оранжевый цвет термоактивированного диатомита объясняется переходом всего содержащегося в нём железа в форму оксида железа (III). Он отчасти включается в состав силикатной плёнки на поверхности частиц, поэтому в фильтратах при рНисх>3.12 не отмечается присутствие ионов Fe3+. Но в сильнокислой среде (рН<3) Fe2O3 хорошо растворим, и на концентрацию Fe3+ в растворе извлечения не влияют сопутствующие реакции образования гидроксокомплексов. Поэтому в данных условиях из диатомита, прокалённого при 850°С, также интенсивно выщелачивается железо.
Относительный выход алюминия и железа из диатомита.
На основе данных о валовом химическом составе и выходе алюминия и железа из диатомита в зависимости от рН раствора извлечения, были рассчитаны показатели относительного выхода этих элементов (в пересчёте на 100 г породы и в массовых процентах) для нативного диатомита и диатомита, прокалённого при 850°С. Результаты приведены в таблицах 2.10, 2.11, 2.12 и 2.13 и на графиках, представленных на рисунках 2.5, 2.6, 2.7 и 2.8.
Таблица 2.10
Относительный выход алюминия из нативного диатомита в зависимости от значения рН раствора извлечения
| рН исх | 1,02 | 1,94 | 2,70 | 4,01 | 5,72 | 6,07 | 8,30 | 9,60 | |
| CAl3+, мг/см3 | 0,0175 | 0,0129 | 0,0033 | 0,0011 | 0,0000 | 0,0000 | 0,0000 | 0,0000 | |
| Относительный выход Al, | мг/100 г породы | 9,397 | 6,708 | 1,650 | 0,591 | 0,000 | 0,000 | 0,000 | 0,000 |
| масс. % | 0,332 | 0,237 | 0,058 | 0,021 | 0,000 | 0,000 | 0,000 | 0,000 | |
 |
 |
Таблица 2.11
Относительный выход алюминия из диатомита, прокалённого при 850°С, в зависимости от значения рН раствора извлечения
| рН исх | 1,08 | 2,15 | 3,12 | 4,80 | 5,72 | 6,48 | 8,30 | 9,60 | ||||
| CAl3+, мг/см3 | 0,0186 | 0,0109 | 0,0038 | 0,0000 | 0,0000 | 0,0000 | 0,0000 | 0,0000 | ||||
Относительный выход Al, | мг/100 г породы | 10,416 | 5,504 | 1,930 | 0,000 | 0,000 | 0,000 | 0,000 | 0,000 | |||
| масс. % | 0,368 | 0,194 | 0,068 | 0,000 | 0,000 | 0,000 | 0,000 | 0,000 | ||||
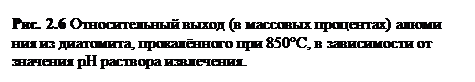 |
Таблица 2. 12
Относительный выход железа из нативного диатомита в зависимости от значения рН раствора извлечения
| рН исх | 1,02 | 1,37 | 1,94 | 2,70 | 3,32 | 4,01 | 4,50 | 6,07 | 8,30 | 9,60 | ||||
| CFe3+, мг/см3 | 11,07 | 3,56 | 0,79 | 0,40 | 0,00 | 0,59 | 0,79 | 0,00 | 0,00 | 0,00 | ||||
Относительный выход Fe, | мг/100 г породы | 5,944 | 1,957 | 0,004 | 0,002 | 0,000 | 0,003 | 0,004 | 0,000 | 0,000 | 0,000 | |||
| масс. % | 0,527 | 0,174 | 0,036 | 0,018 | 0,000 | 0,028 | 0,036 | 0,000 | 0,000 | 0,000 | ||||
 |
Таблица 2.13
Относительный выход железа из диатомита, прокалённого при 850°С, в зависимости от значения рН раствора извлечения
| рН исх | 1,08 | 2,15 | 3,12 | 4,80 | 5,72 | 6,48 | 8,30 | 9,60 | |
| CFe3+, мг/см3 | 4,74 | 1,18 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | |
| Относительный выход Fe, | мг/100 г породы | 2,650 | 0,006 | 0,000 | 0,000 | 0,000 | 0,000 | 0,000 | 0,000 |
| масс. % | 0,235 | 0,053 | 0,000 | 0,000 | 0,000 | 0,000 | 0,000 | 0,000 | |

 |
Буферное действие диатомита в системе твёрдая фаза – раствор
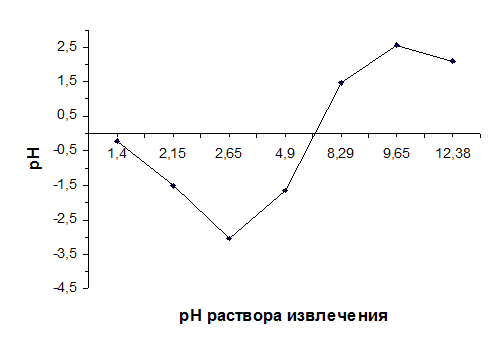
Проведённые эксперименты показали, что порошок диатомита влияет на реакцию раствора извлечения: он повышает значения рН кислых растворов, щелочных же, напротив, понижает. Буферное действие породы гораздо сильнее проявляется в кислой среде, причём нативный диатомит воздействует на величину рН раствора гораздо эффективнее диатомита, прокалённого при 850°С: для него максимальное значение │ΔрН│составило 4,34 при рНисх =2,7. Подвергнутый термообработке диатомит способен изменять рН раствора извлечения максимум на 1,95 единицы рН при рНисх=3,12.
При исследовании влияния порошка нативного диатомита на концентрацию Al3+ в растворах AlCl3 (исходное значение СAl3+ 0,0086 мг/см3) с различными значениями рН были получены данные, особенно ярко демонстрирующие его буферное действие в интервале значений рН 1,4-12,38, особенно в щелочной среде.
Результаты исследований приведены в таблицах 2.14, 2.15 и 2.16 и отражены на графиках, приведённых на рисунках 2.9, 2.10 и 2.11.
Таблица 2.14
Влияние порошка нативного диатомита на величину рН раствора извлечения (1 М раствора KCl c установленным значением рН)
| рН исх | 1,02 | 1,94 | 2,70 | 4,01 | 6,07 | 8,30 | 9,60 | |||
ΔрН | -0,45 | -1,48 | -4,34 | -1,66 | -1,19 | 0,82 | 1,12 |
 |
Таблица 2.15
Влияние порошка нативного диатомита на величину рН раствора извлечения (раствора AlCl3 c установленным значением рН)
| рН исх | 1,40 | 2,15 | 2,65 | 4,90 | 8,29 | 9,65 | 12,38 |
| ΔрН | -0,23 | -1,52 | -3,03 | -1,63 | 1,48 | 2,58 | 2,10 |
 |
 |
Таблица 2.16
Влияние порошка диатомита, прокалённого при 850°С,
на величину рН раствора извлечения (1 М раствора KCl c установленным значением рН)
| рН исх | 1,08 | 2,15 | 3,12 | 4,80 | 6,48 | 8,30 | 9,60 | |||
ΔрН | -1,71 | -0,98 | -1,95 | -1,07 | 0,30 | 0,57 | 0,85 |
 |
Буферное действие диатомита в кислой среде связано:
с адсорбцией протонов на сколах частиц алюмосиликатов и последующим разрушением их кристаллической решётки;
с адсорбцией ионов H+ на гидроксилированной поверхности опалового кремнезёма за счёт сил ионного притяжения вплоть до рН~2, при котором число заряженных центров на поверхности кремнезёма равно нулю (точка нулевого заряда).
Кроме того, Кольтгофом и Стенжером было показано, что сильнокислой среде гидроксилированная поверхность кремнезёма активно адсорбирует ионы Fe3+ и Al3+ с образованием кислотных групп на его поверхности [2, 237]. Реакция сопровождается вытеснением протонов и снижением концентраций исследуемых ионов в растворах. Можно предположить, что именно этим объясняется уменьшение величины ΔрН при рНисх<2,7.
Гидроксилированная поверхность кремнезёма имеет точку нулевого заряда при рН~2 [3, 913]. При более высоких значениях рН она проявляет слабые кислотные свойства, а при рН >~6 степень ионизации возрастает, и водород Si―OH группы легче диссоциирует. Переходя в раствор, протоны уменьшают степень его кислотности. Кроме того, при рН>7 – 8 растворимость кремнезёма начинает заметно расти [3, 66]. Как показано Р. Айлером, реакции гидратации и деполимеризации происходят с участием гидроксил-ионов (см. рис. 1.3), но при рН<8 образовавшийся силикат-ион гидролизуется с образованием молекул растворимого кремнезёма Si(OH)4 и ионов ОН‾ [2, 91], поэтому при рН<9,6 буферное действие породы, проявлялось слабее, чем в кислой среде. При рН>10,7 кремнезём весь растворяется с образованием силикат-ионов, что приводит к понижению концентрации гидроксил-ионов в растворе извлечения.
При термической активации происходит частичная дегидратация силанольной поверхности аморфного кремнезёма и для её регидратации требуется многодневное выдерживание образцов в нейтральном водном растворе [3, 915]. Это значительно ослабляет буферное действие опаловой составляющей диатомита, прокалённого при 850°С. Частичное разрушение алюмосиликатов снижает адсорбцию протонов с их участием и изменяет значение показателей выхода железа и алюминия. В целом диатомит, прокалённый при 850°С, обладает менее выраженным буферным действием по сравнению с нативным.
Влияние порошка нативного диатомита на концентрацию Al3+ в растворе AlCl3 в зависимости от значения рН раствора извлечения
В присутствии порошка нативного диатомита происходило заметное снижение концентрации алюминия в растворе AlCl3 c исходной CAl3+ 0,0086 мг/см3 и установленными значениями рН:
рНисх 1,4-4,9 – отмечалось значительное уменьшение содержания алюминия в фильтрате по сравнению с раствором извлечения вплоть до CAl3+ =0 при рН 4,9;
рНисх 4,9-12,4 – было зафиксировано присутствие ионов Al3+ в исследуемых растворах, с максимальной концентрацией 0,0038 мг/см3 при рН 8,29;
рНисх 12,38 – CAl3+ в фильтрате равна нулю.
Повышение концентрации исследуемого иона в фильтрате по срав- нению с раствором извлечения отмечалось только при рН<~2-2,5.
Данные, отражающие влияние нативного диатомита на значение CAl3+ в фильтрате в зависимости от рН раствора извлечения, приведены в таблице 2.17 и отражены на графике, приведённом на рисунке 2.12.
Таблица 2.17
Влияние нативного диатомита на значение CAl3+ в фильтрате в зависимости от значения рН раствора извлечения:
| рН исх | 1,40 | 2,15 | 2,65 | 4,90 | 8,29 | 9,65 | 12,38 |
| CAl3+, мг/см3 | 0,0164 | 0,0062 | 0,0010 | 0,0000 | 0,0038 | 0,0017 | 0,0000 |
 |
Резкое уменьшение концентрации исследуемого иона в фильтратах при рНисх<4,9 связано с тем, что его адсорбция на обменных позициях глинистых минералов и поверхности аморфного кремнезёма происходит быстрее, чем трансформация поверхностных слоёв кристаллической решётки алюмосиликатов, так как требует меньших затрат энергии. Адсорбировавшись на поверхности кристаллитов, ионы Al3+ затрудняют проникновение протонов внутрь, защищая решётку от разрушения. В кислой среде происходит наложение процессов поглощения Al3+ диатомитом и выщелачивания алюминия из его глинистой составляющей.
Ульрихом [48, 708] было показано, что при рН 4,2-5,0 вытеснение Al из кристаллических решёток минералов сопровождается образованием полимерных аквагидроксокомплексов алюминия, занимающих их обменные позиции. Можно предположить, что этим объясняется снижение поглощения диатомитом ионов Al3+ из раствора при рНисх 4,90-8,29. К тому же подщелачивание раствора извлечения способствует активизации гидролиза, а образующиеся в растворе катионы Al(OH)x3-x нельзя определить по выбранной нами методике. При более щелочной реакции среды весь алюминий раствора переходит в форму комплексных ионов переменной основности и активно поглощается порошком диатомита.
Выводы
В результате проведённых исследований можно сделать следующие выводы об особенностях поведения алюминия и железа инзенского диатомита в моделируемых условиях внешней среды:
Прокаливание диатомита при 850°С в течение 4 часов приводит к разрушению входящих в его состав слоистых алюмосиликатов и частично иммобилизует полуторные окислы.
В кислой среде порошок диатомита становится источником подвижных форм алюминия и железа, из прокалённого при 850°С диатомита выход исследуемых элементов в раствор происходит при более низком значении его рН.
Диатомит обладает буферным действием в широком диапазоне значений рН (1-12,4), при кислой реакции среды оно более выражено, чем при щелочной.
Нативный диатомит способен поглощать ионы Al3+ из раствора хлористого алюминия, при кислом рН падение концентрации ионов происходит только за счёт адсорбции на отрицательно заряженных поверхностях, в щелочной среде процесс осложняется гидролизом соли и поглощением аквагидроксокомплексов алюминия.
При рН растворах извлечения менее 5,72 нативный диатомит становится источником подвижного алюминия; в сильнокислой реакции среды (рН<4,0-4,5) его выход в раствор резко возрастает; из прокалённого при при 850°С диатомита выход алюминия происходит при более кислой реакции среды (рН<4,8).
Выщелачивание железа из породы имеет место при более низком значении рН (<3,32) не только за счёт глинистых
Список литературы
Айлер Р. Колллоидная химия кремнезёма и силикатов: Пер. с англ. – – М.: Госстройиздат, 1959. – 288 с.
Айлер Р. Химия кремнезёма: Пер. с англ. В 2-х частях, ч.1 – – М.: Мир, 1982. – 416 c.
Айлер Р. Химия кремнезёма: Пер. с англ. В 2-х частях, ч.2 – – М.: Мир, 1982. – 706 c.
Антонова Н. Б. Международный проект «Химическая бомба замедленного действия» // Проблемы окружающей среды и природных ресурсов. Вып. 2. – М.: ВИНИТИ, 1995. – С. 20 – 32.
Боброва Е. К., Бобров А. А. Минеральные новообразования диоксида кремния в растениях и почве // Минералогия и жизнь: биоминеральные взаимодействия. – Сыктывкар: Ин-т геологии Коми, 1996. – С. 50.
Быков В. Т. структура и адсорбционные свойства природных сорбентов // Природные сорбенты / Отв. ред. В. Т. Быков. – М.: Наука, 1967. – 187 с.
Вернадский В. В. Биогеохимическая роль алюминия и кремния в почвах // Труды по биогеохимии и геохимии почв. – М.: Наука, 1992. – 437 с.
Власов В. В., Дистанов У. Г. О составе кремнезёма кремнистых пород палеогена Среднего Поволжья // Доклады АН СССР. Т. 128. – №6. – – 1959. – С. 114 – 116.
Воронков М. Г. и др. Кремний и жизнь: биохимия, фармакология и токсикология соединений кремния. / М. Г. Воронков, Г. И. Зелчан, Э. Я. Лукевиц. – Рига: Зинанте, 1978. – 587 с.
Воронков М. Г., Кузнецов И. Г. Земная кремниевая жизнь // Химия и жизнь. – 1984. – №12. – С. 95 – 99.
Воронков М. Г., Кузнецов И. Г. Кремний в живой природе. – Новосибирск: Наука, 1984. – 157 с.
Геология и полезные ископаемые мезо-кайнозойских отложений Ульяновской области / Под ред. А. П. Дедкова. – Казань, 1964. -334 с.
Грег С., Синг К. Адсорбция, удельная поверхность, пористость: Пер. с англ. – М.: Мир, 1984. – 310 с.
Дистанов У. Г. Геолого-промышленные типы месторождений осадочных кремнистых пород СССР. Критерии их прогноза и поисков // Происхож- дение и практическое использование кремнистых пород: Сб. ст. АН СССР / Отв. редакторы В. Н. Холодов, В. И. Седнецкий. – – М.: Наука, 1987. – С. 157 – 167.
Добровольский В. В. Основы биогеохимии: Учеб. пособие для геогр., биол., с-х. спец. вузов. – М.: Высшая школа, 1998. – 413 с.
Ермолаев А. А. Кремний в сельском хозяйстве. – М.: Линф, 1992. – 256 с.
Жузе А. П. Кремнистые осадки в современных озёрах. // Геохимия кремнезёма: Сб. ст. АН СССР / Отв. ред. Н. М. Страхов. – – М.: Наука, 1966. – С. 301 – 314.
Иванов И. А. Диатомовая земля Ульяновской области // Вестник Среднего Поволжья. – 1925. – № 8 – 9. – С. 137 – 144.
Использование соединений кремния в сельском хозяйстве / В. М. Дьяков, В. В. Матыченков, В. А. Чернышев, Я. М. Аммосова // Актуальные вопросы химической науки и технологии и охраны окружающей среды. Вып. 7. – М.: НИИТЭХИМ, 1990. – 32 с.
Каглер М., Воборский Я. Фильтрование пива. – – М.: Агропромиздат, 1986. – 279 с.
Каледа Г. А. Основные черты эволюции кремнистого осадконакопления // Геохимия кремнезёма: Сб. ст. АН СССР / Отв. ред. Н. М. Страхов. – – М.: Наука, 1966. – С. 369 – 385.
Кельцев Н. В. Основы адсорбционной техники. М.: Химия, 1984. – 512 с.
Кнорре Д. Г., Крылова Л. Ф., Музыкантов В. С. Физическая химия: Учебник для биол. ф-тов университетов и пед. вузов. – 2-е изд., испр. и доп. – М.: Высшая школа, 1990. – 416 с.
Ковда В. А. Биогеохимия почвенного покрова / Отв. ред. О. В. Зонн. – – М.: Наука, 1985. – 263 с.
Кремнистые породы СССР / Отв. ред. У. Г. Дистанов. – Казань: Татарское книжное издательство, 1976. – 412 с.
Лопаткин А. А. Теоретические основы физической адсорбции. М.: Изд-во МГУ, 1983. – 344 с.
Надольский О. К. Диатомиты, трепелы и опоки Ульяновской области // Краеведческие записки Ульяновского краеведческого музея. Вып 2. – – 1958. – С. 319 – 329.
Орлов Д. С. Химия почв. – М.: Изд-во МГУ, 1992. – 400 с.
Оспанова Н. К. Нескелетное и скелетное биоминералообразование в истории Земли // Минералогия и жизнь: биоминеральные взаимодействия.. – Сыктывкар: Ин-т геологии Коми, 1996. – С. 58.
Петров В. П. Практическое значение кремнистых горных пород // Проис- хождение и практическое использование кремнистых пород: Сб. ст. АН СССР / Отв. редакторы В. Н. Холодов, В. И. Седнецкий. – – М.: Наука, 1987. –168 – 172 с.
Почвоведение / И. С. Кауричев , Н. П. Палос, И. Н. Розов и др.; Под ред. И. С. Кауричева. – 4-е изд., перер. и доп. – – М.: Агропромиздат, 1989. – 716 с.
Практикум по агрохимии / Б. А. Ягодин, И. П. Дерюгин, Ю. П. Жуков и др.; Под ред. Б. А. Ягодина. – М.: Агропромиздат, 1977. – 512 с.
Рохов Ю. Д. Мир кремния: Пер. с англ. – М.: Химия, 1990. – 147с.
Руководство по химическому и технологическому анализу воды. – – М.: Стройиздат, 1973. – 273 с.
Симонов Г. А. Органо-минеральные комплексы почв – проблемы диагностики // Минералогия и жизнь: биоминеральные взаимодействия. – Сыктывкар: Ин-т геологии Коми, 1996. – С. 62 – 63.
Соколова Т. А. Химические основы мелиорации кислых почв. – – М.: Изд-во МГУ, 1993. – 180 с.
Соколова Т. А., Дронова Т. Я. Изменение почв под влиянием кислотных выпадений. – М.: Изд-во МГУ, 1993. – 64 с.
Тарасевич Ю. И. Высокодисперсные минеральные адсорбенты // Журнал Всесоюзного химического общества. – 1989. – №2. – С. 61 – 69.
Химические основы буферности почв / Т. А. Соколова, Г. В. Мотузова, Т. Д. Обуховская. – М.: Изд-во МГУ, 1991. – 108 с.
Хмельницкий Р. А. Физическая и коллоидная химия: Учебник для с.-х. cпец. вузов. – М.: Высш. шк., 1988. – 400 с.
Холодов В. Н. Эволюция кремненакопления в истории Земли // Происхождение и практическое использование кремнистых пород: Сб. ст. АН СССР / Отв. редакторы В. Н. Холодов, В. И. Седнецкий. – – М.: Наука, 1987. – С. 31 – 49.
Шуменко С. И. Роль биогенного фактора в кремненакоплении // Происхождение и практическое использование кремнистых пород: Сб. ст. АН СССР / Отв. редакторы В. Н. Холодов, В. И. Седнецкий. – – М.: Наука, 1987. – С. 61 – 72.
Diatoms // http://silicasecchidisk.conncoll.edu/
Diatoms industrial use: diatomaceous earth as an insecticide // http://hjs.geol.uib.no/diatoms/
Hench L., West J. The sol – gel process // Chem. Rev. – 1990. – V. 90. – – P. 33 – 72.
Kemp A., Pearce R., Koizumi I. The role of mat-forming diatoms in the formation of Mediterranean sapropels // Nature. – 1999. – V. 398. – – P. 57 – 60.
Tracy A. Willareal, Cynthia Pilskan, Mark Brzezinski. Upward transport of oceanic nitrate by migrating diatom mats // Nature. – 1999. – V. 397. – – P. 423 – 424.
Ulrich B. Natural and anthropogenic components of soil acidification // Leit. Pflanzenern. Bodenkunde. – 1986. – V. 149. – P. 707 – 717.
Приложение
Каталог разведанных месторождений диатомита Ульяновской области.
| № | Наименование месторождения (района) | Местоположение месторождения | Геологический индекс | Запасы по категориям, тыс. м3 | Мощность продуктивного слоя, м | Мощность вскрыши, м | Краткая качественная характеристика | Области применения | Кем разведано | |||||||||||||||||||||||||
| 1 | Барышское (Барышский) | Против северного конца г. Барыш, на правом берегу р. Сыр-Барыш, в 0,5 км от ж.-д. Станции. | Pg1 sz1 | А – 1028, В – 825 (Протокол ТКЗ № 22 от 6. VI -61 г.) | От 7 до 25 (средняя 16,3) | От 1,1 до 10,8 (средняя 4,65) | Q от 0,816 до 1,176 (сред. по 5 aн. 0,933); H20 – 3,33 – 6,72 (4,95); SiO2 – 77,64 – 89,24 (80,90); Al203 – 5.57 – 8,16 (6,92); Fe2Оз – 2,06 – 6,53 (3,94); СаО – 0,06 – 1,3 (0,56); MgO – 0,48 – 1,16 (0,90); SO3 – 0,0 – 1,37 (0,26); п.п.п. – 3,65 – 6,62 (4,87). | Для производства легковесного строительного кирпича марки „75” кл. „А" (ГОСТ 6316-55). Разрабатывается Барышским кирпичным заводом | Л. А. Джиошвили, Куйбышевгеолстромтрест. 1955; Л. В. Мирошникова, КГРЭ, 1960 | |||||||||||||||||||||||||
| 2 | Вырыпаев-ское (“Гель-шерт”) (Инзен-ский) | В 0,8 км востоко-северо-восточнее с. Малые Озимки, в 2,5 км северо-восточнее ж.-д. ст. Вырыпаевка | Pg1 sz1 | А2 – 1190, В – 1900, C1 – 4380 | Средняя 19,7 | От 0,6 до 11,8 (средняя 4,4) | Q от 0,68 до 1,14 (сред. 0.84); Н2О – 2.57 – 5,84 (4,64); SiO2, – 78,34 – 84,88 (22,0); Al2O3 – 5.05 – 6:60 (5,9); Fe2O3 – 2,77 – 3,78 (3,13); ТiO2 – О.З6 – 0.54 (0,42); СаО – 0,3 – 1,3 (0,81); MgO – 0,69 – 1,17 (0,93); SO3 – 1,01 – 1,17 (0,28); п.п.п. – 3,14 – 8,14 (5,17); SiO2 раств. – 9,48 – 18,12 (12,35) | Для производства легковесного строительного кирпича, теплоизоляционных изделий. Не разрабатывается | К. Я. Бабич, Средне-Волжский ин-т прикладной минералогии, 1932; А. А. Дьяченко, КГРЭ. 1959 | |||||||||||||||||||||||||
| 3 | Вязовское (Инзенский) | В 2,5 км юго-восточнее с. Вязовка, в 4 – 5 км севернее ж.-д. разъезда Должниково, в 2,5 км от линии ж.д. | Pg1 sz1 | В – 4300 (Протокол ТКЗ от 13.V. -32 г.) | 14 | 2,72 | Q в порошке 0,447 – 0,560;SiO2 – 80,39 – 82,96; А12O3 – 6,02 – 6,68; Fe2O3 – 2,63 – 3,47;CaO – 0,84 – 0,98; MgO – 0,85 – 1,18; SO3 – 0,27 – 0,33; п.п.п. – 5,15 – 6,51; SiO2 раств. – 7 – 10 | Для производства легковесного строительного кирпича, теплоизоляционных изделий. Не разрабатывается | К. Я. Бабич, Средне-Волжский ин-т прикладной минералогии,
Популярное: Как выбрать специалиста по управлению гостиницей: Понятно, что управление гостиницей невозможно без специальных знаний. Соответственно, важна квалификация... Как построить свою речь (словесное оформление):
При подготовке публичного выступления перед оратором возникает вопрос, как лучше словесно оформить свою... Как распознать напряжение: Говоря о мышечном напряжении, мы в первую очередь имеем в виду мускулы, прикрепленные к костям ...  ©2015-2024 megaobuchalka.ru Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. (238)
|
Почему 1285321 студент выбрали МегаОбучалку... Система поиска информации Мобильная версия сайта Удобная навигация Нет шокирующей рекламы |
||||||||||||||||||||||||
(0.011 сек.)