 |
Главная |
Краткие теоретические сведения
|
из
5.00
|
Состояние данной массы газа характеризуется тремя величинами (параметрами): объемом V, давлением р и термодинамической температурой Т. В природе и технике, как правило, происходят изменения всех величин одновременно, но при этом соблюдается закономерность, выраженная уравнением состояния газа:
 (2.10)
(2.10)
где С =const
Для постоянной массы газа произведение объема на давление, деленное на термодинамическую температуру, есть величина постоянная.
Закон Бойля – Мариотта для изотермического процесса, т. е. процесса, протекающего при постоянной температуре (Т1 = Т2), является частным случаем объединенного газового закона:
 (2.11)
(2.11)
Т.е давление данной массы газа при постоянной температуре изменяется обратно пропорционально его объему при T=const.
Проверить эту зависимость экспериментально можно, используя прибор для изучения газовых законов (см. рис.2.9).
Прибор состоит из металлического гофрированного цилиндра переменного объема (сильфона) 1, манометра 2 и резинового шланга 3. Прикрепленная к сильфону демонстрационная шкала 4 позволяет измерять объем воздуха в цилиндре в условных единицах:
1 г/см2 =1атм= 101325 Па

Рисунок 2.9 – Экспериментальная установка
Порядок выполнения работы
1.Определить цену деления шкалы манометра.
2.Собрать установку по рисунку 2.9.
3.Измерить температуру воздуха Т1 в помещении, перевести градусы в Кельвины.
4.Определить по барометру атмосферное давление Ратм
5.Вращением винта 7 опустить крышку сильфона до 7 деления демонстрационной шкалы. С помощью кранов 5 и 6 зафиксировать в сильфоне некоторую массу воздуха V1 и замерить на манометре избыточное давление воздуха ΔР1. Перевести значение в (Па): 1атм= 101325 Па. Рассчитать давление Р1 по формуле  .
.
6.Снять показания V1, Т1 и данные занести в таблицу 2.8.
7.Не меняя массу газа, вращением винта 7 постепенно поднять крышку сильфона до 8 деления демонстрационной шкалы. Снять показания приборов ΔP2,V2,T2. Рассчитать давление Р2 по формуле  и данные занести в таблицу 2.8.
и данные занести в таблицу 2.8.
8.Не меняя массу газа, вращением винта 7 постепенно опустить крышку сильфона до 5,5 деления демонстрационной шкалы. Снять показания приборов ΔP3,V3,T3 и данные занести в таблицу 2.8. Рассчитать давление Р3 по формуле  .
.
9.Перенести сильфон в сосуд с горячей водой. Через 2-3 мин наступит тепловое равновесие, т. е. температуры воды и воздуха в сильфоне станут одинаковыми. Измерить температуру воды Т4
10.Не меняя объем воздуха V3 снять показания давления ΔР4 в и данные записать в таблицу 2.8
11.Рассчитать давление Р4 по формуле 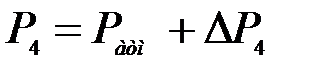 .
.
Таблица 2.8 – Экспериментальные данные
| № | Атмосферное давление Ратм=105Па | Избыточное давление ∆Р | Давление газа Р (Па) | Объем V усл.ед | Температура Т (К) |
| Сср | ΔС | ΔСср | ε% | |
| (атм) | (Па) | ||||||||||
| 1 |
|
|
| ||||||||
| 2 | |||||||||||
| 3 | |||||||||||
| 4 | |||||||||||
|
из
5.00
|
Обсуждение в статье: Краткие теоретические сведения |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы


