 |
Главная |
Какие металлы технически возможно (легче всего) получить из оксидов вакуумированием? Дайте обоснование ответа.
|
из
5.00
|
Что такое металлургический процесс? Перечислите типы металлургических процессов и дайте их краткую характеристику.
Металлургическим процессом получения цветных металлов назовем такие процессы (операции, технологические приемы), в которых проводится отделение компонентов пустой породы и примесей от ценных составляющих или изменение химического состава исходных материалов.
Классификация металлургических процессов – пиро и гидрометаллургические процессы.
Пирометаллургические процессы проводятся при высоких температурах чаще всего с полным и реже с частичным расплавлением материалов. Гидрометаллургические процессы - в водных средах при температурах максимально до ~300 °С.
Пиро: обжиг, плавка, дистилляция.
Основные гидрометаллургические процессы (стадии гидрометаллургических процессов): выщелачивание – избирательное растворение; очистка растворов от примесей; осаждение металла из раствора.
2. Опишите принцип построения изотермических разрезов потенциальной диаграммы системы Fe - O (в координатах Р O 2 - T ) в области температур, при которых оксиды железа и металл не образуют растворов. Т.е. в системе могут существовать только фаза чистого железа и фазы чистых оксидов – FeO , Fe 3 O 4 , Fe 2 O 3 .
Согласно правилу фаз для однофазной системы С = 2-2+2=2, для двухфазной С=2-3+2=1. Третья фаза - это газ, содержащий кислород. Газовую фазу необходимо обязательно учитывать при рассмотрении всех фазовых равновесий. Т.е. двухфазные системы яв-ся моновариантными, т.е. каждой температуре в этих областях соответствует постоянное давление кислорода по всей моновариантной области. В однофазных областях имеются две степени свободы и при постоянной температуре давление О2 резко возрастает от металлического края области гомогенности к кислородному. Если кроме температуры будет также задан и состав, т.е. использована последняя степень свободы, то система становится нонвариантной. Это значит, что для каждого состава, лежащего внутри области гомогенности вюстита, магнетита, гематита, твёрдого раствора кислорода в железе, жидких расплавов, существует только одно равновесное парциальное давление кислорода в данной системе и любое отклонение от него при постоянной температуре приведет к изменению состава вещества в ту или иную сторону, в зависимости от концентрации кислорода в газовой фазе.
От каких параметров зависит скорость осаждения штейновой капли в шлаке? Как измениться величина механических потерь меди со шлаком при увеличении температуры шлака? Поясните, пользуясь уравнением Стокса.
Согласно формуле Стокса скорость осаждения капли определяется:

◦ v - скорость осаждения капли, см/с;
◦ g - ускорение свободного падения, см/с2;
◦ ρ1 и ρ2 - соответственно плотность более и менее плотной жидкости, г/см3;
◦ µ1 и µ2 - вязкость более плотной и менее плотной жидкости, П;
◦ r - радиус осаждающейся капли, см.
Скорость осаждения зависит от плотности шлака и штейна, вязкости шлака и радиуса капли.
Как изменится величина механических потерь меди со шлаком при увеличении температуры шлака – у всех шлаков вязкость резко уменьшается с увеличением температуры, т.е. уменьшится вязкость шлака, отсюда следует что уменьшится скорость осаждения – уменьшится величина мех.потерь.
Дайте определение понятия “поверхностное натяжение жидкости”. Перечислите методики измерения поверхностного натяжения жидкостей при высоких температурах. Дайте краткое описание каждой методики. Опишите возможные проблемы при проведении измерений поверхностного натяжения расплавленных шлаков и штейнов.
Межфазное (поверхностное) натяжение жидкости – поверхностным натяжением называют величину, численно равную половине силы, которую необходимо приложить к тонкой пластинке единичной длинны, чтобы оторвать ее от поверхности жидкости.
Единицей измерения поверхностного натяжения в соответствии с определением σ является: 
Поверхностным натяжением называют энергию, необходимую для увеличения площади поверхности раздела фаз на единицу 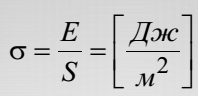
Анализ размерности показывает, что два определения совпадают: 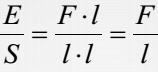
Метод лежащей капли (Метод Башфорта)
Суть метода заключается в измерении формы поверхности капли жидкости: лежащей на твердой поверхности - подложке. 
Метод лежащей капли (Метод Дорсея)
В 30-50-х годах был разработан ряд упрощенных методов обмера формы капли. Наиболее известный из этих методов принадлежит Дорсею.
По методу Дорсея требуется измерить лишь несколько величин, характеризующих форму капли

Метод максимального давления в газовом пузырьке (метод Кантора)
Сущность метода заключается в измерении давления, которое требуется для отрыва пузырька газа от поверхности тонкой трубки, помещенной в жидкость. В момент отрыва пузырька от капилляра работа по расширению газа в пузырьке сравняется с работой, затрачиваемой на образование новой поверхности жидкость-газ
Арасш=Апов
Тогда поверхностное натяжение можно рассчитать, как: 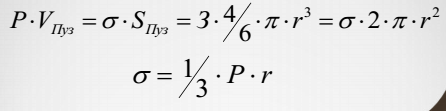
Удобным и достаточно надежным является метод максимального давления в газовом пузырьке. Его достоинством является хорошая теоретическая разработка, возможность исследования различных расплавов при высоких температурах, высокая точность.
Недостатки метода: 1.) необходимость подбора нейтральных по отношению к расплаву капилляров; 2.) разрушение капилляра не позволяет выбрать правильный расчетный радиус и понижает точность измерения.
Поверхностное натяжение шлакового расплава при повышении температуры возрастает. При достижении очень высоких температур, когда все комплексные ионы распадутся на составляющие, поверхностное натяжение шлака с ростом температуры будет снижаться, т. е. подчиняться закономерностям нормальных жидкостей.
5. Растворимость кобальта в шлаке, приведенном в контакт с чистым кобальтом, составила 0,6% (ат.) от массы шлака. Рассчитайте, растворимость кобальта при повышении давления кислорода в 10 раз. Принять, что кобальт растворяется в шлаке только в форме оксида. Коэффициент активности кобальта в шлаке, состав шлака и температура не меняются.
Решение:
Co+1/2 O2=CoO
Kp=a(CoO)/a(Co)* 
a(Co) = 1
Kp=exp(-∆G°/RT)
a(CoO)= Kp* 
a(CoO)=[CoO]
Кд=  →
→ 
CoO=Co2++O2-
X=  =S2 → Kp*(Po2)^1/2 · Kд= S2
=S2 → Kp*(Po2)^1/2 · Kд= S2
S= 
S1=0.6 % от массы шлака
p2=p1(O2)·10
S2=  =
= 
0.6 - 
X - 
X=1.78*0.6=1.068 %
S=1.068 % атм от массы шлака
При измерении плотности жидкости методом максимального давления в пузырьке величину заглубления капилляра увеличили с 2 см до 5 см, при этом столб манометрической жидкости (спирта) увеличился с 10 см до 25 см. Чему равна плотность исследуемой жидкости?
· Справочные данные: плотность спирта 0,8 г/см3,
· угол наклона манометра 30о.
h1 = 5 см
h2 = 2 см
P1-P2=ρжид·g·(h1-h2)
P=H·ρспирта·g → P1=H1·ρспирта·g H1=25*cos 30= 25*0.866=21.65
P2=H2·ρспирта·g H2=10 *cos 30= 10*0.866=8.66
(H1- H2) ·ρспирта·g = ρжид·g·(h1-h2)
(H1- H2) ·ρспирта = ρжид·(h1-h2)
ρжид=  =
= 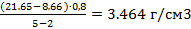
В закрытую ампулу загрузили тщательно перемешанные сульфид меди и оксид железа, из ампулы полностью откачали воздух и нагрели. Выдержали систему при определенной температуре до наступления равновесия. Сколько фаз (включая газовую) может максимально существовать в системе в равновесии? Дайте обоснование ответа
Если система находится в равновесии. то С=0. Число компонентов 3 = медь, железо, кислород. Температура и давление постоянны, а значит число изменяемых параметров =0. С=К-Ф, 0=К-Ф, 0=3-Ф. Число фаз = 3.
Какие металлы технически возможно (легче всего) получить из оксидов вакуумированием? Дайте обоснование ответа.
вакуумирование облегчает процесс диссоциации. больше вакуума - более упругий оксид, т.е. менее упругий оксид возможно получить из оксида вакуумированием.
9. Процесс окисления сульфида железа (FeS2) воздухом исследуется при помощи дифференциально-термического метода. Изобразите общий вид экспериментальной установки, общий вид кинетической кривой и опишите механизм процесса окисления пирита кислородом воздухом.
Дифференциальный термический анализ (ДТА) основан на регистрации разности температур исследуемого вещества и инертного образца сравнения при их одновременном нагревании или охлаждении. При изменении температуры в образце могут протекать процессы с изменением энтальпии, как например, плавление, перестройка кристаллической структуры, испарение, реакции дегидротации, диссоциации или разложения, окисление или восстановление. Такие превращения сопровождаются поглощением или выделением тепла, благодаря чему температура образца и эталона начинают различаться. Этим методом удается зафиксировать даже малые изменения температуры образца, благодаря конструкции прибора, а именно тому, что регистрирующие термопары от образца и эталона соединены навстречу друг другу. Повышенная чувствительность дифференциального метода позволяет исследовать образцы малого веса (до нескольких мг).

2FeS2+5O2=2FeO+4SO2
6FeO+O2=2Fe3O4
Что произойдет в фазовом состоянии системы, если в системе металл-оксид-газ изменить температуру (повысить или понизить)? Что произойдет, если изменить давление кислорода (увеличить или снизить)?
Равновесное Po2 которое
11. Выведите аналитический вид зависимости состава восстановительной газовой фазы (CO+СО2) от температуры (т.е. изменение содержания CO в газовой фазе от температуры или отношения CO / CO 2 ), который требуется для восстановления оксида MeO до Me, если металл не летучий.
МеО+CO=Me+CO2
Реакция восстановления зависит от температуры. Задав температуру мы получает точное значение CO/CO2.
Kp= 
∆G°= - RTlnKp → 
Воспользовавшись диаграммой Fe-S, определите, какие фазы и в каком количестве будут находиться в закрытой системе, если общее количество железа 112 гр, серы - 96 гр. Температура 900 К (627). Указание: объемом газа пренебречь (т.е. выходом серы в газ пренебречь).
112+96=208 – 100% Fe = 112 – 53.85% S = 96 – 46.15%
Fe1-xS x FeS2
43 46.15 53
FeS2=(46.75-43)/(53-43) = 3.75/100=0.375
Fe1-xS = (53-46.75)/(53-43)=6.25/10=0.625
13. Какие справочные данные необходимы для того, чтобы рассчитать равновесное давление серы в системе, содержащей Сu, Сu2S при температуре 1000 К? Проведите расчет равновесного PS 2 .
2Cu (тв)+ 1/2 S2 = Cu2S(тв)
Kp= 
∆G°= - RTlnKp →  = e (101064/8,31*1000)=е12,16=190994.5
= e (101064/8,31*1000)=е12,16=190994.5
∆G°= -131884+30,82*1000= -101064 Дж/моль
P(S)= 
a(Cu2S) = ?
a(Cu) = ?
14. Рассчитайте плотность газа, состоящего из 60% (вес.) H 2 и 40% (вес.) H 2 O при температуре 1500 К.
15. Исследуется процесс получения элементарной серы из SO 2 отходящих газов плавильного агрегата путем введения в газоход печи потока природного газа. Введите обозначения, напишите реакцию и запишите систему уравнений, определяющую выход элементарной серы (т.е. доля серы (в %), которая перейдет в результате химической реакции из SO 2 в S 2 ). Условно принимаете, что газ состоит только из SO 2 . Принять, что реакция протекает до равновесия.


Производство серы из SO2:
SO2 + CH4 ⇒ Sn + H2S + H2O + CO2 выход серы – 60-65%

|
из
5.00
|
Обсуждение в статье: Какие металлы технически возможно (легче всего) получить из оксидов вакуумированием? Дайте обоснование ответа. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

