|
Главная |
Уровни взаимосвязи между ката– и анаболизмом.
|
из
5.00
|
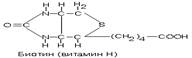
ВИТАМИН “Н” (БИОТИН, коэнзим R , антисеборейный)
|
|
Химическая природа: циклическое производное мочевины (имидазоловое и тиоэфирные кольца), боковая цепь которого представлена валериановой кислотой.
Коферментные формы: остаток биотина, связанный с -аминогруппой остатка лизина (биоцитин).
Участие в метаболизме: биотиновые ферменты катализируют два основных типа реакций:
а) реакции декарбоксилирования (с участием CO2 или HCO3-), сопряженные с распадом АТФ. Пример: ацетил-КоА и пируваткарбоксилазные реакции.
б) реакции транскарбоксилирования (без участия АТФ) – обмен карбоксильной группой между субстратами. Пример: обратимое превращение пировиноградной и щавелевоуксусной кислот.
в) имеют важное значение в синтезе ВЖК, белков, пуриновых нуклеотидов.
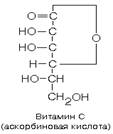
ВИТАМИН “С”(аскорбиновая кислота, антицинготный, антискорбутный)
|
|
Химическая структура: лактон кислоты со структурой, близкой к структуре L-глюкозы. Является сильной кислотой. Природные изомеры, обладающие витаминной активностью, относятся к L-ряду.
Коферментные формы: не известны.
Участие в метаболизме: биологическая роль связана с его участием в окислительно-восстановительных реакциях:
1. Витамин С, являясь сильным восстановителем, играет роль кофактора в реакциях окислительного гидроксилирования, что необходимо для окисления аминокислот пролина и лизина в оксипролин и в оксилизин в процессе биосинтеза коллагена.
2. Участвует в синтезе стероидных гормонов коры надпочечников (кортикостероидов).
3. Участвует в синтезе аминокислоты триптофана.
4. Способствует распаду тирозина и гемоглобина в тканях.
5. Необходим для всасывания железа.
6. Участвует в неспецифической иммунной защите организма.
Суточная потребность - около 100 мг в сутки.
Лечебная доза - до 1-2 г в сутки.
11. Катаболизм (диссимиляция) – расщепление крупных молекул до более простых веществ в результате окислительных процессов или процессов гидролиза и фосфоролиза, сопровождающееся разрывов ковалентных связей и высвобождением энергии.
Примеры: гликолиз, гликогенолиз, окисление жирных кислот.
12. Анаболизм (ассимиляция) – синтез сложных органических соединений из простых молекул в результате восстановительных процессов (как правило), сопровождающийся образованием связей между малыми молекулами в процессе синтеза более высокомолекулярных соединений и осуществляющийся с затратой энергии.
Примеры: глюконеогенез, синтез жирных кислот, фотосинтез у растений.
13. Отличия катаболизма от анаболизма:
| Отличительный признак | Катаболизм | Анаболизм |
| 1. Энергия | Высвобождается (экзергонический процесс) | Затрачивается (эндергонический процесс) |
| 2. Характер процесса | Окислительный | Восстановительный |
| 3. Локализация в клетке (компартментация метаболических процессов) | Цитоплазма, митохондрии, лизосомы | Цитоплазма клетки, рибосомы, ЭПС, КГ, ядро |
| 4. Обратимость реакций | Практически необратимы | В основном обратимы |
Также процессы катаболизма и анаболизма различаются по механизмам регуляции.
Уровни взаимосвязи между ката– и анаболизмом.
1. На уровне источников углерода (субстратов).
Продукты катаболизма – исходные субстраты для продуктов анаболизма. Важнейшие метаболиты, на уровне которых происходит пересечение метаболических путей: глюкозо-6-фосфат, пируват, ацетил-КоА.
2. На уровне восстановленных эквивалентов.
В процессе катаболизма происходит восстановление кофермента, который затем используется для анаболических процессов.
НАДФН – основной донор электронов в восстановительных реакциях биосинтеза. НАДН и ФАДН2 – основные акцепторы и переносчики электронов при окислении «топливных молекул».
3. На энергетическом уровне.
Катаболизм основных пищевых веществ сопровождается высвобождением энергии, которая может аккумулироваться в форме АТФ. При анаболических процессах происходит потребление АТФ с образованием АДФ и неорганического фосфата, используемых в реакциях диссимиляции для нового синтеза АТФ.
14. Макроэргические соединения (греч. makros большой + ergon работа, действие) – соединения, содержащие богатую энергией (макроэргическую) связь, при гидролизе которой изменения свободной энергии системы составляют более 5 ккал/моль.
Все известные М.с. содержат фосфорильную (—РО3Н2) или ацильную группы и могут быть описаны формулой Х—Y, где Х — атом азота, кислорода, серы или углерода, а Y — атом фосфора или углерода. Реакционная способность М.с. связана с повышенным сродством к электрону атома Y, что обусловливает высокую свободную энергию гидролиза макроэргической связи.
Примеры – фосфоенолпируват, 1,3-дифосфоглицерат, креатинфосфат, ацетил-КоА, АТФ, АДФ, пирофосфат.
15. Адениловая система – система адениловых нуклеотидов, которая включает в себя АТФ, АДФ, АМФ, неорганический фосфат и ионы Mg2+.
Роль адениловой системы:
1) играет центральную роль в энергообмене всех клеток
2) благодаря неустойчивости АТФ энергия ее концевой фосфоангидридной связи АТФ может использоваться на синтез фосфорилированных метаболитов, имеющих свободную энергию гидролиза меньше, чем АТФ. Обратное превращение АДФ в АТФ требует энергии.
Основные процессы, использующие энергию гидролиза АТФ:
1. Синтез различных веществ.
2. Активный транспорт (транспорт веществ через мембрану против градиента их концентраций). 30% от общего количества расходуемого АТФ приходится на Na+,К+-АТФазу.
3. Механическое движение (мышечная работа).
16. Реакции и процессы, сопряженные с гидролизом АТФ, в клетках животных и растений:
1. Клетки скелетных мышц (главная функция – мышечное сокращение) широко используют катаболизм энергосубстратов (анаэробный гликолиз у белых мышечных волокон и окислительное фосфорилирование в красных мышечных волокнах) и запасание выделяющейся энергии в форме АТФ – основного источника энергии для сокращения и расслабления.
2. Кардиомиоциты - постоянно сокращаются и расслабляются, поэтому используют аэробный катаболизм энергосубстратов и интенсивный синтез АТФ, имеют высокую окислительную способность.
3. Гепатоциты– основные структуры обезвреживания веществ и биосинтеза, обеспечивают энергосубстратами мозг, мышцы и другие ткани. Содержат много митохондрий, активно идут процессы микросомного окисления, глюконеогенез, синтез мочевины и кетоновых тел.
4. Нейроны– основная работа – транспорт ионов для генерации ПД. Интенсивный дыхательный обмен, высокая гликолитическая и окислительная способность. Не содержат запасов энергосубстратов, не окисляют жирные кислоты. Основной энергосубстрат – глюкоза.
5. Адипоциты– основное место запасания, мобилизации и синтеза триацилглицеролов. Основной источник глицерол-3-фосфата в процессах синтеза – глюкоза. Пентозофосфатный путь.
6. Клетки почек– выполняют осмотическую работу, активный мембранный транспорт в ходе образования мочи, поддержание кислотно-щелочного баланса. В качестве энергосубстратов используют жирные кислоты, лактат, кетоновые тела. Идет интенсивное образование ионов аммония и глюконеогенез.
7. Эритроциты– транспорт О2 и СО2. Не имеют митохондрий, получают энергию путем анаэробного гликолиза. Синтезируют 2,3-дифосфоглицерат, способствующий высвобождению О2 из гемоглобина в тканях.
17. Механизмы образования АТФ в клетках животных и растений:
а) Фотосинтетическое фосфорилирование – синтез АТФ у растений за счет квантов солнечной энергии.
б) Окислительное фосфорилирование – синтез АТФ за счет энергии, выделяющейся при окислении водорода субстрата кислородом с участием дыхательной цепи. Основной способ синтеза АТФ для большинства клеток.
в) Субстратное фосфорилирование – синтез АТФ за счет энергии гидролиза макроэргической связи субстрата (пример: фосфоглицераткиназная и пируваткиназная реакции анаэробного гликолиза).
Для митохондрий характерно ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ.
18. Окислительное фосфорилирование – синтез АТФ за счет энергии, выделяющейся при окислении водорода органических субстратов кислородом с участием дыхательной цепи.
Основные положения хемиосмотической теории Митчелла:
а) Энергия, выделяющаяся при транспорте электронов I, III и IV комплексами дыхательной цепи, используется для перекачивания протонов в межмембранное пространство, генерируя градиент pH.
б) Обратный поток протонов по протонным каналам АТФ-синтазы в матрикс обеспечивает энергией головку АТФ-синтазы для синтеза АТФ.
19. Метаболический путь – последовательность химических превращений конкретного вещества в клетке:
а) Циклический метаболический путь – замкнутая последовательность химических превращений, приводящая в итоге к регенерации исходного вещества. Примеры: цикл лимонной кислоты, орнитиновый цикл мочеобразования Кребса.
б) Линейный метаболический путь – линейная последовательность химических реакций. Примеры: гликолиз, пентозофосфатный путь.
Регуляторные ферменты – ферменты, регулирующие метаболизм клеток, которые обычно располагаются либо в начале метаболических путей, либо в местах ключевых разветвлений, где сходятся два и большее число путей и которые катализируют в клетке либо практически необратимые реакции, либо реакции, протекающие наиболее медленно. Примером может служить фосфофруктокиназа-1, ацетил-КоА-карбоксилаза, пируваткарбоксилаза, протеинкиназа.
|
из
5.00
|
Обсуждение в статье: Уровни взаимосвязи между ката– и анаболизмом. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы