 |
Главная |
Размеры атомов. Связь размера атома с положением в периодической системе элементов. Понятие об ионах
|
из
5.00
|
Содержание
1. Классы неорганических веществ
2. Размеры атомов. Связь размера атома с положением в периодической системе элементов. Понятие об ионах
3. Водородная связь
4. Энтальпия
5. Растворы электролитов. Понятие об электролитической диссоциации
6. Мембранные сенсоры и биосенсоры
7. Литература
Классы неорганических веществ
Классификация неорганических веществ прошла долгий путь развития и складывалась постепенно, начиная с первых опытов алхимиков.
Химические элементы делятся на элементы с металлическими и неметаллическими свойствами.
Многие элементы в соответствии с Периодическим законом проявляют одновременно в той или иной мере свойства металлов и неметаллов. Такие элементы называют амфотерными.
В силу большого своеобразия химических свойств особо выделяют благородные газы - элементы VIII A-группы.
Соответственно подразделению элементов классифицируют простые (одноэлементные) вещества - формы существования элементов в свободном виде.
Классификация сложных веществ (двух- или многоэлементных веществ) по составу основана на наличии в соединении самого распространенного в природе элемента кислорода и на самом распространенном соединении кислорода - воде.
Кислород образует соединения со всеми элементами, кроме He, Ne и Ar. Среди производных кислорода только соединения со фтором (например дифторид кислорода OF2) содержат кислород в положительной степени окисления; практически все остальные соединения кислорода - это оксиды.
При реакции оксидов с водой (напрямую или косвенным путем) получаются гидроксиды - кислотные, основные или амфотерные.
Гидроксиды разных типов реагируют между собой и образуют кислородсодержащие соли, состоящие из катионов и анионов (кислотных остатков). Такие соли называют средними. Если соли содержат два химически разных катиона или два разных кислотных остатка, их называют соответственно двойными и смешанными.
При наличии в составе кислотного остатка атомов водорода, способных к дальнейшему замещению катионами, соли называются кислыми, при наличии гидроксогрупп OH− (или оксогрупп O2−) - основными солями.
Еще один обширный класс сложных веществ - бинарные соединения.
Размеры атомов. Связь размера атома с положением в периодической системе элементов. Понятие об ионах
Атом состоит из положительно заряженного ядра и вращающихся вокруг него отрицательно заряженных частиц‑электронов, составляющих его электронную оболочку. Сумма зарядов электронов равна по модулю положительному заряду ядра, поэтому атом в целом представляет собой электронейтральную систему. Размеры атома определяются размерами его электронной оболочки и составляют величину порядка 10–8 см.
Массы различных элементов находятся в пределах от 1,6×10–24 до 4×10–22 г.
В ядерной физике масса, заряд и энергия измеряются специальными единицами. Масса измеряется в атомных единицах массы (а.е.м.). За атомную единицу принята 1/12 массы атома углерода, равная 1,66057×10–30 г. Элементарным называется заряд, который равен по абсолютной величине заряду электрона: 1 е =1,601×10‑19 Кал = 4,802×10‑10 в единицах CГСE. Энергия измеряется в электрон-вольтах (эВ). Электрон‑вольт соответствует энергии, которую приобретает электрон при движении в электрическом поле с разностью потенциалов в 1В (Вольт): 1эВ = 3,8276 ×10‑20 кал (калорий). В ядерной физике часто применяется единица, в миллион раз большая:
МэВ = 106 эВ = 1,602×10‑6 эрг = 3,83×10‑14 кал = 1,60219·10‑13 Дж.
Электроны в оболочке атома расположены слоями. Число электронных слоев равно порядковому номеру химического элемента в периодической системе элементов Д.И. Менделеева.
В первом, ближайшем к ядру слое К вращается не более двух электронов. В следующем за ним слое L – не более 8, в слое М – не более 18, а в четвертом слое N – не более 32 электронов. Таким образом, наибольшее число электронов этих слоев равно удвоенному квадрату номера слоя Z = 2n2. В последующих слоях это правило нарушается, и количество электронов может составлять: в пятом слое О – от 1 до 29, в шестом слое Р – от 1 до 9 и в дополнительном (последнем) слое Q – не более 2 электронов.
Каждый атом существует лишь в определенных дискретных энергетических состояниях, соответствующих строго определенному значению его энергии.
Переход атома из одного энергетического состояния в другое сопровождается поглощением или излучением энергии. В обычном же состоянии атом не излучает.
Если одному из электронов при столкновении с какой-либо частицей извне будет сообщена некоторая дополнительная энергия, то он перейдет на более удаленную орбиту того слоя, которому соответствует его новая энергия. В этом случае атом приходит в возбужденное состояние, и тогда один из электронов внешнего слоя перескакивает на освободившееся место. Через короткое время (порядка 10‑8 с) атом возвращается в нормальное состояние, испуская при этом видимый свет, ультрафиолетовое или рентгеновское излучение.
Ион (греч. ιоν — «идущий») — электрически заряженная частица (атом, молекула), образующаяся, обычно, в результате потери или присоединения одного или нескольких электронов атомами или молекулами.
Заряд иона кратен заряду электрона. Понятие и термин ион ввёл в 1834 Майкл Фарадей, который, изучая действие электрического тока на водные растворы кислот, щелочей и солей, предположил, что электропроводность таких растворов обусловлена движением ионов. Положительно заряженные ионы, движущиеся в растворе к отрицательному полюсу (катоду), Фарадей назвал катионами, а отрицательно заряженные, движущиеся к положительному полюсу (аноду) — анионами.
В виде самостоятельных частиц они встречаются во всех агрегатных состояниях вещества — в газах (в частности, в атмосфере), в жидкостях (в расплавах и в растворах), в кристаллах и в плазме (в частности в межзвёздном пространстве).
Являясь химически активными частицами, ионы вступают в реакции с атомами, молекулами и между собой. В растворах ионы образуются в результате электролитической диссоциации и обусловливают свойства электролитов.
Водородная связь
Водородная связь — разновидность невалентного взаимодействия между атомом водорода H, ковалентно связанным с атомом A группы A-H молекулы RA-H и электроотрицательным атомом B другой молекулы (или функциональной группы той же молекулы) BR. Результатом таких взаимодействий являются комплексы RA-H•••BR различной степени стабильности, в которых атом водорода выступает в роли мостика, связывающего фрагменты RA и BR. Атом водорода, соединенный с атомом сильно электроотрицательного элемента, способен к образованию еще одной химической связи с подобным атомом водорода. Эта связь называется водородной. Возникновение водородной связи можно в первом приближении объяснить действием электростатических сил. Атом с большой электроотрицательностью, например, фтор в молекуле HF смещает на себя электронное облако, приобретая значительный эффективный отрицательный заряд, а ядро атома водорода (протон) почти лишается электронного облака и приобретает эффективный положительный заряд. Между протоном атома водорода и отрицательно заряженным атомом фтора соседней молекулы возникает электростатическое притяжение, что и приводит к образованию водородной связи. Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, т.е. их объединение в димеры или полимеры. Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак. Водородная связь в значительной мере определяет свойства и таких биологически важных веществ как белки и нуклеиновые кислоты.
Энтальпия
Энтальпиия, также тепловая функция и теплосодержание — термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц.
Если термомеханическую систему рассматривать как состоящую из макротела (газа) и поршня с грузом Р = p S, уравновешивающего давление газа р внутри сосуда, то такая система называется расширенной.
Энтальпия или энергия расширенной системы Е равна сумме внутренней энергии газа U и потенциальной энергии поршня с грузом
Eпот = pSx = pV
H = E = U + pV
Таким образом, энтальпия в данном состоянии представляет собой сумму внутренней энергии тела и работы, которую необходимо затратить, чтобы тело объёмом V ввести в окружающую среду, имеющую давление р и находящуюся с телом в равновесном состоянии. Энтальпия системы H — аналогично внутренней энергии — имеет вполне определенное значение для каждого состояния, т. е. является функцией состояния. Следовательно, в процессе изменения состояния
ΔH = H2 − H1
Энтальпией системы удобно пользоваться в тех случаях, когда в качестве независимых переменных, определяющих состояние системы, выбирают давление р и температуру Т
H = H(p,T)
Энтальпия — величина аддитивная, т. е. для сложной системы равна сумме энтальпий её независимых частей
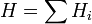 .
.
Энтальпия определяется с точностью до постоянного слагаемого, которому в термодинамике часто придают произвольные значения (например, при расчете и построении тепловых диаграмм). При наличии немеханических сил величина энтальпии системы равна
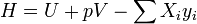
где Xi — обобщённая сила; yi — обобщённая координата.
Изменение энтальпии не зависит от пути процесса, так как изменение объёма при постоянном давлении определяется только начальным и конечным состоянием системы. Если система каким-либо путём возвращается в исходное состояние (круговой процесс), то изменение любого её параметра равно нулю, а отсюда ΔU = 0 и ΔH = 0.
|
из
5.00
|
Обсуждение в статье: Размеры атомов. Связь размера атома с положением в периодической системе элементов. Понятие об ионах |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

