 |
Главная |
Рентгеноэлектронная спектроскопия
|
из
5.00
|
Содержание
Введение
. Эксперементальные методы
Рентгеноэлектронная спектроскопия
1.2 Ифракрасная спектроскопия
1.3 Дифракционные методы
. Теоретические методы
Полуэмпирические методы
Неэмпирические методы
Кванто-механические методы
Метод Хюккеля
Заключение
Список использованных источников
ВВЕДЕНИЕ
В современной органической химии большое значение имеют различные физические методы исследования. Их можно разделить на две группы. К первой группе относятся методы, позволяющие получать различные сведения о строении и физических свойствах вещества, не производя в нем никаких химических изменений. Из методов этой группы, пожалуй, наибольшее применение получила спектроскопия в широком диапазоне областей спектра - от не слишком жестких рентгеновских лучей до радиоволн не очень большой длины. Ко второй группе относятся методы, в которых используются физические воздействия, вызывающие химические изменения в молекулах. В последние годы к ранее применявшимся широкоизвестным физическим средствам воздействия на реакционную способность молекулы прибавились и новые. Среди них особое значение имеют воздействия жестких рентгеновских лучей и потоков частиц больших энергий, получаемых в атомных реактора
Целью данной курсовой работы является - узнать о методах исследований строения молекул.
Задача курсовой работы:
выяснить виды методов и изучить их.
ЭКСПЕРЕМЕНТАЛЬНЫЕ МЕТОДЫ
Рентгеноэлектронная спектроскопия
Метод исследования электронного строения химического соединения, состава и структуры поверхности твердых тел <http://www.xumuk.ru/encyklopedia/2/4324.html>, основанный на фотоэффекте с использованием рентгеновского излучения. При облучении вещества происходит поглощение рентгеновского кванта hv (h-постоянная Планка, v-частота излучения), сопровождающееся эмиссией электрона <http://www.xumuk.ru/encyklopedia/2/5311.html> (наз. фотоэлектроном) с внутренних или внешних оболочек атома <http://www.xumuk.ru/encyklopedia/401.html>. Энергия связи электрона <http://www.xumuk.ru/encyklopedia/2/5311.html> Есв в образце в соответствии с законом сохранения энергии <http://www.xumuk.ru/encyklopedia/2/4157.html> определяется уравнением: Есв = hv-Eкин, где Eкин-кинетическая энергия фотоэлектрона. Значения Есв электронов <http://www.xumuk.ru/encyklopedia/2/5311.html> внутренних оболочек специфичны для данного атома <http://www.xumuk.ru/encyklopedia/401.html>, поэтому по ним однозначно можно определить состав хим. соединения. Кроме того, эти величины отражают характер взаимодействия исследуемого атома <http://www.xumuk.ru/encyklopedia/401.html> с другими атомами <http://www.xumuk.ru/encyklopedia/401.html> в соединении, т.е. зависят от характера химической связи. Количеств состав образца определяют по интенсивности I потока фотоэлектронов. Принципиальная схема прибора для РЭС-электронного спектрометра-показана на рисунке 1. Образцы облучают рентгеновским излучением из рейтгеновской трубки либо синхротронным излучением <http://www.xumuk.ru/encyklopedia/2/4085.html>. Фотоэлектроны попадают в анализатор-прибор, в котором из общего потока выделяются электроны <http://www.xumuk.ru/encyklopedia/2/5311.html> с определенной Екин. Сфокусировать монохроматический поток электронов <http://www.xumuk.ru/encyklopedia/2/5311.html> из анализатора направляется в детектор, где определяется его интенсивность I. В рентгеноэлектронном спектре разным атомам <http://www.xumuk.ru/encyklopedia/401.html> соответствуют свои максимумы интенсивности (рисунок 2), хотя некоторые максимумы могут сливаться, давая одну полосу с увеличенной интенсивностью. Линии спектра обозначают следующим образом: рядом с символом элемента называют исследуемую орбиталь <http://www.xumuk.ru/encyklopedia/2/3124.html> (напр., запись Cls означает, что регистрируют фотоэлектроны с орбитали 1s углерода <http://www.xumuk.ru/encyklopedia/2/4636.html>).
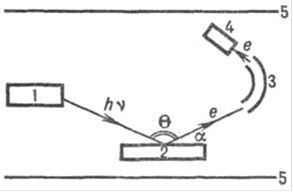
Рисуник 1- Схема электронного спектрометра: 1-источник излучения; 2-образец; 3- анализатор; 4-детектор; 5-экран для защиты от магнитного поля
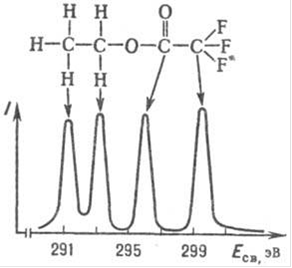
Рисунок 2- Рентгеноэлектронный спектр Сls этилтрифторацетата
РЭС позволяет исследовать все элементы, кроме Н, при содержании их в образце ~ 10-5 г (пределы обнаружения элемента с помощью РЭС 10-7-10-9 г). Относительное содержание элемента может составлять доли процента. Образцы могут быть твердыми, жидкими или газообразными. Величина Eсв электрона <http://www.xumuk.ru/encyklopedia/2/5311.html> внутренней оболочки атома <http://www.xumuk.ru/encyklopedia/401.html> А в химических соединениях зависит от эффективного заряда qА на этом атоме <http://www.xumuk.ru/encyklopedia/401.html> и электростатического потенциала U, создаваемого всеми другими атомами <http://www.xumuk.ru/encyklopedia/401.html> соединения: Eсв = kqА + U, где k-коэффициент пропорциональности.
Для удобства в РЭС вводят понятие химического сдвига Eсв, равного разности между Есв в исследуемом соединении и некотором стандарте. В качестве стандарта обычно используют значение Eсв, полученное для кристаллической модификации элемента; например, стандартом при исследовании соединении S служит кристаллическая сера <http://www.xumuk.ru/encyklopedia/2/4017.html>. Поскольку для простого вещества qА 0 и U = 0, то Eсв = kqA + U. Таким образом, химический сдвиг свидетельствует о положительном эффективном заряде на изучаемом атоме <http://www.xumuk.ru/encyklopedia/401.html> А в химическом соединении, а отрицательный об отрицательном заряде, причем значения Eсв пропорционально эффективному заряду на атоме <http://www.xumuk.ru/encyklopedia/401.html>. Поскольку изменение эффективного заряда на атоме <http://www.xumuk.ru/encyklopedia/401.html> А зависит от его степени окисления <http://www.xumuk.ru/encyklopedia/2/4206.html>, характера соседних атомов <http://www.xumuk.ru/encyklopedia/401.html> и геометрической структуры соединения, по Eсв можно определять природу функциональных групп, степень окисления <http://www.xumuk.ru/encyklopedia/2/4206.html> атома <http://www.xumuk.ru/encyklopedia/401.html>, способ координации лигандов и т.д. Энергии связи электронов <http://www.xumuk.ru/encyklopedia/2/5311.html> функциональных атомных групп слабо зависят от типа химического соединения, в котором находится данная функциональная группа.
|
из
5.00
|
Обсуждение в статье: Рентгеноэлектронная спектроскопия |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

