|
Главная |
Наиболее известные яды
|
из
5.00
|
Из истории и художественной литературы известно, что в прошлом в качестве ядов злоумышленники широко использовали мышьяк, сулему, цианистый калий. Нужно сразу отметить, что в организм человека яды могут попасть не только по злому умыслу, но и в процессе своей профессиональной деятельности при нарушении условий труда и техники безопасности. Как уже было сказано, в малых количествах даже самые страшные яды могут быть полезны человеку и потому применяются в медицине. Яды также используют для борьбы с грызунами, для протравы семян и т.д. Полностью отказаться от ядов пока человек не может. Поэтому полезно знать их опасность, симптомы отравления и меры первой помощи.
Мышьяк
Мышьяк попадает в организм чаще всего не в элементной форме, а в виде соединений. Хроническое отравление (при поступлении в организм в малых дозах, но в течение длительного времени) проявляется в раздражении слизистых оболочек глаз и верхних дыхательных путей. Кроме того, появляется непроходящий насморк, кашель, конъюнктивит, кровохарканье, а в более тяжелых случаях присоединяются симптомы поражения центральной нервной системы. Соединения мышьяка оказывают раздражающее действие на кожу. При длительных действиях они могут вызвать образование злокачественных опухолей.
При остром отравлении, т.е. при попадании в желудок в большой дозе, появляется металлический привкус во рту, наблюдается затруднение глотания, вызывается рвота и проявляются сильные боли в животе с последующим поносом. При очень сильных отравлениях может развиться паралитическая форма - судороги различных мышц, потеря сознания, паралич сосудодвигательного и дыхательного центров.
Все эти симптомы вызваны тем, что соединения мышьяка являются сильными капилляротоксическими ядами. Они вызывают увеличение проницаемости сосудистых стенок и паралич капилляров. Кроме того, при отравлениях мышьяком нарушаются обмен веществ и функция центральной и периферической нервной системы.
При оказании помощи в случаях отравления соединениями мышьяка проводят промывание желудка теплой водой и взвесью в воде оксида магния (магнезии), вводят антидоты (см. далее), немедленно и обязательно госпитализируют.
Следует отметить, что понос - частая реакция организма на отравление. С древних времен при отравлениях широко использовали лекарства, вызывающие рвоту, понос, усиленное мочеотделение, потоотделение, слюновыделение. Этими путями стремились вывести из организма ядовитые вещества.
Следует также отметить, что непосредственный контакт соединений мышьяка с тканями, в частности As2O3, приводит к их гибели без предшествующего раздражения. Иными словами, гибель тканей протекает почти безболезненно. Это свойство соединений мышьяка и, в частности Аs2O3, используют в стоматологической практике для удаления нейронов (нервной ткани). Для этого на обнаженную пульпу зуба (ткань, содержащую нервы, кровеносные и лимфатические сосуды) наносят кусочек пасты величиной с булавочную головку. Содержащийся в ней Аs2O3 диффундирует в пульпу и через 24...48 ч нерв погибает.
Соединения селена также ядовиты и по этим свойствам напоминают соединения мышьяка. Неспроста в периодической системе Д.И. Менделеева эти два элемента находятся рядом.
Ртуть
Ртуть - при комнатных температурах легкоподвижная жидкость. Для металлов она относительно легко испаряется, а пары ртути чрезвычайно ядовиты. Поскольку ртуть содержится в медицинских термометрах, то с нею человек может столкнуться в домашних условиях. Разбитый термометр и вылившаяся, но не собранная ртуть может представить опасность для здоровья человека. Характерными признаками ртутного отравления является слюнотечение, своеобразное покраснение десен и размягчение зубов. Появляется тяжелое нервное расстройство: головная боль, нарушение пищеварения, дрожание рук и головы. При слабом отравлении появляется вялость, бессонница, ослабление памяти.
Восприимчивость к отравлению ртутью различных людей может весьма сильно отличаться. Некоторые люди испытывают симптомы отравления даже от металлических зубных пломб, состоящих из амальгамированной меди.
Некоторые соединения ртути также чрезвычайно ядовиты. Известно, что ионы ртути (II) способны прочно соединяться с белками. Ядовитое действие хлорида ртути (II) HgCl2 (сулемы) проявляется прежде всего в некрозе (омертвлении) почек и слизистой оболочки кишечника. В результате ртутного отравления почки теряют способность выделять из крови продукты жизнедеятельности организма.
Интересно, что хлорид ртути (I) Hg2Cl2 (древнее название каломель) безвреден для организма человека. Вероятно, это объясняется чрезвычайно низкой растворимостью соли, в результате чего ионы ртути не попадают в заметных количествах в организм.
При хроническом отравлении ртутью и ее соединениями проявляются нервные нарушения, бывает повышенная психическая возбудимость, вегетативные сдвиги, проявляющиеся в непроизвольном движении мышц лица с его покраснением. Отравление проявляется в потливости и красном дермографизме (при слабом нанесении штриха на коже появляется красная полоса). При хроническом отравлении появляется так называемый ртутный тремор - вначале мелкое дрожание пальцев рук, затем резкое усиление, дрожание всего тела, непроизвольные движения.
При остром отравлении появляется повышение температуры, озноб, воспаление дыхательных путей и легких; наблюдается слюнотечение, набухание и слюноточивость десен. Все это сопровождается потерей аппетита, тошнотой, рвотой, болями в животе, кровянистым поносом, головными болями, расстройством речи, изменением походки.
Лечение при отравлении ртутью включает покой, прием антидотов и витаминов. Рекомендуют принимать яичный белок и молоко. Содержащиеся в этих продуктах белки связывают ртуть, локализуют ее в полости желудка, а затем выводят из организма.
Цианистый калий и синильная кислота
Цианистый калий (цианид калия) KCN - соль синильной кислоты HCN. Оба соединения являются быстродействующими и сильными ядами. Ядовитые свойства синильной кислоты начали использовать задолго до того, как она была идентифицирована и выделена в чистом виде. Отметим, что в небольших количествах синильная кислота часто встречается в растительном мире. Наиболее известен в этом отношении горький миндаль. В семенах миндаля содержится органическое соединение амигдалин, который расщепляется на виноградный сахар, бензальдегид (масло горького миндаля) и синильную кислоту. Расщепление протекает под действием имеющегося в горьком миндале энзима - эмульсина. Этот процесс протекает самопроизвольно без вмешательства человека. Таким образом, в семенах миндаля, персика, абрикоса, вишни и других растений в небольших количествах всегда имеется синильная кислота. Современные клинические наблюдения показали, что отравление со смертельным исходом наступает после употребления около 100 очищенных ядер абрикосов. Древнегреческие жрецы умели извлекать синильную кислоту из листьев персика. Возможно, теперь Вам станут понятными такие выражения, как «наказание персиком», «не преступай - иначе умрешь от персика». Для человека смертельная доза синильной кислоты составляет всего лишь 50 мг.
При остром отравлении синильной кислотой и ее солями теряется сознание, наступает паралич дыхания и сердца. На начальной стадии отравления человек испытывает головокружение, ощущение давления во лбу, острую головную боль, учащенное дыхание, сердцебиение. Первая помощь при отравлении синильной кислотой и ее солями - свежий воздух, кислородное дыхание, тепло. Противоядиями являются нитрит натрия NaNO2 и органические нитросоединения: амилнитрит C5H11ONO и пропилнитрит C3H7ONO. Считают, что действие нитрита натрия сводится к превращению гемоглобина в мета-гемоглобин. Последний прочно связывает цианидные ионы в цианметагемоглобин. Этим путем дыхательные ферменты освобождаются от цианидных ионов, что и приводит к восстановлению дыхательной функции клеток и тканей.
В качестве противоядий на синильную кислоту широко используют серосодержащие соединения: коллоидную серу, тиосульфат натрия Na2S2O3, тетратионат натрия Na2S4O6, а также серосодержащие органические соединения, в частности, аминокислоты - глутатион, цистеин, цистин. Синильная кислота и ее соли при взаимодействии с серой превращаются в тиоцианаты в соответствии с уравнением
+ S → HNCS
Тиоцианаты же совершенно безвредны для человеческого организма.
С давних пор при опасности отравления цианидами рекомендовалось держать за щекой кусочек сахара. В 1915 г. немецкие химики Рупп и Гольце показали, что глюкоза взаимодействует с синильной кислотой и некоторыми цианидами с образованием нетоксичного соединения циангидрина глюкозы:
Считают, что это обстоятельство было причиной неудачной попытки отравить Распутина в 1916 г. в доме Юсупова добавлением цианида калия в сладкие пирожные, к которым он питал слабость.
Свинец
Свинец и его соединения являются довольно сильными ядами. Подумать страшно, что еще в начале текущего столетия водопроводные трубы в городах изготавливали из свинца. Затем их постепенно заменяли железными. В Санкт-Петербурге замена свинцовых труб в старых домах была завершена лишь в 50-х годах текущего столетия.
В организме человека свинец накапливается в костях, печени и почках. Ученые считают, что свинец является синергистом (от греч. synergos - вместе действующий) и способствует увеличению токсичности других металлов. Симптомами свинцового отравления служит серная кайма на деснах («свинцовая кайма»), бледность лица и губ, запоры, потеря аппетита. При остром отравлении появляются сильные боли в области живота («свинцовые колики»), параличи или боли в суставах, судороги, обмороки.
Талий
Весьма токсичны соединения химического элемента таллия, который относят к числу редких. Этот элемент является кумулятивным ядом. Под кумуляцией в медицине понимают накопление в организме веществ и вследствие этого усиление их действия. Токсичность соединений таллия принимают в четыре раза выше токсичности соединений мышьяка (III). Соединения таллия воздействуют на центральную нервную систему, на органы пищеварения и почки. Характерным признаком отравления таллием является выпадение волос. Первая помощь при отравлении - промывание желудка водой с активированным углем и 0,3%-ным раствором тиосульфата натрия Na2S2O3. В медицине на основе соединений таллия готовят препараты для удаления волосяного покрова.
Уместно опять же отметить, что опасные для здоровья человека химические элементы - ртуть, таллий и свинец - расположены в периодической системе рядом.
Следует указать, что все цветные и особенно тяжелые (расположенные в конце периодической системы) металлы в количествах выше допустимых ядовиты. На них существуют нормы предельно допустимых концентраций (ПДК). Здесь нет возможности остановиться на вредном воздействии всех этих элементов и симптомах отравления. Интересующиеся данными вопросами могут обратиться к специальной литературе. Автор же описал наиболее опасные и наиболее известные в этом отношении химические элементы и их соединения. Следует отметить лишь еще одно важное обстоятельство. Ученые установили, что токсичность солей металлов в мягкой воде, как правило, гораздо выше, чем в жесткой. Для тех, кто вынужден пользоваться для приготовления пищи жесткой водой, появляется хоть какое-то утешение.
Углекислый газ
Углекислый газ в больших количествах содержится в организме человека и потому не может быть ядовитым. За 1 ч взрослый человек выдыхает примерно 20 л (около 40 г) этого газа. При физической работе количество выдыхаемого углекислого газа увеличивается до 35 л. Он образуется в результате сгорания в организме углеводов и жиров. Однако при большом содержании CO2 в воздухе наступает удушье из-за недостатка кислорода. Максимальная продолжительность пребывания человека в помещении с концентрацией CO2до 20% (по объему) не должна превышать 2 ч. В Италии имеется получившая широкую известность пещера («Собачья пещера»), в которой человек стоя может находиться длительное время, а забежавшая туда собака задыхается и гибнет. Дело в том, что примерно до пояса человека пещера заполнена тяжелым (по сравнению с азотом и кислородом) углекислым газом. Поскольку голова человека находится в воздушном слое, то он не ощущает никаких неудобств. Собака же при ее росте оказывается в атмосфере углекислого газа и потому задыхается.
Врачи и биологи установили, что при окислении в организме углеводов до воды и углекислого газа на одну затраченную молекулу кислорода выделяется одна молекула CO2. Таким образом, отношение выделенного CO2 к поглощенному O2 (величина дыхательного коэффициента) равна единице. В случае окисления жиров дыхательный коэффициент равен примерно 0,7. Следовательно, определяя величину дыхательного коэффициента, можно судить, какие вещества преимущественно сгорают в организме. Экспериментально установлено, что при кратковременных, но интенсивных мышечных нагрузках энергия получается за счет окисления углеводов, а при длительных - преимущественно за счет сгорания жиров. Полагают, что переключение организма на окисление жиров связано с истощением резерва углеводов, что обычно наблюдается через 5...20 мин после начала интенсивной мышечной работы.
Заключение
Выявление биологической роли отдельных химических элементов в функционировании живых организмов (человека, животных, растений) - важная и увлекательная задача. Минеральные вещества, как и витамины, часто действуют как коферменты при катализе химических реакций, происходящих все время в организме.
Нет сомнения, что в живых организмах ионы металлов находятся в основном в виде координационных соединений с "биологическими" молекулами, которые выполняют роль лигандов.
Весьма интересен вопрос о принципах отбора природой химических элементов для функционирования живых организмов. Не вызывает сомнения, что их распространенность не является решающим фактором. Здоровый организм сам способен регулировать содержание отдельных элементов. При наличии выбора (пищи и воды) животные инстинктивно могут вносить лепту в это регулирование.
Список литературы
1) alhimik.ru/kunst/man's_elem.html
2) n-t.ru/ri/kk/hm16.htm
3) www.smed.ru/guides/184/
) Экспресс подготовка к ВНО 2013
) Т.А. Сало, В.П. Попович «Биология в таблицах и схемах 7-9»
Приложение
Таблица 1
| Химический элемент | Суточное поступление, мг | |
| взрослые | дети | |
| K | 2000-5500 | 530 |
| Na | 110-3300 | 260 |
| Ca | 800-1200 | 420 |
| Mg | 300-400 | 60 |
| Zn | 15 | 5 |
| Fe | 10-15 | 7,0 |
| Mn | 2,0-5,0 | 1,3 |
| Cu | 1,5-3,0 | 1,0 |
| Mo | 0,075-0,250 | 0,06 |
| Cr | 0,05-0,2 | 0,04 |
| Co | Около 0,2 (витамин В12) | 0,001 |
| Cl | 3200 | 470 |
| PO43- | 800-1200 | 210 |
| SO42- | 10 | - |
| I | 0,15 | 0,07 |
| Se | 0,05-0,07 | - |
| F | 1,5-4,0 | 0,6 |
Таблица 2
| Элемент | Символ | Содержание(%) | Значение для клетки и организма |
| Карбон | C | 15-18 | Главный структурный компонент всех органических соединений клетки |
| Оксиген | O | 65-75 | Главный структурный компонент всех органических соединений клетки |
| Нитроген | N | 1,5-3,0 | Обязательный компонент аминокислот |
| Гидроген | H | 8-10 | Главный структурный компонент всех органических соединений клетки |
| Фосфор | P | 0,0001 | Содержится в составе костей и зубной эмали, НК, АТФ и некоторых ферментов |
| Калий | K | 0,15-0,4 | Содержится в виде ионов, активирует ферменты белкового синтеза, обуславливает ритм сердечной д-ти, |
| Сульфур | S | 0,15-0,20 | Содержится в составе некоторых аминокислот, ферментов, витамина B |
| Хлор | Cl | 0,05-0,10 | Самый важный анион в организме животных, компонент HCl в желудочном соке |
| Кальций | Ca | 0,04-2,00 | Содержится в составе костей и зубов, активирует свертываемость крови и сокращение мышечных волокон |
| Магний | Mg | 0,02-0,03 | Содержится в составе зубов и костей, активирует энергетический обмен, а так же синтез ДНК |
| Натрий | Na | 0,02-0,03 | Содержится в виде ионов, обеспечивает нормальный ритм сердечной д-ти, влияет на синтез гормонов |
| Феррум | Fe | 0,010-0,015 | Содержится в составе ферментов, гемоглобина и миоглобулина |
| Йод | I | 0,0001 | Содержится в составе гормонов щитовидной железы |
| Купрум | Cu | 0,0002 | Содержится в составе некоторых ферментов, участвует в кроветворении, синтезе гемоглобина |
| Манган | Mn | 0,0001 | Содержится в составе некоторых ферментов или повышает их активность, участвует в развитии костей |
| Молибден | Mo | 0,0001 | Содержится в составе некоторых ферментов |
| Кобальт | Co | 0,0001 | Содержится в составе витамина B12, участвует в развитии эритроцитов |
| Цинк | Zn | 0,0003 | Содержится в составе ферментов |
Таблица 3
| Химическое соединение | Значение |
| Вода | - Придает клетке упругость и определяет ее форму - Участвует в процессах жизнедеятельности - Обеспечивает перемещение питательных в-в - Участвует в регуляции температуры в клетке |
| Минеральные соли | - Важны для процессов жизнедеятельности. Например, соли железа и магния необходимы для образования хлорофилла |
| Углеводы | - Источник энергии (при их расщеплении выделяется энергия, необходимая клетке) - Строительный материал (образуют целлюлозную клеточную стенку и т.д.) |
| Жиры | - Запасной источник энергии (запасаются, а при необходимости используются) |
| Белки | - Строительный материал (входят в состав клеточных структур) - Регулируют процессы жизнедеятельности и т.д. |
| Нуклеиновые Кислоты | - Сохраняют наследственную (генетическую) информацию - Передают эту информацию потомкам - Регулируют синтез белков |
| Фитогормоны | - Регулируют и координируют процессы роста и развития |
| Витамины | - Выполняют важные биохимические и физиологические функции |
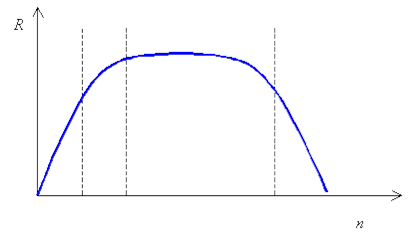
Рис. 1 Зависимость ответной реакции (R) от дозы (n) для жизненно необходимых элементов
Таблица 4
| Дефицит элемента | Типичный симптом |
| Ca | Замедление роста скелета |
| Mg | Мускульные судороги |
| Fe | Анемия, нарушение иммунной системы |
| Zn | Повреждение кожи, замедление роста, замедление полового созревания |
| Cu | Слабость артерий, нарушение деятельности печени, вторичная анемия |
| Mn | Бесплодие, ухудшение роста скелета |
| Mo | Замедление клеточного роста, склонность к кариесу |
| Co | Злокачественная анемия |
| Ni | Учащение депрессий, дерматиты |
| Cr | Симптомы диабета |
| Si | Нарушение роста скелета |
| F | Кариес зубов |
| I | Нарушение работы щитовидной железы, замедление метаболизма |
| Se | Мускульная (в частности, сердечная) слабость |
Таблица 5
| Период | |||||||
Группа