|
Главная |
Разбор тестов по химии для 9, 10 и 11 классов
Всем, читающим сей документ, доброго здравия!
На создание этого файла меня подвигла одна причина. Я не школьный учитель, и для меня занятия с олимповцами является чем-то вроде хобби. Всегда мои подопечные отличались высоким баллом при выполнении тестовых заданий, однако на этой области случился провал, при чем не только у них, но и у большинства участников. Прежде чем устраивать разнос, я решил сам, без дураков, пройти все тестовые задания. После этого мой гнев немножко поугас, зато появилось жгучее желание поделиться некоторыми мыслями. В результате перед вами подробный разбор тестовых заданий, после которых дана моя оценка каждому вопросу.
Надеюсь, моя работа будет с благодарностью принята олимпиадниками нынешними и будущими, а также критика будет полезна неизвестным мне составителям, которые задвинут свою гордость и самомнение в задний карман, и постараются в будущем избежать неприятных моментов, омрачающих их нелегкий труд.
Структура анализа
1. Формулировка вопроса.
2. Разбор вопроса
3. Мое собственное решение
4. Мой ответ и сравнение с ответом авторов
5. Вывод и оценка вопроса.
Поехали!!!!
| 9 класс | |||||||||||||||||||||||||||||||||||

| Вопрос на атомно-молекулярное учение и умение считать атомы, моли и т.д. Требует незначительных и непродолжительных расчетов. В вопросе есть все требуемые данные. Не сложный вопрос. | 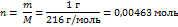 Элементом Va группы является только кислород. Одна ФЕ фармаколита содержит 6 атомов О, поэтому число атомов О будет равно
Элементом Va группы является только кислород. Одна ФЕ фармаколита содержит 6 атомов О, поэтому число атомов О будет равно
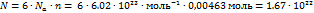
| Ответ Г, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 9 класса. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Вопрос на знание химических свойств простых веществ. Решаем в рамках обычной, даже не углубленной школьной программы. | Ответ Д, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 9 класса. Моя оценка 7/10 | ||||||||||||||||||||||||||||||||

| Вопрос на знание окислительно-восстановительных свойств элементов и умение расставлять СО в сложных веществах. Задание сложнее школьного уровня. | 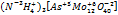
| Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 9 класса. Моя оценка 9/10 | |||||||||||||||||||||||||||||||
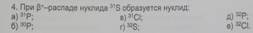
| Вопрос на знание ядерных реакций. Сложность в использовании позитрона | 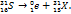 Элемент, заряд ядра которого +15 – Р. Элемент, заряд ядра которого +15 – Р.
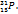
| Ответ А, что совпадает с ответом. Никаких замечаний нет. | Отличный вопрос. Моя оценка 10/10 | |||||||||||||||||||||||||||||||

| Совершенно школьный, очень простой вопрос на знание химических свойств амфотерных элементов | 2Al + 6NaOH + 6H2O = 2Na3[Al(OH)6] + 3H2. Na[Al(OH)4] не подходит, т.к. в условии четко прописана конц. щелочь. | Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Нормальный вопрос для 9 класса. Моя оценка 7/10 | |||||||||||||||||||||||||||||||

| Первое замечание. Дублирование вопроса 1. Снова расчет молей, атомов и молекул. Достаточно объемное решение | ||||||||||||||||||||||||||||||||||

| Сложный вопрос, требует крепких знаний теории гибридизации. Хорошо подобраны неправильные вещества. | N2O – линейная, N2O3 – уголковая, H2O2 – зигзаг, при чем скрученный, H2S – уголковая, O3 – уголковая, SO2 – уголковая. | Ответ А, что совпадает с ответом. Никаких замечаний нет. | Сложный вопрос для 9 класса. Моя оценка 10/10 | |||||||||||||||||||||||||||||||

| Вопрос на знание техники лабораторных работ. Очень простой для тех, кому показывали титрование и неподъемный для остальных. | Ответ Г, что совпадает с ответом. Никаких замечаний нет. | Сомнительный вопрос для 9 класса. Моя оценка 7/10 | ||||||||||||||||||||||||||||||||

| Вопрос на знание химических свойств. Требует всестороннего рассмотрения процесса взаимодействия растворителя с растворенным веществом | Такое будет возможно, если вещество не реагирует с водой и хорошо в ней растворимо. NO2 и Cr2S3 реагируют с водой, Mg с холодной не реагирует, Ca3(PO4)2 малорастворим в воде, AgF – да, Na2CO3·10H2O содержит кристаллизационную воду, поэтому масса безводного карбоната натрия будет меньше 10 г | Ответ Д, что совпадает с ответом. Никаких замечаний нет. | Отличный вопрос для 9 класса. Моя оценка 10/10 | |||||||||||||||||||||||||||||||

| Плохой вопрос. Дело в том, что можно написать несколько уравнений реакций взаимодействия CuS с HNO3. Хорошо, что составитель догадался не включить сумму коэффициентов от второй реакции в перечень неправильных. | CuS + 8HNO3 = CuSO4 + 8NO2 + 4H2O Сумма 22 CuS + 10HNO3 = Cu(NO3)2 + H2SO4 + 8NO2 + 4H2O Сумма 25 | Ответ Е, что совпадает с ответом. | Моя оценка 4/10 | |||||||||||||||||||||||||||||||

| Задача на нахождение формулы вещества. | Сумма долей все элементов равна 1. Тогда обозначим долю водорода за Х.
Х +10,24·Х + 10,24·1,55·Х = 1
Х = 0,0369. Массовая доля фосфора равна 0,0369·10,24 = 0,378. Считая, что в молекуле содержится только один атом Р, выйдем на молярную массу
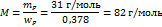
| Ответ Г, что совпадает с ответом. Никаких замечаний нет. | Отличный тест для 9 класса. Моя оценка 10/10 | |||||||||||||||||||||||||||||||

| Задача на кислотно-основные свойства веществ, а именно на теорию Бренстеда, ну, и на остроту зрения, т.к. не с первого раза можно заметить (-) при H2SO4 в ответе Д | Кроме Б, все остальное – глупость, и в серной кислоте существовать не может. Из-за автопротолиза 2H2SO4 D H3SO4+ + HSO4‑. | Ответ Б, что совпадает с ответом. | Возможно, можно было перечень неправильных другим сделать. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Хороший крепенький вопрос на ионные реакции в водных растворах | 3 моль SO42‑ прореагируют с 2 моль Pb2+, при этом образуется 2 моль PbSO4 и останется 1 моль SO42‑. Остальные ионы участия в реакции не принимали, их химические количества остались неизменны, тогда nост = 1,5 +1,5 + 1 + 4 =8 моль | Ответ Б, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 9 класса. Моя оценка 9/10 | |||||||||||||||||||||||||||||||

| Способы выражения состава раствора. Вполне школьный уровень. Правда, нужно знать, что такое глауберова соль. | 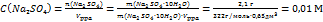 . .
| Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Хороший вопрос для 9 класса. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Задача ни ионные реакции в растворах. Опять повтор, хотя и отличающийся вопрос, добавлено знание окрасок индикаторов | В растворе Na2S протекает процесс протолиза иона S2‑ как остатка слабой кислоты. S2‑ + H2O D HS‑ + OH‑. Среда в растворе становится щелочной, окраска фенолфталеина малиновая | Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Хороший вопрос. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Органика, изомерия. | Нужно знать, что в органических молекулах, в которых отсутствует плоскость симметрии, число оптических изомеров рассчитывается по формуле N = 2n, где n – число стереоцентров. В заданной молекуле 2 стереоцентра, следовательно N = 22 = 4 | Ответ Г, что совпадает с ответом. Никаких замечаний нет. | Стандартный вопрос из органики. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Сборный вопрос. Мое мнение – для 10 класса, где смотрелся бы уместнее | А) – да, например соли карбоновых кислот или аминов, б) – да, т.к. бром менее активный галоген, чем хлор, в) – да, т.к. алкильная группа за счет +I-эффекта понижает полярность связи О-Н и ослабляет кислотные свойства, г) – нет, т.к. у гомологов одинаковая общая формула, а у глицерина и этиленгликоля общие формулы разные, д) – да, е) – да, ацетон – это представитель класса кетонов | Ответ Г, что совпадает с ответом. Никаких замечаний нет. | Плохой вопрос для 9 класса. Моя оценка 4/10 | |||||||||||||||||||||||||||||||

| Химические свойства углеводородов. Необходимо знать, что гидрируются непредельные УВ и малые циклы, в т.ч. и эпоксидный. | Ответ В, что совпадает с ответом. Никаких замечаний нет. | Отличный вопрос для 9 класса. Моя оценка 9/10 | ||||||||||||||||||||||||||||||||

| Химические свойства различных классов органических веществ. | Искомое вещество должно иметь основные свойства. Из перечисленных классов это только амин. | Ответ А, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 9 класса. Моя оценка 9/10 | |||||||||||||||||||||||||||||||

| Классическая расчетная задача на избыток/недостаток |
| Ответ В, что совпадает с ответом. Никаких замечаний нет. | Отличный вопрос для 9 класса. Моя оценка 10/10 | |||||||||||||||||||||||||||||||
| Подведем итог по 9 классу. В целом умеренный уровень сложности. Из 20 вопросов как минимум 14 не должны вызывать никаких затруднений, 2 вопроса неудачные либо чрезмерно сложные для 9 класса, все-таки нужно учитывать уровень олимпиады и тот факт, что практически все ученики приехали на соревнование такого уровня впервые. Все вопросы решаются однозначно, отсутствуют ярко выраженные косяки. С моей точки зрения два вопроса дублируют предыдущие, и их можно было заменить, расширив круг вопросов. По моему мнению, люди из первой десятки должны свободно забирать 23+ балла. Что помешало это сделать в Витебской области – для меня загадка. Но отсылка на сложность в данной ситуации невозможна. И последнее, на прохождение этого теста я затратил 12,5 минут чистого времени. | |||||||||||||||||||||||||||||||||||
| 10 класс | |||||||||||||||||||||||||||||||||||

| Вопрос из темы окислительно-восстановительные свойства. | 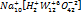
| Ответ Д, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 10 класса. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Вопрос по теме химическая связь | Необходимо знать, какие факторы и как влияют на энергию ковалентной связи. а,б,в – одинарная, г,д – двойная, е – тройная. а) из абв – самая короткая, значит, самая прочная, сравнивать б и в сложнее, но нужно принять во внимание, что в хлоре связь на самом деле не совсем одинарная, а частично кратная, поэтому ее энергия д.б. больше, чем у дилития | Ответ Б, что совпадает с ответом. Никаких замечаний нет. | Достаточно сложный вопрос для любого класса. Моя оценка 10/10 | |||||||||||||||||||||||||||||||

| Вопрос на химические свойства р-элементов. Не очень сложный. | Ответ Г, что совпадает с ответом. Никаких замечаний нет. | Нормальный вопрос. Моя оценка 8/10 | ||||||||||||||||||||||||||||||||
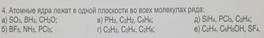
| Вопрос из темы строение молекул. Требует хорошего знания теории гибридизации. Плохой подбор веществ. Особенно для правильного ответа. Считаю, что нельзя использовать несуществующие молекулы. | Ответ А, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 10 класса. Неудачный подбор веществ Моя оценка 6/10 | ||||||||||||||||||||||||||||||||

| Вопрос из темы окислительно-восстановительные процессы. Очень неудачный пример реакции, поскольку допускает написание как минимум двух уравнений, но, правда, как и в 9 классе, второе исключается отсутствием суммы коэффициентов в вариантах выбора | 12MnO2 + 15H2SO4 = 5Mn2(SO4)3 + 2HMnO4. – один из вариантов неправильного (скорее, неподходящего) уравнения 4MnO2 + 6H2SO4 = 2Mn2(SO4)3 + О2 + 6H2О. Сумма 19. | Ответ Е, что совпадает с ответом. | Неудачный выбор реакции. Моя оценка 2/10 | |||||||||||||||||||||||||||||||

| Стандартная расчетная задачка на определение средней М смеси. Пример вполне школьного уровня. | 10·Х + 11·(1-Х) = 10,81 Х = 0,19 | Ответ Б, что совпадает с ответом. Никаких замечаний нет. | Для 10 класса простой вопрос. Моя оценка 6/10 | |||||||||||||||||||||||||||||||
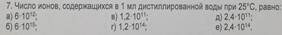
| Расчет по константам равновесия. Плохой вопрос, т.к. в условии отсутствуют значения констант. Справочные данные не могут быть объектом тестового вопроса. Если они нужны для решения, их необходимо дать в условии. | Что касается непосредственно решения, то оно достаточно простое
Ионное произведение воды равно Число ионов будет равно | Ответ Г, что совпадает с ответом. По расчету замечаний нет. | Хороший по задумке, но не по исполнению вопрос. Моя оценка 4/10 | |||||||||||||||||||||||||||||||

| Снова расчет по константам равновесия. Здесь все данные есть. | Рассчитаем рН в растворе HCl. Это совсем несложно, т.к. HCl – кислота сильная. Для сильных одноосновных кислот
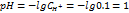 Расчет концентрации ионов Н+ и рН в исходном растворе плавиковой кислоты проведем по упрощенной формуле
Расчет концентрации ионов Н+ и рН в исходном растворе плавиковой кислоты проведем по упрощенной формуле
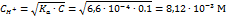 . .
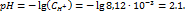
| Ответ Г, что совпадает с ответом. Никаких замечаний нет. | Нормальный рабочий вопрос. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Задача на нахождение формулы вещества. | Сумма долей все элементов равна 1. Тогда обозначим долю водорода за Х.
Х +10,24·Х + 10,24·1,55·Х = 1
Х = 0,0369. Массовая доля фосфора равна 0,0369·10,24 = 0,378. Считая, что в молекуле содержится только один атом Р, выйдем на молярную массу 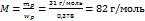 .
Это кислота H3PO3 – фосфористая кислота. Основность фосфористой кислоты – II. .
Это кислота H3PO3 – фосфористая кислота. Основность фосфористой кислоты – II.
| Ответ Б, что совпадает с ответом. Никаких замечаний нет. | Нормальный крепенький вопрос. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Комбинированный вопрос на термохимию и растворимость. | Хорошо известен тот факт, что соли аммония обычно растворяются с поглощением тепла, при чем иногда это растворение сопровождается обмерзанием емкости с раствором | Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Обычный вопрос умеренного уровня сложности. Моя оценка 7/10 | |||||||||||||||||||||||||||||||

| Вопрос из темы химическая термодинамика. Не очень удачный вопрос, вернее, не совсем хорошее вещество K2CO3. | Известно, что энтропия – мера беспорядка системы, чем больше беспорядок, тем выше энтропия, поэтому энтропия жидкости выше энтропии кристаллов, а энтропия газов намного больше энтропии конденсированных фаз. Это все так, и логика составителя понятна, но энтропия некоторых веществ сложного строения может не сильно отличаться от энтропии простого газа, поэтому использование карбоната калия – не очень удачно, лучше было бы взять какой-нибудь оксид металла | Ответ Е, что совпадает с ответом. Не совсем удачный подбор вариантов | Моя оценка 7/10 | |||||||||||||||||||||||||||||||

| Вопрос на знание химических свойств | Основным условием является вообще возможность существования такой смеси, а чтобы смесь существовала, вещества не должны между собой реагировать. Рассмотрим варианты а) SO2 + NO2 = SO3 + NO – не существует б) H2O + SO3 = H2SO4 – не существует в) Cl2 + 2HBr = 2HCl + Br2 – не существует г) Br2 + HF = не идет – существует, можно разделить д) H2SO4 + C2H5OH = разные продукты, зависят от условий, не существует е) N2O + H2S = не идет, существует, можно разделить. Возможно, авторы считают, что идет процесс 3N2O + H2S = 3N2 + SO2 + H2O, но протекание этой реакции при температурах кипения H2S я считаю маловероятной, в первую очередь по кинетическим факторам. Думаю, что вместо N2O лучше было использовать NO2, тогда никаких претензий, а так… | Ответ Г, и Е. Авторы дают Г, но Е тоже можно было отапеллировать. И здесь интересна позиция жюри на местах… | Вопрос хороший по задумке, но неоднозначность вариантов понижает его оценку. Моя оценка 4/10 | |||||||||||||||||||||||||||||||

| Вопрос по теме изомерия, но порадовало очень глубокое погружение в эту тему, набор совершенно нетривиальных вариантов выбора. | Ответ А, что совпадает с ответом. Никаких замечаний нет. | Отличный вопрос. Моя оценка 11/10J | ||||||||||||||||||||||||||||||||

| Вопрос на химические свойства металлов и координационную химию | Достаточно простой вопрос, если вспомнить, что катионы ртути образуют чрезвычайно малорастворимый сульфид, и еще тот факт, что токсичность ртути связана с тем, что она связывает SH-группы цистеина в белках, приводя к его денатурации | Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 10 класса. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Вопрос на химические свойства ароматических УВ. Вопрос на уровне школьной программы. | Ответ А, что совпадает с ответом. Никаких замечаний нет. | Очень простой вопрос для 10 класса. Моя оценка 7/10 | ||||||||||||||||||||||||||||||||

| Вопрос на теоретические основы органической химии. Вопрос не школьного уровня, требует изучения учебников по органической химии для ВУЗов | Если реакция второго порядка, то механизм этой реакции SN2 – бимолекулярное нуклеофильное замещение. Стереохимическим результатом замещения уходящей группы по механизму SN2 является обращение конфигурации асимметрического атома углерода. | Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Крепкий вопрос на знание материала выше школы. Моя оценка 8/10. | |||||||||||||||||||||||||||||||

| Опять строение вещества | Сложность – увидеть в первом соединении хлорид метиламмония [CH3-NH3]+Cl‑ | Ответ А, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 10 класса. Моя оценка 9/10 | |||||||||||||||||||||||||||||||

| Кислотные свойства органических соединений. | Обычный ряд кислотности спирт < вода < фенол < карбоновая кислота. Но присутствие в молекуле кислоты мощной электронакцепторной группы (NO2, CF3) позволяет резко повысить кислотность. Именно в связи с этим тринитрофенол по своим кислотным свойствам намного превосходит простые карбоновые кислоты | Ответ В, что совпадает с ответом. Никаких замечаний нет. | Обычный вопрос. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Химические свойства карбонильных соединений. Вопрос достаточно сложный. | Для того, чтобы частица присоединилась по карбонильной группе, она должна быть нуклеофильной, т.е. быть или анионом или иметь атом с неподеленной электронной парой. В хлориде метиламмония азот уже четырехвалентен, у него нет неподеленной пары на атоме азота. | Ответ Д, что совпадает с ответом. Никаких замечаний нет. | Достаточно сложный вопрос. Моя оценка 9/10 | |||||||||||||||||||||||||||||||

| Вопрос по химическим свойствам кислот и их производных по карбоксильной группе. Совершенно не сложный для открывавших книги. | Гидролиз нитрилов кислот протекает постадийно R-CN(нитрил) " R-CONH2(амид) " RCOOH (карбоновая кислота) | Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Простой вопрос. Моя оценка 7/10 | |||||||||||||||||||||||||||||||
| Подведем итог по 10 классу. В целом умеренный уровень сложности. Из 20 вопросов как минимум 12 не должны вызывать никаких затруднений, 1 вопрос допускает два ответа, в 2-х вопросах неудачные варианты ответа. 1 вопрос требует дополнительно справочные данные. Грубых ошибок нет. Есть вопросы к выбору тем, есть несколько вопросов на одну тему, тогда как многие просто проигнорированы. Что по баллам? Человек, рассчитывающий на поездку на Республику просто обязан делать этот тест на 23+ балла. Набравшие меньше могут адресовать претензии исключительно себе, но никак не к составителям. Два неудачных вопроса – не повод получать 15 – 20 баллов. И последнее, на прохождение этого теста я затратил 17 минут чистого времени.
| |||||||||||||||||||||||||||||||||||
| 11 класс | |||||||||||||||||||||||||||||||||||

| Вопрос на окислительно-восстановительные свойства. При чем вопрос достаточно неординарный. | 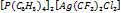 (С6Н5) целиком имеет +1, а Р - -3, т.к. фосфор более электроотрицательный, но можно и прощеJ. По правилам записи комплексных соединений первой записывается положительно заряженная частица, значит у первой частицы общий заряд +1, тогда второй комплексный ион должен иметь заряд -2. Проблема с CF3. Дело в том, что если она пришла из CF4, то у С СО +4, и СF3+, а если из CHF3, то у с СО +2, и CF3‑. Проверка первого варианта дает СО для серебра -1, проверка второго варианта дает СО для серебра +3. Мне кажется, что первый вариант маловероятен.
(С6Н5) целиком имеет +1, а Р - -3, т.к. фосфор более электроотрицательный, но можно и прощеJ. По правилам записи комплексных соединений первой записывается положительно заряженная частица, значит у первой частицы общий заряд +1, тогда второй комплексный ион должен иметь заряд -2. Проблема с CF3. Дело в том, что если она пришла из CF4, то у С СО +4, и СF3+, а если из CHF3, то у с СО +2, и CF3‑. Проверка первого варианта дает СО для серебра -1, проверка второго варианта дает СО для серебра +3. Мне кажется, что первый вариант маловероятен.
| Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Достаточно сложный вопрос. Моя оценка 9/10 | |||||||||||||||||||||||||||||||

| Задачка на определение формул. Достаточно хорошего уровня. | Для решения я использовал закон эквивалентов
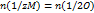 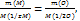 откуда откуда 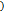 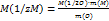 . Подстановка массовых долей кислорода и металла из набора ответов приводит к следующим решениям
а) M(1/zM) = 2 г/моль
б) M(1/zM) = 2,52 г/моль
в) M(1/zM) = 3,11 г/моль
г) M(1/zM) = 3,43 г/моль
д) M(1/zM) = 3,76 г/моль
е) M(1/zM) = 4,5 г/моль
Только в варианте е) при z = 2 M = 9 г/моль, что отвечает Be . Подстановка массовых долей кислорода и металла из набора ответов приводит к следующим решениям
а) M(1/zM) = 2 г/моль
б) M(1/zM) = 2,52 г/моль
в) M(1/zM) = 3,11 г/моль
г) M(1/zM) = 3,43 г/моль
д) M(1/zM) = 3,76 г/моль
е) M(1/zM) = 4,5 г/моль
Только в варианте е) при z = 2 M = 9 г/моль, что отвечает Be
| Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Хороший вопрос. Моя оценка 10/10 | |||||||||||||||||||||||||||||||

| Вопрос из темы строение молекул. Требует хорошего знания теории гибридизации. Плохой подбор веществ. Считаю, что нельзя использовать несуществующие молекулы. | Ответ Г, что совпадает с ответом. | Хороший вопрос. Моя оценка 8/10 | ||||||||||||||||||||||||||||||||

| Задача на определение формулы неорганического соединения. | Можно было решать по примеру решения 9 и 10 классов, но мы пошли другим путем. Нужно обратить внимание, что массовые доли Р и О почти одинаковы, значит и массы этих элементов близки. А(Р) = 31, значит m(O) должна быть 32, что дает 2О. и остаток РО2, а единственной кислотой с таким кислотным остатком является фосфорноватистая кислота Н3РО2. Фосфорноватистая кислота одноосновна. | Ответ А, что совпадает с ответом. Никаких замечаний нет. | Простой вопрос. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Вопрос на расчет по константам равновесия. Задачка среднего уровня сложности. Проблема в том, что составители забыли дать численное значение Ka(CH3COOH), или посчитали, что школьники в 11 кл обязаны такую ерунду знать напамять. | Расчет концентрации ионов Н+ и рН в исходном растворе уксусной кислоты проведем по упрощенной формуле (я протолитические равновесия считаю почти 30 лет, поэтому многие константы знаю наизусть) 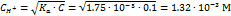 . .
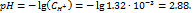 После прибавления к раствору уксусной кислоты ацетата натрия образовался буферный раствор, рН которого (надеюсь, меня простят читатели, что без вывода) считается по уравнению Гендерсона-Хассельбаха
После прибавления к раствору уксусной кислоты ацетата натрия образовался буферный раствор, рН которого (надеюсь, меня простят читатели, что без вывода) считается по уравнению Гендерсона-Хассельбаха
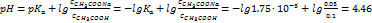 Ну, и далее посчитать разницу рН
Ну, и далее посчитать разницу рН
| Ответ Г, что совпадает с ответом. | По моему мнению, вопрос должен был быть или снят, или на доске жюри должно было записать значение Ка. Моя оценка 2/10 | |||||||||||||||||||||||||||||||

| Коэффициенты в ОВР. Усложнение в том, что продукты нужно самим догадаться на основании химических свойств соединений марганца и азота. | 2MnO2 + 2H2SO4 + N2H4 = 2MnSO4 + N2 + 4H2O Сумма коэффициентов 12. | Ответ Г, что совпадает с ответом. Никаких замечаний нет. | Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Вопрос аналогичен таковому в 10 классе №7 с теми же самыми замечаниями |
Ионное произведение воды равно Число ионов будет равно | Ответ Г, что совпадает с ответом. Никаких замечаний нет. | Хороший по задумке, но не по исполнению вопрос. Моя оценка 4/10 | |||||||||||||||||||||||||||||||

| Опять же, повтор такового вопроса из 10 кл. В отличие от него, здесь вещества подобраны грамотно, и не допускают неоднозначностей в определении правильного ответа. | Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 11 класса. Моя оценка 8/10 | ||||||||||||||||||||||||||||||||

| Повтор. Для 11 класса даже слишком простой вопрос | Ответ В, что совпадает с ответом. Никаких замечаний нет. | Слишком простой вопрос для 11 класса. Моя оценка 6/10 | ||||||||||||||||||||||||||||||||

| Вопрос на электрохимию. Требует знания определений и, пожалуй, все. | В работающем гальваническом элементе потенциал катода больше потенциала анода. ЭДС рассчитывается как потенциал катода минус потенциал анода без учета количества переходящих электронов | Ответ В, что совпадает с ответом. Никаких замечаний нет. | Обычный вопрос без какой-нибудь фантазии. Моя оценка 7/10 | |||||||||||||||||||||||||||||||


| Достаточно сложный вопрос из курса физической химии. | Можно долго разбирать все варианты, поэтому сразу к правильному. Утверждение б) неверно, т.к. достаточно вспомнить, что в однокомпонентной системе в равновесии могут одновременно находится 3 фазы в тройной точке. | Ответ Б, что совпадает с ответом. Никаких замечаний нет. | Очень сложный вопрос, возможно, выше уровня области Моя оценка 9/10 | |||||||||||||||||||||||||||||||

| Первый косяк. Лично мне очень интересно, в какой микроскоп составитель увидел асимметрический углерод в положении 2 в молекуле 2-метил-2-хлорбутана. На этом рассмотрение можно закрывать, т.к. на дурацкий вопрос можно дать только дурацкий ответ | Понятно, что для решения нужно было вспомнить, что SN1 идет с рацемизацией асимметрического центра и выбрать именно этот ответ… | Нет ответа | Вопрос д.б. быть снят. Моя оценка 0/10 | |||||||||||||||||||||||||||||||

| Вопрос на знание полимеров | Знание в чистом виде | Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Обычный проходной вопрос для 11 класса. Моя оценка 8/10 | |||||||||||||||||||||||||||||||

| Биохимия. Хороший вопрос, разнообразивший тематику тестов. | Переход аскобат D дегидроаскорбат является ОВР, а, значит, должен катализироваться оксидоредуктазой | Ответ Д, что совпадает с ответом. Никаких замечаний нет. | Моя оценка 9/10 | |||||||||||||||||||||||||||||||

| Вопрос на теоретические основы органической химии | Ответ Б, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 11 класса. Моя оценка 8/10 | ||||||||||||||||||||||||||||||||

| Аналитическая химия | Для того, чтобы дать правильный ответ на этот вопрос нужно было предварительно заглянуть в любое практическое руководство по аналитической химии, в котором можно прочитать, что ионы Fe3+ с ионами F‑ образуют очень прочный бесцветный комплекс FeF63‑, образование которого применяют для маскировки бурой окраски иона Fe3+. | Ответ Е, что совпадает с ответом. Никаких замечаний нет. | Очень хороший вопрос. Моя оценка 10/10 | |||||||||||||||||||||||||||||||

| Обычная расчетная задачка на перерасчет величин, подобного типа расчеты любой химик должен делать на автомате. | 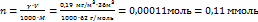 . .
| Ответ Д, что совпадает с ответом. Никаких замечаний нет. | Простой вопрос. Моя оценка 7/10 | |||||||||||||||||||||||||||||||

| Методы получения спиртов через магнийорганику. Уровень вопроса вполне соответствует области | Нужно учесть, что в условии вопроса не указано, что осуществлено выделение спирта из алкоголята, хотя этот момент часто опускается в цепочках | Ответ Д, что совпадает с ответом. Никаких замечаний нет. | Отличный вопрос. Моя оценка 10/10 | |||||||||||||||||||||||||||||||

| Химические свойства органических соединений. | Для того, чтобы органическое соединение проявляло амфотерные свойства, в его молекуле должны присутствовать одновременно основная и кислотная функции. В молекуле пикриновой кислоты в наличии только кислотная. | Ответ В, что совпадает с ответом. Никаких замечаний нет. | Нормальный и вполне уместный вопрос для 11 класса. Моя оценка 9/10 | |||||||||||||||||||||||||||||||

| Снова аналитическая химия. И опять претензия к составителям – без справочных данных по значениям Ksp этот вопрос нужно снимать. | Это самый плохой вопрос из всего набора. Абсолютно надуманный и искусственный вопрос. Поскольку это единственный вопрос, на который я дал ответ, расходящийся с авторским, попробую восстановить всю логику решения, думаю, что вам будет интересно Ну, во-первых, что значит – с минимальной погрешностью? Если под минимальной погрешностью автор подразумевает минимальную остаточную концентрацию, то вопрос не имеет смысла, ибо полноту осаждения можно регулировать, увеличивая избыток осадителя. Ну, допустим, нужно исходить из минимальной растворимости осадка в воде, ок. Для этого надо знать Ksp. Которых нет. Ладно, напрягаем память (в Лурье не лезу из принципа, у олимпиадников Лурье под боком не было). Гидроксид Ksp порядка 10-15, значит растворимость порядка 10-5, карбонат вроде 10-9, значит растворимость на уровне 10-5, гидрофосфат вроде еще выше, средний фосфат не помню, ну, пусть как у кальция, Ksp на уровне 10-20, значит растворимость опять около 10-5, сульфид помню, там порядок 10-22, значит растворимость приблизительно 10-11 и остался глиоксимат, Ksp которого я, если честно, и не встречал особо нигде, но чтобы растворимость была ниже, чем у сульфида, Ksp для него должен быть ниже 10-35, чегой-то сомнительно, поскольку это внутрикомплексное соединение, то константы там на уровне 10-10 – 10-20 обычно, поэтому делаю выбор в пользу сульфида | Ответ Г, что не совпадает с ответом. Авторский ответ Б. Ну, а теперь ради принципа, лезем в справочник Ksp(Ni(OH)2) = 2·10-15 Ksp(NiS) = 3.2 10-19 Ksp(Ni(gly)2) = 2.3·10-25 Ksp(NiHPO4) нету Ksp(Ni3(PO4)2) нету Ksp(NiCO3) = 1.3·10-7 Итак, значения Ksp авторов вопроса опровергают, молярная растворимость сульфида никеля ниже, чем диметилглиоксимата | Надеюсь, все всем понятно. 0/10 | |||||||||||||||||||||||||||||||
| Подведем итог по 11 классу. Все гораздо хуже, чем в 9 и 10 классах. В целом достаточный уровень сложности. Из 20 вопросов как минимум 14 не должны вызывать никаких затруднений, тем более, что это все-таки 11 класс, и большинство не первый раз участвует в олимпиаде областного уровня. 2 вопроса – косяки, при чем жестокие. 2 вопроса просто плохие. 3 вопроса требуют дополнительных справочных данных без которых они не решаются, строго говоря. Что по баллам? Человек, рассчитывающий на поездку на Республику просто обязан делать этот тест на 22+ балла. И последнее, на прохождение этого теста я затратил 16 минут чистого времени.
| |||||||||||||||||||||||||||||||||||
| Теперь в целом. А в целом ситуация куда как грустнее. Но вначале плюсы · Адекватный уровень вопросов · Однозначно определяемые ответы, мало дискуссионных вопросов Теперь минусы · Катастрофически узкий охват тем · Присутствие в комплекте вопросов одного класса нескольких заданий на одну тему. · Наличие явно невычитанных и плохо составленных вопросов. · Для 11 класса, в котором решается судьба поступления, слишком много косяков · Плагиат. Лень копаться в архиве, но несколько вопросов передраны из прошлых лет и других олимпиад. · Практически не было оригинальных или нестандартных вопросов. | |||||||||||||||||||||||||||||||||||
Ну, вот, вроде как все. Буду рад дополнительным вопросам и критическим замечаниям.
Прошедшим дальше – успехов на Респе, и пусть победит достойнейший!!!!!

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы


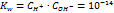 . Для чистой воды
. Для чистой воды 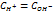 , следовательно
, следовательно 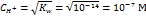 .
.