 |
Главная |
Способы выражения концентраций растворов
|
из
5.00
|
Содержание
| Содержание | ||
| Список условных обозначений | ||
| Предисловие | ||
| 1. | Способы выражения концентрации раствора | |
| 2. | Теоретические основы биоэнергетики | |
| 2.1 | Основные понятия термодинамики | |
| 2.2 | Первый закон термодинамики | |
| 2.3 | Тепловой эффект реакции. Закон Гесса | |
| 2. 4 | Энтропия. II закон термодинамики | |
| 2. 5 | Энергия Гиббса как критерий самопроизвольности процесса | |
| 3. | Кинетика химических реакций | |
| 3.1. | Кинетическая классификация химических реакций | |
| 3.2. | Факторы, влияющие на скорость химических реакций | |
| 3.3 | Основные свойства ферментов | |
| 3.4 | Ферментативный катализ | |
| 4. | Кислотно-основное равновесие | |
| 4.1. | Кислотность и основность среды | |
| 4.2. | Буферные системы организма | |
| 5. | Комплексные соединения | |
| 6. | Биогенные элементы | |
| 7. | Окислительно-восстановительные процессы | |
| 8. | Высокомолекулярные вещества (ВМС) | |
| 8.1. | Общие понятия, классификация высокомолекулярных соединений | |
| 8.2. | Общая характеристика растворов высокомолекулярных соединений | |
| 8.3. | Водные растворы белков | |
| 8.4. | Набухание высокомолекулярных соединений | |
| 8.5. | Вязкость растворов высокомолекулярных соединений | |
| 8.6. | Осмотическое (онкотическое) давление в растворах ВМС | |
| 8.7. | Мембранное равновесие Донанна | |
| 8.8. | Специфические свойства растворов ВМС | |
| 9. | Классификация и номенклатура органических соединений | |
| 9.1. | Классификация органических соединений | |
| 9.2. | Номенклатура органических соединений | |
| 10. | Пространственное строение органических соединений. | |
| 10.1. | Структурная изомерия | |
| 10.2. | Стереоизомерия. Хиральные молекулы. Энантиомеры молекул с одним и более хиральными центрами | |
| 10.3. | Диастереомерия | |
| 11. | Амины | |
| 12. | Спирты, фенолы | |
| 13. | Альдегиды, кетоны | |
| 14. | Карбоновые кислоты | |
| 15. | Гетерофункциональные соединения | |
| 15.1. | Аминоспирты | |
| 15.2. | Гидроксикислоты | |
| 15.3. | Оксокислоты | |
| 15.4. | Гетерофункциональные производные бензола |
| 15.5. | Аминокислоты | |
| 15.6. | Пептиды, белки | |
| 16. | Углеводы | |
| 16.1. | Моносахариды | |
| 16.2. | Производные моносахаридов. | |
| 16.3. | Дисахариды | |
| 16.4. | Полисахариды | |
| 17. | Гетероциклические соединения | |
| 17.1. | Пятичленные гетероциклы с одним гетероатомом | |
| 17.2. | Пятичленные гетероциклы с двумя гетероатомами | |
| 17.3. | Шестичленные азотсодержащие гетероциклы с одним гетероатомом. | |
| 17.4. | Шестичленные азотсодержащие гетероциклы с двумя гетероатомами. | |
| 17.5. | Конденсированные гетероциклы | |
| 18. | Нуклеиновые кислоты | |
| 18.1. | Нуклеозиды | |
| 18.2. | Нуклеотиды | |
| 18.3. | Нуклеиновые кислоты | |
| 19. | Липиды | |
| 19.1. | Омыляемые липиды | |
| 19.2. | Неомыляемые липиды | |
| 19.2.1. | Терпены | |
| 19.2.2. | Стероиды | |
| Тесты | ||
| Литература |
Список условных обозначений
АДФ – аденозин дифосфат
АМФ – аденозин монофосфат
АТФ –аденозин трифосфат
ВМС – высокомолекулярные соединения
ДНК – дезоксинуклеиновые кислоты
ОВП – окислительно-восстановительные процессы
РНК – рибонуклеиновые кислоты
ПРЕДИСЛОВИЕ
Химия относится к числу естественных наук, изучающих окружающий нас мир во всем богатстве его форм и многообразии происходящих в нем явлений.
Мир материален: все существующее в нем представляет собой различные виды материи, находящейся в состоянии непрерывного движения, изменения и развития. Каждый отдельный вид материи, обладающий определенными физическими и химическими свойствами, называют веществом. Вещество не является неделимым. Представления о том, что вещества состоят из отдельных, очень малых частиц возникли еще в Древней Греции. Современная теория строения вещества полностью основана на представлениях и идеях Михаила Васильевича Ломоносова.
Химия является фундаментальной наукой и мощным инструментом исследования и познания процессов в живых системах. Поэтому студенты медицинских специальностей должны хорошо усвоить основные идеи, законы и методы этой науки. Данное пособие поможет получить знания, которые могут быть использованы при рассмотрении физико-химической сущности и механизмов процессов, происходящих в живом организме на молекулярном и клеточном уровне и для выполнения в необходимых случаях расчетов этих процессов. Пособие «Химия» способствует формированию у студентов целостного естественнонаучного подхода к изучению человеческого организма, а также дает возможность к обобщению химических и физико-химических аспектов важнейших биохимических процессов и различных видов равновесий, происходящих в живом организме.
Способы выражения концентраций растворов
Количественной характеристикой растворов является концентрация. Концентрацией называется масса или количество вещества, содержащаяся в определённой массе или объёме раствора. Существуют следующие способы выражения концентраций.
1. Массовая доля – это отношение массы растворённого вещества к массе раствора:
 %
%
Из определения массовой доли следует, что можно рассчитать массу растворенного вещества и массу раствора:
 ;
;
 .
.
Массу раствора можно также рассчитать следующим образом:
 .
.
1. Молярная концентрация – это отношение количества вещества к объёму раствора:
 , размерность молярной концентрации – моль/л.
, размерность молярной концентрации – моль/л.
Так как количество вещества равно отношению массы вещества к его молярной массы:
 , то
, то  .
.
Отсюда можно рассчитать массу растворенного вещества:
 .
.
2. Молярная концентрация эквивалента – это отношение количества эквивалентов вещества к объёму раствора:
 , моль/л.
, моль/л.
3. Моляльная концентрация– это отношение количества вещества к массе растворителя:
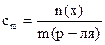 , моль/кг.
, моль/кг.
Mр-ля = mр-р – mр.в.
4. Титр – это масса вещества, содержащаяся в 1 мл раствора:
Т=m/V ;  , г/мл.
, г/мл.
|
из
5.00
|
Обсуждение в статье: Способы выражения концентраций растворов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

