 |
Главная |
Описание установки и метода измерения
|
из
5.00
|
ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ ТЕПЛОЕМКОСТЕЙ ВОЗДУХА МЕТОДОМ АДИАБАТИЧЕСКОГО РАСШИРЕНИЯ
Цель работы: определение коэффициента Пуассона для воздуха методом адиабатического расширения.
Оборудование: стеклянный сосуд, жидкостный манометр, барометр, термометр, насос Шинца.
Вопросы теории
Теория теплоемкости идеального газа. Связь теплоемкостей с числом степеней свободы молекул газа. Адиабатический процесс и изопроцессы. Изображение газовых процессов на диаграммах (P,V), (P, T), (V, T). Применение первого начала термодинамики к процессам в идеальном газе.
Указания к теоретической подготовке
Согласно теории теплоемкости изменение внутренней энергии идеального газа зависит от числа степеней свободы молекулi и изменения температуры DT:
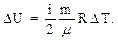
С другой стороны, по первому началу термодинамики при изохорическом процессе все подводимое количество теплоты  идет на приращение внутренней энергии DU: Qv = DU .
идет на приращение внутренней энергии DU: Qv = DU .
Отсюда следует, что молярная теплоемкость при постоянном объеме:

Применив первое начало к изобарическому процессу и установив связь между теплоемкостями Сm p и Cm v:  ;
;  ,
,
можно найти показатель адиабаты через число степеней свободы молекул газа:
 .
.
Число степеней свободы молекулы показывает, какое число координат нужно задать для однозначного определения положения молекулы в пространстве. Одноатомные свободные молекулы имеют три степени свободы, связанные с поступательным движением; жесткие двухатомные – пять степеней свободы: три поступательных и две вращательных; трехатомные - шесть: три поступательных и три вращательных. Воздух (смесь газов) состоит, в основном, из двухатомных газов, поэтому считают, что число степеней свободы воздуха равно пяти.
Описание установки и метода измерения
Установка состоит из стеклянного сосуда 1, закрытого пробкой, в которую вставлены клапан 4 и трубки для присоединения насоса и манометра.
С помощью насоса 2 в сосуде можно создать повышенное давление, измеряемое манометром 3. Через некоторое время вследствие теплообмена через стенки сосуда установится тепловое равновесие воздуха в сосуде с окружающей средой, воздух будет иметь комнатную температуру и находиться под давлением P1, превышающим атмосферное давление на величину, измеряемую манометром.
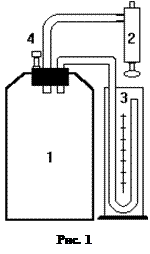 Если быстрым, кратковременным нажатием клапана дать воздуху из сосуда расшириться, то давление уменьшится до атмосферного (при этом уровни жидкости в правом и левом коленах манометра сравняются), а температура понизится. Через некоторое время из-за теплообмена с окружающей средой воздух в сосуде нагревается до комнатной температуры, давление повышается до P2.
Если быстрым, кратковременным нажатием клапана дать воздуху из сосуда расшириться, то давление уменьшится до атмосферного (при этом уровни жидкости в правом и левом коленах манометра сравняются), а температура понизится. Через некоторое время из-за теплообмена с окружающей средой воздух в сосуде нагревается до комнатной температуры, давление повышается до P2.
Показания манометра перед адиабатическим расширением h1 и после изохорического нагревания h2 связаны с давлениями газа P1 и P2, которые много меньше атмосферного P0, поэтому рабочую формулу можно получить в виде:

|
из
5.00
|
Обсуждение в статье: Описание установки и метода измерения |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

