 |
Главная |
Общая характеристика окислительно-восстановительного титрования. Классификация
|
из
5.00
|
Дробный и систематический метод
1. Основные понятия темы
Специфические реакции позволяют обнаруживать ион в отдельной порции анализируемого раствора, не считаясь с присутствием других ионов. При этом последовательность обнаружения ионов может быть произвольной.
Дробным анализом называют обнаружение ионов с помощью специфических реакций в отдельных порциях анализируемого раствора, производимое в любой последовательности.
Дробный анализ применяют агрохимические и заводские лаборатории, особенно в тех случаях, когда состав исследуемого материала достаточно хорошо известен и требуется только проверить отсутствие некоторых примесей. Если же используемые реакции не специфичны, а мешающее действие посторонних ионов устранить не удается, то проведение дробного анализа невозможно. В этом случае применяют систематический ход анализа.
Сисmемаmическим ходом анализа – называется определенная последовательность выполнения аналитических реакций, при которой каждый ион обнаруживают после того, как будут обнаружены и удалены другие ионы, мешающие его обнаружению.
Допустим, что раствор нужно испытать на присутствие катиона Са2+, но в нем одновременно может содержаться и ион Ва2+. Катион Са2+ принято обнаруживать в виде оксалата:
CaC12 + (NH4)2С2О4 = СаС2О4+ 2NH4Cl
Эта реакция достаточно чувствительна, но не специфична, так как оксалат аммония (NH4)2C204 дает белый кристаллический осадок не только с Са2+, но также с Ва2+ и некоторыми другими ионами. Поэтому прежде чем обнаруживать катион Са2+, необходимо проверить, присутствует ли в растворе мешающий ион Ва2+. Последний можно обнаружить в отдельной порции раствора, действуя хроматом калия, с которым Ва2+ дает характерный желтый осадок:
BaCl2 + К2Сг04 = ВаСг04↓ + 2KCl
Присутствие иона Са2+ не мешает обнаружению иона Bа2+ этой реакцией, так как хромат кальция СаСгО4 хорошо растворим в воде (выпадает в осадок только из очень концентрированных растворов солей кальция).
Дальнейший ход анализа зависит от результата проведенного испытания. Если окажется, что ион Bа2+ отсутствует, то в другой порции раствора можно обнаруживать катион Са2+, действуя оксалатом аммония (NH4)2С2О4. Если же катион Bа2+ присутствует, то прежде чем обнаруживать Са2+, следует полностью удалить из раствора ионы Bа2+. Для этого на весь раствор действуют избытком хромата калия К2Сr04 (или дихромата калия К2Сr207), убеждаются, что ионы Bа2+ полностью осаждены в виде хромата бария BaСrО4 и, отделив осадок, беспрепятственно обнаруживают катионы Са2+.
Следовательно, в систематическом ходе анализа применяют не только реакции обнаружения отдельных ионов, но также и реакции отделения их друг от друга.
Разделение ионов чаще всего основывается на различной растворимости аналогичных солей (например, ВаСr04 и СаСrО4). Иногда в этих целях используют и различную летучесть соединений. Так, отделение катиона NH4+ от ионов Na+, К+ и Mg2+ осуществляют выпариванием раствора и прокаливанием сухого остатка. При этом непрочные соли аммония разлагаются, улетучиваются, и соединения Na+, К+ и Mg2+ освобождаются от мешающих примесей этих солей, отделяя один ион от другого, нужно внимательно следить за полнотой этого разделения, без которой результаты анализа будут ошибочными. Например, при неполном удалении иона NH4+ можно в дальнейшем „переоткрыть” К+ и Nа+, так как с реактивами на эти катионы взаимодействуют и соли аммония. Полноту удаления мешающего иона проверяют в каждом случае специальной пробой. Систематический анализ не следует противопоставлять дробному: эти методы взаимно дополняют друг друга. Каждый из них имеет свою область применения.
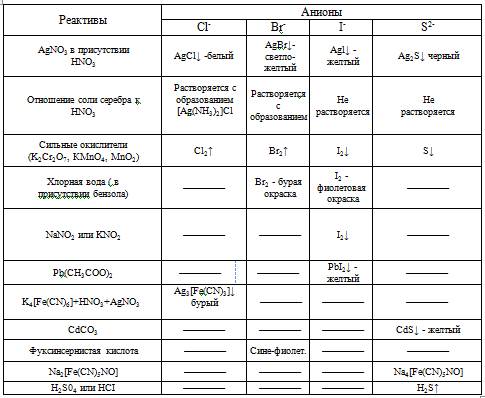
Анализ смеси анионов II аналитической группы
Анионы второй аналитической группы: Cl-, Br-, I-, S 2-
Большинство солей, образуемых анионами второй группы, растворимы в воде.
Исключение составляют соли серебра, ртути и свинца. Групповой реактив на вторую группу анионов - нитрат серебра в присутствии азотной кислоты, который образует с анионами второй группы серебряные соли, не растворимые в воде и, в отличие от анионов первой группы, не растворимые в разбавленной азотной кислоте.
Реакции анионов второй группы
Общая характеристика окислительно-восстановительного титрования. Классификация.
В ОВТ используются реакции, связанные с изменением степени окисления реагируемых веществ, т.е. реакция окисления и восстановления. Все методы в ОВТ основаны на колич. окислении или восстановлении анализируемого вещества. Другое название этих методов – оксидиметрия, редоксиметрия – происходит от названия нач.слогов окисл. и восстан.
Методы в ОВТ классифиц-т в соответствии с примененяемым титрованным раствором. Наиболее распространенные из них:
1. Пермангонатометрия – определение основано на использовании реакций окисления раствором KMnO4
2. Йодометрия - определение основано на использовании растворов I2 или I—ионов.
3. Хроматометрия – определение основано на использовании растворов дихромата или хромата К, а иногда Cr2O3
4. Броматометрия – основано на использовании реакций раствором KBr
Для расчетов в титриметрических методах с использованием ОВР необходимо знать молярные концентрации и массы эквивалента.
Эквивалент в-ва в реакциях окисления-восстановления – условная частица, приходящаяся на один принятый или отданный электрон.
Молярная масса эквивалента вещества – масса одного моля эквивалентов этого в-ва.
В титриметрических методах, основанных на проведении реакции О-В, для обнаружения конечной точки титрования разные приемы:
· Исчезновение или появление окраски титранта или титруемого вещества
· Специфические и окислительно-восстан. индикаторы
· Инструментальные методы
Так, при титровании р-ра KMnO4 окончание титрования определяют по появлению розового окрашивания при появлении одной лишней капли избытка титранта.
ОВИндикаторы - в основном органические соединения, способные в окислению или восстановлению. Их окисленная и востановленная формы имеют разные окраски. Индикаторами этого типа являются, например, дифениламин, салициловая к-та и т.д.
|
из
5.00
|
Обсуждение в статье: Общая характеристика окислительно-восстановительного титрования. Классификация |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

