 |
Главная |
Количественный состав растворов
|
из
5.00
|
Растворы.
Раствор— это гомогенная система, состоящая из двух или более компонентов и продуктов их взаимодействия.
Растворы всегда однородны и по агрегатному состоянию могут представлять собой газ, жидкость или твердое вещество. Любые газы смешиваются друг с другом в любых соотношениях. Такие растворы чаще называют газовыми смесями. В жидкостях могут растворяться газы, другие жидкости и твердые вещества (агрегатное состояние таких растворов жидкое). Аналогично существуют растворы газов, жидкостей и твердых веществ в твердых веществах. Например, при кристаллизации расплава серебра и золота можно получить твердые растворы различного состава.
В истинных растворах вещество дисперсной фазы раздроблено до мельчайших частиц — молекул или ионов. Такие частицы непросто увидеть даже «вооруженным» глазом, поскольку их размеры не превышают 5 нм (5 • 10~9 м).
Чаще всего растворы состоят из двух компонентов — растворителя и растворенного вещества. Понятия «растворитель» и «растворенное вещество» достаточно условны. Растворителем считают то вещество, агрегатное состояние которого не изменяется при образовании раствора. Например, в системах аммиак—вода, нитрат серебра—вода растворителем является вода, несмотря на то, что в 65% -м растворе нитрата серебра массовая доля соли больше, чем воды. Если же раствор образовался при смешении газа с газом, жидкости с жидкостью, твердого вещества с твердым веществом, то растворителем считают тот компонент, которого в растворе больше. Если одним из компонентов раствора является вода, ее чаще всего и считают растворителем. Например, 60%-ю азотную кислоту привычнее считать водным раствором HNO3, а не раствором воды в азотной кислоте.
Растворимость.
Количественный состав растворов
Большинство твердых веществ не может растворяться в каком-то определенном объеме воды в неограниченном количестве. Всякий раз * мы замечаем, что при растворении наступает такой момент, когда вещество перестает растворяться, добавленный избыток его выпадает из раствора б виде осадка. Такой раствор, в котором при данных условиях взятое вещество больше не растворяется, называется насыщенным раствором.
• Запишите в тетрадь определение насыщенного раствора.
Масса растворенного вещества, необходимая для образования насыщенного раствора, при одних и тех же условиях у разных веществ различна. Например, в 100 г воды при 0°С может раствориться не более 15 г нитрата калия или не больше 30 г нашатыря, или не больше 15 г медного купороса, при 20 °С — 33 г нитрата калия, 37 г нашатыря 20 г медного купороса и т. д.
Масса вещества (в граммах), образующая при данных условиях насыщенный раствор в 100 г растворителя (воды), называется коэффициентом растворимости. Растворимость— одна из характеристик вещества. С изменением температуры или давления растворимость меняется. Зависимость растворимости некоторых твердых веществ от температуры представлена на рис. 1.
1. Пользуясь кривой, приведенной на рис. 1, определите растворимость NH4CI при 50 °С, КСIOз при 90 °С, CuSO4 при 85 °С.
2. Рассчитайте растворимость квасцов при 50 °С, если из 75 г раствора, насыщенного при этой температуре, можно выделить 25 г соли.
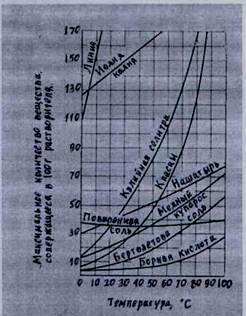 Рис. В График зависимости растворимости некоторых твердых веществ от температуры
Рис. В График зависимости растворимости некоторых твердых веществ от температуры
| Как правило, с повышением температуры растворимость твердых веществ резко возрастает. Например, растворимость нитрата калия при 0°С составляет 10 г в 100 г воды, при 45 °С — 75 г, при 60°С— 110 г, а при 80°С — 130 г. Но есть и исключения. Так, растворимость сульфата натрия до 32 °С возрастает, а затем слегка понижается. Аналогично ведет себя весьма плохо растворимый сульфат кальция. Многие жидкости смешиваются с водой в любых соотношениях уже при обычных условиях. К ним относятся сильные минеральные кислоты, спирт. |
Однако существует большое число жидкостей, нерастворимых в воде: анилин, бензол масла и тд.
Растворимость газов в воде в противоположность растворимости твердых веществ понижается с повышением температуры. Следует * отметить, что растворимость большинства газов в воде вообще гораздо ниже, чем растворимость твердых веществ. Исключение составляют газы, вступающие с водой в химические реакции: аммиак, оксид углерода(1У), оксид серы (IV), хлороводород и др.
Некоторые твердые вещества в отдельных случаях могут образовывать перенасыщенные, или пересыщенные растворы, в которых растворенного вещества содержится больше, чем достаточно при данных условиях для насыщения. Получить такие растворы можно при очень медленном, осторожном охлаждении горячего концентрированного раствора. В какой-то момент температура раствора станет
такой, при которой он в соответствии с растворимостью вещества становится насыщенным, а избыток вещества должен выпасть в осадок в виде кристаллов. Этого может не произойти, если отсутствуют так называемые центры кристаллизации. В этом случае в растворе вещества удерживается больше, чем требуется для насыщения, и раствор становится перенасыщенным.
Перенасыщенный раствор — весьма нестойкая система: от легкого толчка или попадания очень малого инородного тела (например, пылинки), которое может послужить центром кристаллизации, из него мгновенно выпадает в осадок избыток растворенного вещества, а раствор становится насыщенным — переходит в устойчивое состояние.
3. В чем отличие перенасыщенного раствора от насыщенного?
4. При каких условиях может образовываться перенасыщенный раствор?
|
из
5.00
|
Обсуждение в статье: Количественный состав растворов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

