 |
Главная |
СТАНДАРТИЗАЦИЯ РАБОЧЕГО РАСТВОРА
|
из
5.00
|
ПЕРМАНГАНАТА КАЛИЯ KMnO4
Перманганат калия обычно содержит ряд примесей, поэтому нельзя считать, что раствор, приготовленный из навески, имеет точную концентрацию, т.е. является стандартным. Кроме того, концентрация перманганата в растворе понижается из-за его взаимодействия с органическими веществами и другими восстановителями, присутствующими в воде.
Раствор перманганата калия должен храниться в склянке из темного стекла, так как под действием света происходит разложение его по реакции:
4 KMnO4 +2 H2O à 4 MnO2 ¯ + 4 KOH + 3O2
Через 5-7 дней после приготовления раствор перманганата калия отфильтровывают через стеклянный фильтр и проводят его стандартизацию.
Молярную концентрацию эквивалента раствора перманганата калия обычно устанавливают по стандартному раствору перекристаллизованного кристаллогидрата щавелевой кислоты Н2С2О4. 2Н2О.
«Редоксометрия»
«Перманганатометрия»
(.Стандартизация титранта по раствору первичного стандарта.
Задание: стандартизировать титрант - раствор KMnO4.
Цель работы: научиться стандартизировать основной титрант метод перманганатометрии - раствор KMnO4, а именно: получить навыки проведения прямого безындикаторного титрования восстановителей в перманганатометрии; закрепить навыки составления ОВ реакций и расчета молярных масс эквивалентов окислителя и восстановителя; закрепить навыки выполнения расчетов нормальности раствора по результатам прямого титрования.
Реактивы: титрант - раствор KMnO4 (приблизительная концентрация 0,05 н.); раствор первичного стандарта -0,05000 н. Na2C2O4; 1 М H2SO4 - для создания среды.
Приборы: электроплитки.
Посуда: бюретки со стеклянным краном; пипетки Мора; мерный цилиндр для отмеривания раствора H2SO4; колбы для титрования (3 шт.); воронки; дозатор для пипеток или резиновая груша.
Ход выполнения работы
Бюретку наполнить раствором KMnO4, точную концентрацию которого следует установить, и готовить ее к работе, как обычно. Так как раствор KMnO4 имеет темную окраску, то нулевое деление на бюретке и отсчеты объема при титровании следует устанавливать и определять по верхнему краю мениска. В колбу для титрования мерным цилиндром внести 10 мл 1 М раствора H2SO4 и 10,00 мл анализируемого раствора Na2C2O4 (пипетка Мора). Содержимое колбы нагреть на плитке до 80...900 С, т.е. до начала запотевания внутренних стенок колбы для титрования (не кипятить!), и титровать горячую реакционную смесь раствором KMnO4. В начале титрования каждую следующую каплю раствора KMnO4 прибавлять лишь после того, как полностью обесцветится окраска от предыдущей капли. Титрование закончить при появлении бледно-розовой окраски, устойчивой в течение 30 с. Повторять титрование до получения трех сходящихся, т.е. отличающихся друг от друга не более чем на 0,1 мл, результатов.
По результатам титрования рассчитать нормальность раствора KMnO4, как обычно при использовании прямого титрования. Результаты занести в таблицу:
Составить уравнение реакции с использованием электронно-ионного метода, определить фактор эквивалентности окислителя и восстановителя и рассчитать молекулярные массы их эквивалентов. Охарактеризовать условия выполнения титрования.
| Номер титрования | Первичный стандарт Na2C2O4 | Титрант KMnO4 | |
| C(1/2Na2C2O4), моль/л | V(Na2C2O4), мл | V(KMnO4), мл | |
| 0,05000 | |||
| 0,05000 | |||
| 0,05000 |
СТАНДАРТИЗАЦИЯ РАСТВОРА ПЕРМАНГАНАТА КАЛИЯ. ПЕРМАНГАНАТОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ПЕРОКСИДА ВОДОРОДА
Задание: стандартизировать титрант - раствор KMnO4.
Цель работы: научиться стандартизировать основной титрант метод перманганатометрии - раствор KMnO4, а именно: получить навыки проведения прямого безындикаторного титрования восстановителей в перманганатометрии; закрепить навыки составления ОВ реакций и расчета молярных масс эквивалентов окислителя и восстановителя; закрепить навыки выполнения расчетов нормальности раствора по результатам прямого титрования.
Реактивы: титрант - раствор KMnO4 (приблизительная концентрация 0,05 н.); раствор первичного стандарта -0,05000 н. Na2C2O4; 1 М H2SO4 - для создания среды, раствор пероксида водорода
Приборы: электроплитки, водяная баня
Посуда: бюретки со стеклянным краном; пипетки Мора; мерный цилиндр для отмеривания раствора H2SO4; колбы для титрования (3 шт.); воронки; дозатор для пипеток или резиновая груша.
1. Стандартизация 0,05 н 1/5KMnO4
Стандартный раствор перманганата калия является вторичным. Приготовление этого раствора имеет ряд особенностей. Свежеприготовленный раствор кипятят в течение 10 минут, а затем выдерживают несколько дней для того, чтобы прошли процессы окисления органических веществ, которые могут содержаться в воде. Образовавшийся осадок MnO2 следует обязательно удалить, так как данное вещество катализирует разрушение перманганата.
4 KMnO4 +2 H2O à 4 MnO2 ¯ + 4 KOH + 3O2
Диоксид марганца отфильтровывают с помощью стеклянного фильтра. Стандартные растворы KMnO4 следует хранить в сосудах тёмного стекла с притёртыми пробками. Стандартизацию растворов следует проводить каждый раз перед применением. В качестве первичного стандарта для стандартизации раствора KMnO4 используют Na2C2O4, H2C2O4×2H2O, Fe, As2O3 и другие вещества. Например:
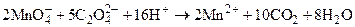
Реакция взаимодействия между перманганат- и оксалат-ионами, протекает медленно, поэтому её проводят при нагревании (около 70°С). Данная реакция является автокаталитической - роль катализатора выполняют ионы Mn2+, образующиеся в ходе реакции.
Cтандартизацию раствора перманганата калия проводят по следующей методике. В 3 колбы для титрования вносят по 10,00 мл 0,05000 М 1/2H2C2O4, прибавляют в каждую колбу по 10 мл 20% (1M) раствора H2SO4, нагревают до температуры примерно 70 °С и медленно титруют стандартизируемым раствором перманганата калия до слабо-розового окрашивания, устойчивого в течение не менее 15 секунд.
Расчёт молярной концентрации 1/5KMnO4 в стандартизируемом растворе проводят по следующей формуле

где С(1/2 H2C2O4) = 0,05000 моль/л, V(1/2 H2C2O4)= 10,00 мл.
|
из
5.00
|
Обсуждение в статье: СТАНДАРТИЗАЦИЯ РАБОЧЕГО РАСТВОРА |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

